フルオロスルホン酸
| フルオロスルホン酸 | |
|---|---|
| |

| |
フルオロスルホン酸 | |
別称 フルオロ硫酸 | |
| 識別情報 | |
| CAS登録番号 | 7789-21-1 |
| EC番号 | 232-149-4 |
| 国連/北米番号 | 1777 |
| RTECS番号 | LP0715000 |
| 特性 | |
| 化学式 | FSO3H |
| モル質量 | 100.06 g/mol |
| 示性式 | FSO2OH |
| 外観 | 無色液体 |
| 密度 | 1.84 g/cm3, 液体 |
| 融点 |
-87.3 ℃ |
| 沸点 |
165.5 ℃ |
| 水への溶解度 | 可溶 |
| 酸解離定数 pKa | -10 |
| 構造 | |
| 分子の形 | 四面体形 |
| 双極子モーメント | N/A |
| 危険性 | |
| 安全データシート(外部リンク) | ICSC 0996 |
| EU分類 | 有害 (Xn) 腐食性 (C) |
| EU Index | 016-018-00-7 |
| Rフレーズ | R20, R35 |
| Sフレーズ | (S1/2), S26, S45 |
| 関連する物質 | |
| 関連物質 | 五フッ化アンチモン トリフルオロメタンスルホン酸 フッ化水素酸 |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
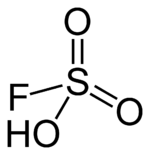
フルオロスルホン酸(フルオロスルホンさん、fluorosulfonic acid)はスルホン酸の一種、一般に入手できる酸の中では最も強いものの1つである。フルオロ硫酸(フルオロりゅうさん、fluorosulfuric acid)とも呼ばれる。硫酸 SO2(OH)2 のヒドロキシ基の1つをフッ素原子に置き換えた、四面体型の構造を持つ分子である。
性質[編集]
粘性の低い無色の液体である。極性の高い有機溶媒(ニトロベンゼン、ジエチルエーテル、酢酸、酢酸エチルなど)に可溶だが、アルカンなど非極性溶媒には溶けない。高い酸性度を持ち、ほとんど全ての有機化合物を溶解するが、これには弱いブレンステッド酸さえも含まれる[1]。ゆっくりと加水分解されてフッ化水素と硫酸になる。一方、類似の構造を持つ化合物であるトリフルオロメタンスルホン酸 CF3SO3H はフルオロスルホン酸と同様に強酸であり、水に対して安定である。
製造[編集]
三酸化硫黄とフッ化水素の反応で合成される。
また、フッ化水素カリウム (KHF2) やフッ化カルシウム (CaF2) を 250 ℃ で発煙硫酸と処理することによっても得られる。不活性ガスを通じてフッ化水素を追い出せばガラス製の装置で蒸留できる[2]。
マジック酸[編集]
カルボラン骨格を持つ化合物がより強い酸として知られているが[3]、フルオロスルホン酸は単純なブレンステッド酸の中では最も強いものの1つである。ルイス酸である五フッ化アンチモンとの組み合わせは「マジック酸」と呼ばれる非常に強いプロトン化剤として知られている。例えばハメットの酸度関数では純フルオロスルホン酸はH0=−15.07、ルイス酸を添加した(FSO3H)0.8・(SbF5)0.2はH0=−20を示す[4]。
用途[編集]
アルカンを異性化させたり、アルケンによって炭化水素をアルキル化する[5]。実験室ではフッ素化剤としても用いられる[2]。
安全性[編集]
毒性および腐食性が高いとされる。加水分解により毒性の高いフッ化水素を発生させる。硫酸の場合と同様、フルオロスルホン酸に水を加えるのは危険である。毒物及び劇物取締法により、毒物として指定された。[6]
出典[編集]
- ^ Encyclopedia of Reagents for Organic Synthesis; Wiley: New York, 2001.
- ^ a b Cotton, F. A.; Wilkinson, G. (1980). Advanced Inorganic Chemistry: A Comprehensive Text (4th ed). Wiley: New York, p. 246.
- ^ Juhasz, M.; Hoffmann, S.; Stoyanov, E.; Kim, K.-C.; Reed, C. A. (2004). "The Strongest Isolable Acid". Angew. Chem., Int. Ed. 43: 5352–5355. doi:10.1002/anie.200460005
- ^ 田中元治『基礎化学選書8 酸と塩基』裳華房、(1971)
- ^ Olah, G.; Farooq, O.; Husain, A.; Ding, N.; Trivedi, N.; Olah, J. (1991) "Superacid FSO3H/HF-Catalyzed Butane Isomerisation". Catalysis Lett. 10: 239–248.
- ^ “国立医薬品食品衛生研究所毒物及び劇物取締法 (毒劇法) 毒物劇物の検索”. www.nihs.go.jp. 国立医薬品食品衛生研究所. 2021年11月23日閲覧。

