膜貫通型タンパク質

膜貫通型タンパク質 (英語: transmembrane protein; TP) は、細胞膜全体に広がる膜内在性タンパク質の一種である。多くの膜貫通型タンパク質は、膜を通過する特定の物質の輸送を可能にするゲートウェイとして機能する。これらのタンパク質は、膜を通して物質を移動させるために、しばしば大きな構造変化を起こす。これらは通常、疎水性が非常に高く、水中で凝集および沈殿する。抽出には界面活性剤や非極性溶媒を必要とするが、一部 (βバレル) は変性剤を用いて抽出することもできる。
膜または膜貫通型セグメントにまたがるペプチド配列、すなわち膜貫通型セグメントは、大部分が疎水性であり、疎水性プロットを用いて可視化することができる[1]。膜貫通型タンパク質は、膜貫通型セグメントの数に応じて、シングルスパン (バイトピックまたは一回膜貫通型) またはマルチスパン (ポリトピックまたは複数回膜貫通型) に分類できる。他のいくつかの膜内在性タンパク質はモノトピックと呼ばれ、それらも永続的に膜に付着しているが、膜を通過(貫通)しないことを意味する[2]。
分類
[編集]構造による分類
[編集]膜貫通型タンパク質には2つの基本的なタイプ[3]、αへリックス型とβバレル型がある。αヘリックス型タンパク質は、細菌細胞の内膜や真核生物の原形質膜に存在し、時には外膜にも存在する[4]。これは膜貫通型タンパク質の主要なカテゴリーである。ヒトでは、全タンパク質の27%がαへリックス膜タンパク質であると推定されている[5]。βバレル型タンパク質は、これまでのところグラム陰性菌の外膜、グラム陽性菌の細胞壁、ミトコンドリアや葉緑体の外膜にしか存在しないか、あるいは膜孔形成毒素として分泌されることがある。すべてのβバレル膜貫通型タンパク質は、最も単純な上下のトポロジーを持っており、これは共通の進化の起源と同様のフォールディング(折り畳み)メカニズムを反映していると考えられる。
タンパク質ドメインに加えて、ペプチドによって形成された珍しい膜貫通要素も存在する。代表的な例は、二量体の膜貫通型βヘリックスを形成するペプチドであるグラミシジンA (Gramicidin A)である[6]。このペプチドは、抗生物質としてグラム陽性菌によって分泌される。膜貫通型ポリプロリンIIヘリックスは、天然タンパク質では報告されていない。しかし、この構造は、特別に設計された人工ペプチドで実験的に観察されている[7]。
トポロジーによる分類
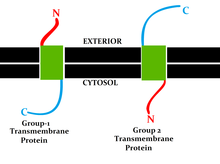
[編集]この分類は、脂質二重層の異なる側にあるタンパク質のN末端とC末端の位置 (英語版) を指す。タイプI、II、III、およびIVはシングルパス分子 (英語版) である。タイプI膜貫通型タンパク質は、ストップ・トランスファー・アンカー配列[訳語疑問点]で脂質膜に固定されており、そのN末端ドメインは、合成時に小胞体(ER)内腔 (成熟型が細胞膜上にある場合は細胞外空間) を標的とする。タイプIIおよびIIIはシグナルアンカー配列[訳語疑問点]で固定されており、タイプIIはそのC末端ドメインで小胞体内腔に標的化され、タイプIIIはそのN末端ドメインで小胞体内腔に標的化される。タイプIVは、そのN末端ドメインが細胞質に標的化されるIV-Aと、N末端ドメインがER内腔に標的化されるIV-Bに細分化されている[8]。4つのタイプでの区分の意味合いは、タンパク質がタイプに依存する方向にER膜を通過しなければならない転座およびER結合翻訳時に特に顕著となる。
3次元構造
[編集]
膜タンパク質の構造は、X線結晶構造解析、電子顕微鏡法、またはNMR分光法によって決定することができる[10]。これらのタンパク質の最も一般的な三次構造は、膜貫通型ヘリックスバンドルとβバレルである。膜タンパク質のうち、脂質二重層 (環状脂質シェルを参照) に付着している部分は、大部分が疎水性アミノ酸で構成されている[11]。
疎水性表面を持つ膜タンパク質は、比較的柔軟性があり、比較的低レベルで発現する。このため、十分なタンパク質を入手し、結晶を成長させることが困難になる。したがって、膜タンパク質は機能的に重要であるにもかかわらず、その原子分解能構造を決定することは球状タンパク質よりも困難である[12]。2013年1月現在、プロテオーム全体の20~30%を占めるにもかかわらず、タンパク質構造が決定された膜タンパク質は0.1%未満である[13]。このような困難さと膜タンパク質の重要性から、疎水性プロットに基づく構造予測法や、ポジティブ・インサイド・ルールなどの手法が開発されてきた[14][15][16]。
熱力学的安定性とフォールディング
[編集]αヘリックス膜貫通型タンパク質の安定性
[編集]膜貫通型αヘリックスタンパク質は、膜内で完全にアンフォールディング(unfolding; 折り畳みの展開)しないため、熱変性の研究から判断すると非常に安定している (完全にアンフォールディングするには、非極性媒体中であまりにも多くのαヘリックス水素結合を切断する必要がある)。一方、これらのタンパク質は、膜内での非天然の凝集、モルテン・グロビュール状態への移行、非天然ジスルフィド結合の形成、または局所的に不安定な周辺領域や非規則的なループのアンフォールディングのために、容易にミスフォールディング(misfold; 誤った折り畳み)する[要出典]。
また、アンフォールド状態を適切に定義することも重要である。界面活性剤ミセル内の膜タンパク質のアンフォールド状態は、熱変性実験の状態とは異なる[要出典]。この状態は、折り畳まれた疎水性αヘリックスと、界面活性剤で覆われた部分的に折り畳まれていないセグメントの組み合わせを表している。例えば、ラウリル硫酸ナトリウム(SDS)ミセル中の「アンフォールド」のバクテリオロドプシンは、4つの膜貫通型αヘリックスが折り畳まれているが、タンパク質の残りの部分はミセルと水の界面に位置しており、さまざまなタイプの非天然両親媒性構造を採ることができる。このような界面活性剤変性状態と天然状態の間の自由エネルギーの差は、水溶性タンパク質の安定性 (< 10 kcal/mol)と同じようなものである[要出典]。
αヘリックス膜貫通型タンパク質のフォールディング
[編集]αヘリックス膜貫通型タンパク質の生体内(in vitro)でのリフォールディング(再折り畳み)は技術的に困難である。バクテリオロドプシンのようにリフォールディング実験に成功した例は比較的少ない。生体内では、そのようなタンパク質はすべて、通常、大きな膜貫通型トランスロコン内で翻訳的に折り畳まれている。トランスロコンチャネルは、発生期の膜貫通型αヘリックスに非常に不均一な環境を提供する。比較的極性の高い両親媒性αヘリックスは、その極性残基がトランスロコンの中央の水で満たされたチャネルに面することができるため、トランスロコン内で膜貫通配向を採ることができる (ただし、膜表面にあるか、生体内ではアンフォールドされていない)。このような機構は、極性αヘリックスを膜貫通型タンパク質の構造に組み込むために必要である。両親媒性ヘリックスは、タンパク質が完全に合成されて折り畳まれるまでトランスロコンに付着したままである。タンパク質が折り畳まれずにトランスロコンに付着したままの状態が長く続くと、タンパク質は特定の「品質管理」細胞系によって分解される[要出典]。
βバレル膜貫通型タンパク質の安定性とフォールディング
[編集]βバレル膜貫通型タンパク質の安定性は、化学的変性研究に基づく水溶性タンパク質の安定性と類似している。βバレル膜貫通型タンパク質の中には、カオトロピック試薬下や高温下でも非常に安定なものがある。それらの生体内(in vivo)でのフォールディングは、タンパク質Skpなどの水溶性シャペロンによって促進される。また、βバレル膜タンパク質は、進化の過程でシートの数が増えたり、2倍になったりしても、同じ祖先に由来すると考えられている。いくつかの研究では、異なる生物間での巨大な配列保存と、構造を保持しフォールディングを助けるアミノ酸も保存されていることが示されている[17]。
3次元構造
[編集]光吸収駆動型トランスポーター
[編集]酸化還元駆動型トランスポーター
[編集]- 膜貫通型シトクロムb様タンパク質: ユビキノール-シトクロムcレダクターゼ (シトクロムbc1複合体); シトクロムb6f複合体; ギ酸脱水素酵素、呼吸性硝酸レダクターゼ; コハク酸デヒドロゲナーゼ(フマル酸還元酵素)。電子伝達系を参照のこと。
- 細菌およびミトコンドリアからのシトクロームcオキシダーゼ
電気化学的 電駆動型トランスポーター
[編集]- プロトン輸送またはナトリウム輸送 F型およびV型ATPアーゼ
P-P結合加水分解駆動型トランスポーター
[編集]- P型カルシウムATPアーゼ (5種類の異なるコンホメーション)
- カルシウムATPアーゼ調節因子ホスホランバンとサルコリピン
- ABCトランスポーター
- 一般分泌経路(Sec)トランスロコン(プレプロティン・トランスロカーゼSecY)
ポーター (単輸送体、共輸送体、対向輸送体)
[編集]- ミトコンドリアキャリアタンパク質
- 主要ファシリテーター・スーパーファミリー (グリセロール-3-リン酸トランスポーター、ラクトースパーミアーゼ、多剤輸送体EmrD)
- 抵抗性結節-細胞分裂 (英語版) (多剤排出トランスポーターAcrB、多剤耐性を参照)
- ジカルボキシレート/アミノ酸: カチオン共輸送体 (プロトングルタミン酸共輸送体)
- 一価カチオン/プロトン対向輸送体 (ナトリウム/プロトン対向輸送体1 NhaA)
- 神経伝達物質ナトリウム共輸送体
- アンモニア輸送体
- 薬物/代謝物輸送体 (小型多剤耐性トランスポーターEmrE - 構造が誤って格納されている)
イオンチャネルを含むα-ヘリカルチャネル
[編集]- カリウムチャネルKcsAやKvAPのような電位依存性イオンチャネル、および内向き整流カリウムイオンチャネルKirbac
- 大導電性機械受容チャネル(MscL)
- 小導電性機械受容性イオンチャネル (MscS)
- CorA金属イオン輸送体 (英語版)
- 神経伝達物質受容体 (アセチルコリン受容体) のリガンド依存性イオンチャネル
- アクアポリン
- 塩化物チャネル
- 外膜補助タンパク質 (多糖トランスポーター) - 細菌外膜からのαヘリックス膜貫通型タンパク質
酵素
[編集]- メタンモノオキシゲナーゼ
- ロンボイドプロテアーゼ
- ジスルフィド結合形成タンパク質 (DsbA-DsbB複合体)
αヘリックス膜貫通型アンカーを持つタンパク質
[編集]- T細胞受容体膜貫通型二量体化ドメイン
- チトクロムc亜硝酸レダクターゼ複合体
- 硫酸ステリルスルホヒドロラーゼ
- スタニン
- グリコホリンA二量体
- イノウイルス(繊維状ファージ)主要コートタンパク質
- ピリン
- 肺サーファクタント関連タンパク質
- モノアミンオキシダーゼAおよびB
- 脂肪酸アミド加水分解酵素[18]
- シトクロムP450オキシダーゼ
- コルチコステロイド11β-デヒドロゲナーゼ。
- シグナルペプチドペプチダーゼ
- ストマチン相同体に特異的な膜プロテアーゼ
単一のポリペプチド鎖からなるβバレル
[編集]- 8つのβストランドからかるβバレルで、「せん断数」が10 (n=8、S=10)。次が含まれる。
- OmpAのような膜貫通型ドメイン (OmpA)
- 病原性関連外膜タンパク質ファミリー (OmpX)
- 外膜タンパク質Wファミリー (OmpW)
- 抗菌ペプチド耐性および脂質Aアシル化タンパク質ファミリー(PagP)
- リピドAデアシラーゼPagL
- 透過性ファミリーポリン (NspA)
- オートトランスポータードメイン (n=12、S=14)
- FadL外膜タンパク質輸送体ファミリー、脂肪酸輸送体FadL (n=14、S=14) を含む
- 三量体ポリンとして知られる一般的な細菌ポリンファミリー (n=16、S=20))
- マルトポリン、またはシュガーポリン (sugar porins) (n=18、S= 22)
- ヌクレオシド特異的ポリン (n=12、S=16)
- 外膜ホスホリパーゼA1 (n=12、S=16)
- TonB依存受容体とそのプラグドメイン。それらは、リガンド依存性外膜チャネル (n=22、S=24) であり、コバラミン輸送体BtuB、Fe(III)-ピオケリン受容体FptA、受容体FepA、ヒドロキサメート鉄吸収受容体FhuA、輸送体FecA、およびピオバジン受容体FpvAを含む
- 外膜プロテアーゼOmpTおよびアドヘシン/インベイシンOpcAタンパク質を含む外膜タンパク質OpcAファミリー (n=10、S=12)
- 外膜タンパク質Gポリンファミリー (n=14、S=16)
注: nとSは、それぞれβストランド数とβバレルの「せん断数」[19]である。
複数のポリペプチド鎖からなるβバレル
[編集]- 三量体オートトランスポーター (n=12、S=12)
- 外膜排出タンパク質、TolCや多剤耐性タンパク質を含む三量体外膜因子 (n=12、S=18) としても知られている
- MspAポリン (オクタマー、 n=S=16) および α溶血素 (ヘプタマー n=S=14)。これらのタンパク質は分泌される。
参照項目
[編集]脚注
[編集]- ^ Manor, Joshua; Feldblum, Esther S.; Arkin, Isaiah T. (2012). “Environment Polarity in Proteins Mapped Noninvasively by FTIR Spectroscopy”. The Journal of Physical Chemistry Letters 3 (7): 939–944. doi:10.1021/jz300150v. PMC 3341589. PMID 22563521.
- ^ Steven R. Goodman (2008). Medical cell biology. Academic Press. pp. 37–. ISBN 978-0-12-370458-0 24 November 2010閲覧。
- ^ Jin Xiong (2006). Essential bioinformatics. Cambridge University Press. pp. 208–. ISBN 978-0-521-84098-9 13 November 2010閲覧。
- ^ alpha-helical proteins in outer membranes include Stannin and certain lipoproteins, and others
- ^ “Mapping the human membrane proteome: a majority of the human membrane proteins can be classified according to function and evolutionary origin”. BMC Biol. 7: 50. (2009). doi:10.1186/1741-7007-7-50. PMC 2739160. PMID 19678920.
- ^ Nicholson, L. K.; Cross, T. A. (1989). “Gramicidin cation channel: an experimental determination of the right-handed helix sense and verification of .beta.-type hydrogen bonding” (英語). Biochemistry 28 (24): 9379–9385. doi:10.1021/bi00450a019. PMID 2482072.
- ^ Kubyshkin, Vladimir; Grage, Stephan L.; Ulrich, Anne S.; Budisa, Nediljko (2019). “Bilayer thickness determines the alignment of model polyproline helices in lipid membranes” (英語). Physical Chemistry Chemical Physics 21 (40): 22396–22408. Bibcode: 2019PCCP...2122396K. doi:10.1039/c9cp02996f. PMID 31577299.
- ^ Harvey Lodish etc.; Molecular Cell Biology, Sixth edition, p.546
- ^ Goder, Veit; Spiess, Martin (31 August 2001). “Topogenesis of membrane proteins: determinants and dynamics”. FEBS Letters 504 (3): 87–93. doi:10.1016/S0014-5793(01)02712-0. PMID 11532438.
- ^ Cross, Timothy A.; Sharma, Mukesh; Yi, Myunggi; Zhou, Huan-Xiang (2011). “Influence of Solubilizing Environments on Membrane Protein Structures”. Trends in Biochemical Sciences 36 (2): 117–125. doi:10.1016/j.tibs.2010.07.005. PMC 3161620. PMID 20724162.
- ^ White, Stephen. "General Principle of Membrane Protein Folding and Stability". Stephen White Laboratory Homepage. 10 Nov. 2009. web.[要検証]
- ^ Carpenter, Elisabeth P; Beis, Konstantinos; Cameron, Alexander D; Iwata, So (October 2008). “Overcoming the challenges of membrane protein crystallography”. Current Opinion in Structural Biology 18 (5): 581–586. doi:10.1016/j.sbi.2008.07.001. PMC 2580798. PMID 18674618.
- ^ Membrane Proteins of known 3D Structure
- ^ Elofsson, Arne; Heijne, Gunnar von (7 June 2007). “Membrane Protein Structure: Prediction versus Reality”. Annual Review of Biochemistry 76 (1): 125–140. doi:10.1146/annurev.biochem.76.052705.163539. PMID 17579561.
- ^ Chen, Chien Peter; Rost, Burkhard (2002). “State-of-the-art in membrane protein prediction”. Applied Bioinformatics 1 (1): 21–35. PMID 15130854.
- ^ Hopf, Thomas A.; Colwell, Lucy J.; Sheridan, Robert; Rost, Burkhard; Sander, Chris; Marks, Debora S. (June 2012). “Three-Dimensional Structures of Membrane Proteins from Genomic Sequencing”. Cell 149 (7): 1607–1621. doi:10.1016/j.cell.2012.04.012. PMC 3641781. PMID 22579045.
- ^ Michalik, Marcin; Orwick-Rydmark, Marcella; Habeck, Michael; Alva, Vikram; Arnold, Thomas; Linke, Dirk; Permyakov, Eugene A. (3 August 2017). “An evolutionarily conserved glycine-tyrosine motif forms a folding core in outer membrane proteins”. PLOS ONE 12 (8): e0182016. Bibcode: 2017PLoSO..1282016M. doi:10.1371/journal.pone.0182016. PMC 5542473. PMID 28771529.
- ^ “Structural adaptations in a membrane enzyme that terminates endocannabinoid signaling”. Science 298 (5599): 1793–6. (November 2002). Bibcode: 2002Sci...298.1793B. doi:10.1126/science.1076535. PMID 12459591.
- ^ “Principles determining the structure of beta-sheet barrels in proteins. I. A theoretical analysis”. J. Mol. Biol. 236 (5): 1369–81. (March 1994). doi:10.1016/0022-2836(94)90064-7. PMID 8126726.
