トリクロロ酢酸
| トリクロロ酢酸 | |
|---|---|
| |
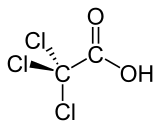
Trichloroethanoic acid | |
| 識別情報 | |
| CAS登録番号 | 76-03-9 |
| KEGG | C11150 |
| |
| 特性 | |
| 化学式 | C2HCl3O2 |
| モル質量 | 163.4 |
| 示性式 | CCl3COOH |
| 外観 | 白色固体 |
| 密度 | 1.6 |
| 相対蒸気密度 | 5.6 |
| 融点 |
58 °C, 331 K, 136 °F |
| 沸点 |
198 °C, 471 K, 388 °F |
| 出典 | |
| 国際化学物質安全性カード | |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
トリクロロ酢酸(トリクロロさくさん、trichloroacetic acid, TCA)は、酢酸のメチル基の3つの水素原子を塩素原子に置換したカルボン酸である。
性質
常温で白色結晶である。潮解性、腐食性を持つ。水によく溶けるほか、エタノール・エーテル類にもよく溶ける。カルボン酸としては酸性が強く、酢酸の約1万倍の強さである。日本では毒物及び劇物取締法により劇物に指定されている。
合成法
触媒の存在下、酢酸に塩素分子を反応させることで合成される。
利用
生化学の分野ではDNAやRNA、タンパク質等の沈殿剤として利用されることがある。またナトリウム塩は除草剤としても用いられることがある。
皮膚を薬剤で処理して再生させるケミカルピーリングの薬剤として、美容整形(皺消し)、イボ(疣贅)[1]や尖圭コンジローマの除去<などに、モノクロロ酢酸同様に用いられる。
小史
トリクロロ酢酸は1840年にジャン=バティスト・デュマによって見出された。[2] この化合物は、当時正電荷を持つと考えられていた水素と負電荷を持つと考えられていた塩素が置換可能であることを示していた。これはイェンス・ベルセリウスが中心となって考えられていた電気化学的二元論や、デュマ自身のエテリン説と矛盾しており、後の原子価説につながる画期的な発見であった。
出典
- ^ 江川 清文. トリクロロ酢酸が著効した小児難治性疣贅の2例. 西日本皮膚科. 2017;79(4):391-395. DOI https://doi.org/10.2336/nishinihonhifu.79.391
- ^ Dumas (1840). “Trichloroacetic acid”. Annalen der Chemie XXXII: 101.
外部リンク
- SIDS初期評価プロファイル(化学物質安全・情報センター)

