ボロン酸

ボロン酸 (ボロンさん、英: boronic acid) はホウ酸のヒドロキシ基をアルキル基やアリール基で置換したものであり、炭素-ホウ素結合を含んでいる。ボロン酸はルイス酸としてはたらく。これらの化合物の特徴は、糖、アミノ酸、ヒドロキサム酸などと可逆な共有結合錯体をつくることである。ボロン酸の pKa はおよそ 9 であるが、水溶液中で四面体型構造をとったボロン酸錯体の pKa はおよそ 7 である。糖と結合したボロン酸は、蛍光の検出や、膜を横切る糖類の選択輸送のトレースなど、分子認識の分野で使用される。
ボロン酸は有機化学で広く登場し、鈴木・宮浦カップリングの主要な中間体でもある。ボロン酸の有機残基における遷移金属のトランスメタル化は、特に重要な概念である。
ボロン酸誘導体であるボルテゾミブという化合物は化学療法の薬として使われる。この分子のホウ素原子は、あるプロテアソームを阻害したり、タンパク質を分解する役割がある。
ボロン酸[編集]
空気中で安定な多くのボロン酸は、商業的に利用できる。高い融点を持つのが特徴である。ボロン酸はすぐに脱水して環状三量体無水物であるボロキシンをつくるので、商業的に販売されているものはかなりの割合でこのような無水物を含んでいる。だが、このことは反応そのものには影響しない。
| ボロン酸 | R | 構造式 | 分子量 | CAS登録番号 | 融点 (°C) |
|---|---|---|---|---|---|
| フェニルボロン酸 | フェニル基 | 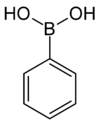 |
121.93 | 98-80-6 | 216-219 |
| 2-チオフェンボロン酸 | チオフェン |  |
127.96 | 6165-68-0 | 138-140 |
| メチルボロン酸 | メチル基 |  |
59.86 | 13061-96-6 | 91-94 |
| cis-プロペニルボロン酸 | プロペン | 85.90 | 7547-96-8 | 65-70 | |
| trans-プロペニルボロン酸 | プロペン | 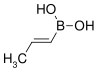 |
85.90 | 7547-97-9 | 123-127 |
| 代表的なボロン酸 | |||||
ボロン酸エステル[編集]
ボロン酸エステル (英: boronate ester) はボロン酸とアルコールからつくられるエステルである。
| 化合物 | 一般化学式 | 一般構造式 |
|---|---|---|
| ボロン酸 |  | |
| ボロン酸エステル |  | |
| ボロン酸とボロン酸エステルの比較 | ||
ボロン酸エステルはホウ酸エステルとアルコールまたはジオールの縮合反応により得られる[1]。フェニルボロン酸は自己縮合してトリフェニル無水物またはトリフェニルボロキシンとよばれる環状三量体をつくる[2]。
| ボロン酸エステル | ジオール | 構造式 | 分子量 | CAS登録番号 | 沸点 (°C) |
|---|---|---|---|---|---|
| アリルボロン酸ピナコラート | ピナコール |  |
168.04 | 72824-04-5 | 50-53 (5 mmHg) |
| 2-フェニル-1,3,2-ジオキサボリナン | トリメチレングリコール |  |
161.99 | 4406-77-3 | 106 (2 mmHg) |
| ジイソプロポキシメチルボラン | イソプロパノール | 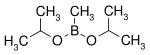 |
144.02 | 86595-27-9 | 105 -107 |
| 代表的なボロン酸エステル | |||||
C-O-B-O-C のような五員環を持つ化合物はジオキサボロランとよばれ、同じく六員環を持つものはジオキサボリナンとよばれる。
ボリン酸とそのエステル[編集]
ボリン酸 (英: borinic acid) とボリン酸エステル (英: borinate ester) は一般構造は R2BOR と表される。
| 化合物 | 一般化学式 | 一般構造式 |
| ボリン酸 | R2BOH |  |
| ボリン酸エステル | R2BOR |  |
出典[編集]
- ^ R. L. Kidwell, M. Murphy, and S. D. Darling (1973). "Phenols: 6-Methoxy-2-Naphthol". Organic Syntheses (英語).; Collective Volume, vol. 5, p. 918
- ^ Robert M. Washburn, Ernest Levens, Charles F. Albright, and Franklin A. Billig (1963). "Benzeneboronic Anhydride". Organic Syntheses (英語).; Collective Volume, vol. 4, p. 68


