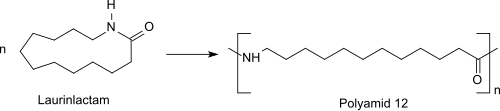
ラウロラクタム
| ラウロラクタム | |
|---|---|

| |
azacyclotridecan-2-one | |
| 識別情報 | |
| CAS登録番号 | 947-04-6 |
| PubChem | 13690 |
| |
| 特性 | |
| 化学式 | C12H23NO |
| モル質量 | 197.32 g mol−1 |
| 外観 | 白色固体 |
| 融点 |
152.5 °C |
| 水への溶解度 | 0.03 wt% |
| 危険性 | |
| 引火点 | 192 °C |
| 発火点 | 320 - 330 °C |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
ラウロラクタム (Laurolactam) は大環状ラクタムのグループに属する有機化合物である。主としてナイロン-12 やコポリアミドなどのエンジニアリングプラスチックの原料として用いられる[1]。
合成
[編集]ラウロラクタムは、12-アミノドデカン酸の誘導体だが、シクロドデカトリエンから作られる。シクロドデカトリエンは水素化されて飽和アルカンのシクロドデカンになる。ラウロラクタムの製造では、ホウ酸と遷移金属塩、例えば酢酸コバルト(II)の存在下で空気または酸素でシクロドデカンを酸化することによりシクロドデカノール(英語: Cyclododecanol)とシクロドデカノンの混合物を得る[2]。この混合物は、銅接触触媒上で定量的に脱水素化されシクロドデカノンになり、ヒドロキシルアミンと反応してシクロドデカノンオキシム(英語: Cyclododecanoneoxime)になる。オキシムは、強酸の存在下でベックマン転位でラウロラクタムに転位する[3][4][5]。

別の製造法は、無水塩化水素の存在下での、塩化ニトロシル[2]によるシクロドデカンの光ニトロソ化である[6]。得られたシクロドデカノンオキシムを濃硫酸で抽出し、160 °Cに加熱してラウロラクタムに転位させる。全体の収率 (光窒素化 + ベックマン転位) は最大 93%である[1]。
性質
[編集]ラウロラクタムは水に不溶の結晶性固体である。工業用品質のものはベージュ色だが、純粋なもの (99.9%) は白色である。多くの有機溶媒、例えば 1,4-ジオキサン、ベンゼン、シクロヘキサンに溶ける。精製は、従来の多段減圧蒸留で行われる。蒸留と、溶液または溶融状態からの結晶化を組み合わせると非常に高純度 (>99%) のラウロラクタムが得られる[7]。ラウロラクタムによるリスクは低いと考えられている。
使用
[編集]モノマーをナイロン-12 に重合させるには開環重合が使用される。反応はカチオンまたはアニオン開始剤または水を用いて行われる。酸によるカチオン重合は、最初に O-プロトン化が起こると考えられる。反応性プロトン化窒素へのモノマーの求核攻撃と、それに続く一級アミンの連続的な開環アシル化により、ポリアミドが形成される[8]。300 °C 減圧化での水の添加により、モノマーのラウロラクタムの開環重合は、最初にプレポリマーへと進行する。このプレポリマーは、その後の重縮合で常圧または減圧、約 250 °Cで高分子のポリアミド (PA 12:-[NH-(CH2)11-CO]n-)へと反応して行く[9]。
ラウロラクタムは、コポリアミド 6/12 製造のためにε-カプロラクタムと共に使われる[10]
脚注
[編集]- ^ a b T. Schiffer, G. Oenbrink: Cyclododecanol, Cyclododecanone, and Laurolactam. In: Ullmann's Encyclopedia of Industrial Chemistry. Wiley-VCH, Weinheim 2002, doi:10.1002/14356007.a08_201.
- ^ a b H.-J. Arpe: Industrielle Organische Chemie. 6., vollst. überarb. Aufl., Wiley-VCH Verlag, Weinheim, 2007, ISBN 978-3-527-31540-6.
- ^ Douglass F. Taber, Patrick J. Straney (December 2010), [PDF “The Synthesis of Laurolactam from Cyclododecanone via a Beckmann Rearrangement”] (German), Journal of Chemical Education 87 (12): pp. 1392, Bibcode: 2010JChEd..87.1392T, doi:10.1021/ed100599q
- ^ Patent US8309714: Process for producing laurolactam. invent1: J. Kugimoto et al., assign1: Ube Industries, Ltd., erteilt am 13. Nov. 2012.
- ^ Y. Furuya et al.: Cyanuric Chloride as a Mild and Active Beckmann Rearrangement Catalyst. In: J.Am.Chem.Soc. 127, Nr. 32, 2005, S. 11240–11241, doi:10.1021/ja053441x
- ^ US 6197999, J. Ollivier, D. Drutel, issued 2001-03-06, assigned to Atofina
- ^ US 8399658, A. Hengstermann et al., "Method for isolation of laurolactam from a laurolactam synthesis process stream", issued 2013-03-19, assigned to Evonik Degussa GmbH
- ^ Stevens, M. P. Polymer Chemistry: An Introduction, Oxford University Press: New York, 1999.
- ^ US 5362448, A. Kawakami et al., "Continuous polymerization method of laurolactam and apparatus therefor", issued 1994-11-08, assigned to Ube Industries, Ltd.
- ^ DE 3730504, E. De Jong et al., "Copolyamides containing caprolactam and laurolactam, process for the preparation thereof and use thereof for heat-sealing textiles", issued 1989-03-16, assigned to Atochem Werke GmbH