ムレキシド
| ムレキシド | |
|---|---|
| |
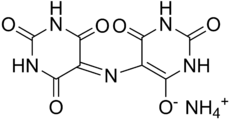
Ammonium 2,6-dioxo-5-[(2,4,6-trioxo-5-hexahydropyrimidinylidene)amino]-3H-pyrimidin-4-olate | |
別称 プルプル酸アンモニウム、アンモニウムプルプラート | |
| 識別情報 | |
| CAS登録番号 | 3051-09-0 [6032-80-0] (hydrate) |
| PubChem | 18275 |
| ChemSpider | 17264 |
| |
| |
| 特性 | |
| 化学式 | C8H8N6O6 |
| モル質量 | 284.19 g mol−1 |
| 危険性 | |
| Rフレーズ | R20 R21 R22 |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
ムレキシド(Murexide)は、プルプル酸のアンモニウム塩である。プルプル酸アンモニウム、アンモニウムプルプラートとも[1]。気体アンモニア中でアロキサンチンを100℃以上に加熱するか、酸化水銀中で5-アミノバルビツール酸を加熱することによって生成する。ウォルター・ハートリー[2]は、吸収スペクトルで調べた時に十分に純粋なムレキシドを得ることが難しいことを見出し、ムレキシドの新しい生成法を開発した。この方法では、アロキサンチンを沸騰した大量の無水アルコールに溶解させ、乾燥した気体アンモニアを溶液中に約3時間通す。この溶液から沈殿物を濾し取り、無水アルコールで洗って乾燥させる。この方法で得られた塩は、無水状態である。また、アルコール性アンモニア中で約75℃でアロキサンを昇華することによっても得られる。形成された紫色の固体は水に容易に溶け、この溶液は、ムレキシドの溶液と区別が付かなくなる。
乾燥状態のムレキシドの外観は赤紫色の粉末で、若干水に溶ける。溶液の色は、強い酸性では黄色、弱い酸性では赤紫色、アルカリ性では青紫色である。カルシウム滴定のpHは、11.3である。
ドイツのユストゥス・フォン・リービッヒとフリードリヒ・ヴェーラーは、1830年代にヘビの排泄物から紫色の物質であるムレキシドを発見していたが、非常に含有量が少なく、これを染料に用いる方法は、当時は確立されなかった[3]。1850年代、パリのDepoully等のフランスの染色業者は、南アメリカの糞の堆積物から大量のムレキシドを抽出し、これを用いて天然の繊維を染色することに成功した。その後、この方法は、イギリス、フランス、ドイツに広がった。
分析化学においては、ムレキシドは、錯滴定指示薬として用いられている。カルシウムイオンに対して最も多く用いられるが、銅、ニッケル、コバルト、トリウムや希土類元素に対しても用いられる。この目的に用いる量が少なくて済むことから、しばしば1:250の硫酸カリウム混合物として用いられる。
ムレキシドは、カルシウムや希土類金属の測定のための比色分析試薬としても用いられる。カルシウムに対しては、必要なpHは11.3で、0.2から1.2 ppmの範囲で検出できる。極大吸収波長は、506 nmである。
ムレキシドとメチルレッドは、有機塩素化合物汚染物質に対する音響破壊の促進剤としての利用も期待されている。
出典
[編集]- ^ 日本化学物質辞書Web 日化辞番号:J9.520F
- ^ Some information on the chemist Walter Noel Hartley is available here
- ^ Peter J. T. Morris and Anthony S. Travis (November 1992), “A History of the International Dyestuff Industry”, American Dyestuff Reporter 81 (11)
 この記事にはアメリカ合衆国内で著作権が消滅した次の百科事典本文を含む: Chisholm, Hugh, ed. (1911). "Murexide". Encyclopædia Britannica (英語). Vol. 19 (11th ed.). Cambridge University Press. p. 34.
この記事にはアメリカ合衆国内で著作権が消滅した次の百科事典本文を含む: Chisholm, Hugh, ed. (1911). "Murexide". Encyclopædia Britannica (英語). Vol. 19 (11th ed.). Cambridge University Press. p. 34.
