グリオトキシン
表示
| グリオトキシン | |
|---|---|
| |
| |
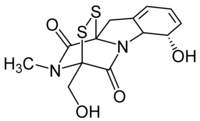
(3R,6S,10aR)-6-hydroxy-3-(hydroxymethyl)-2-methyl-2,3,6,10-tetrahydro-5aH-3,10a-epidithiopyrazino[1,2-a]indole-1,4-dione | |
| 識別情報 | |
| CAS登録番号 | 67-99-2 |
| PubChem | 6223 |
| ChemSpider | 5988 |
| ChEMBL | CHEMBL331627 |
| |
| |
| 特性 | |
| 化学式 | C13H14N2O4S2 |
| モル質量 | 326.39 g mol−1 |
| 外観 | 白から黄白色の固体 |
| 密度 | 1.75 g/ml |
| DMSOへの溶解度 | soluble |
| 危険性 | |
| 安全データシート(外部リンク) | MSDS from Fermentek |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
グリオトキシン (Gliotoxin) は天然ジケトピペラジン類に属する含硫黄マイコトキシンであり[1]、特に数種の海産菌類が産生する。ジケトピペラジンが複数の硫黄原子で架橋された構造を持つepipolythiopiperazine類としては最も著名なものである。これらの化合物は高い生物学的活性を持ち、新規治療法の開拓を目指した多数の研究の対象となってきた[2]。グリオトキシンはボタンタケ科に属するGliocladium fimbriatum から最初に単離され、その学名から命名された。
発生源
[編集]Aspergillus fumigatus[3]、トリコデルマ属、アオカビ属等に属するヒト病原体が産生する。カンジダ属の酵母による産生も報告されている[4]が、他の研究ではカンジダ属による産生は疑わしいものとされている[5][6]。
作用
[編集]免疫抑制作用を有し、好中球・好酸球等の顆粒球、マクロファージ、胸腺細胞等の免疫系の細胞にアポトーシスを引き起こす。In vivoにおいては抗炎症作用が示されている。細胞膜上のチオール基と結合することで様々な微生物に対して毒性を示し[7]、1940年代頃から抗生物質・抗真菌薬、後には抗ウイルス薬としての研究も行われてきた[8]。ファルネシルトランスフェラーゼの阻害剤、20Sプロテアソームのキモトリプシン様活性部位の非競合阻害剤としての作用も有する。
脚注
[編集]- ^ Borthwick AD (2012). “2,5-Diketopiperazines: Synthesis, Reactions, Medicinal Chemistry, and Bioactive Natural Products”. Chemical Reviews 112 (7): 3641–3716. doi:10.1021/cr200398y. PMID 22575049.
- ^ Jiang, C.-S.; Muller, W. E. G.; Schroder, H. C.; Guo, Y.-W., "Disulfide- and Multisulfide-Containing Metabolites from Marine Organisms", Chem. Rev. 2012, 112, 2179-2207, doi:10.1021/cr200173z.
- ^ Scharf, Daniel H and Heinekamp, Thorsten and Remme, Nicole and Hortschansky, Peter and Brakhage, Axel A and Hertweck, Christian (2012). “Biosynthesis and function of gliotoxin in Aspergillus fumigatus”. Applied microbiology and biotechnology (Springer) 93: 467-472. doi:10.1007/s00253-011-3689-1. PMID 22094977.
- ^ Shah, Darshana T and Larsen, Bryan (1991). “Clinical isolates of yeast produce a gliotoxin-like substance”. Mycopathologia (Springer) 116: 203-208. doi:10.1007/BF00436836. (
 要購読契約)
要購読契約)
- ^ Kupfahl C, Ruppert T, Dietz A, Geginat G, Hof H (2007). "Candida species fail to produce the immunosuppressive secondary metabolite gliotoxin in vitro". FEMS Yeast Res. 7 (6): 986–92. doi:10.1111/j.1567-1364.2007.00256.x. PMID 17537180。
- ^ Kosalec I, Puel O, Delaforge M, Kopjar N, Antolovic R, Jelic D, Matica B, Galtier P, Pepeljnjak S (2010). "Isolation and cytotoxicity of low-molecular-weight metabolites of Candida albicans". Front Biosci. 13: 6893–904. doi:10.2741/3197. PMID 18508703。
- ^ Jones, Richard W., and Joseph G. Hancock. (1988). “Mechanism of gliotoxin action and factors mediating gliotoxin sensitivity”. Microbiology 134 (7): 2067-2075. doi:10.1099/00221287-134-7-2067 2024年7月20日閲覧。.
- ^ McDougall, J. K. (November 30, 1968), “Antiviral action of gliotoxin”, Archives of Virology
参考文献
[編集]- MÜLLBACHER, ARNO and WARING, *PAUL and EICHNER, RONALD D. (1985). “Identification of an agent in cultures of Aspergillus fumigatus displaying anti-phagocytic and immunomodulating activity in vitro”. Microbiology (Microbiology Society) 131 (5): 1251-1258. doi:10.1099/00221287-131-5-1251.
- Schweizer, Matthias and Richter, Christoph (1994). “Gliotoxin stimulates Ca2+ release from intact rat liver mitochondria”. Biochemistry (ACS Publications) 33 (45): 13401-13405. doi:10.1021/bi00249a028.
外部リンク
[編集]- Puri, A., Ahmad, A. and Panda, B. P. (2010), Development of an HPTLC-based diagnostic method for invasive aspergillosis. Biomed. Chromatogr., 24: 887–892. doi:10.1002/bmc.1382.
- Gliotoxin product page from Fermentek
