(ジクロロヨード)ベンゼン
| (ジクロロヨード)ベンゼン[1] | |
|---|---|
|

|
(dichloro-λ3-iodanyl)benzene | |
別称 ヨードベンゼンジクロリド 二塩化ヨードベンゼン ヨードソベンゼンジクロリド フェニルヨウ素(III)ジクロリド フェニルヨードソジクロリド フェニルクロロヨードニウムクロリド ヨードジクロロベンゼン | |
| 識別情報 | |
| 略称 | IBD |
| CAS登録番号 | 932-72-9 |
| |
| 特性 | |
| 化学式 | C6H5Cl2I |
| モル質量 | 274.91 g mol−1 |
| 外観 | 黄色固体 |
| 密度 | 2.2 g/cm3 |
| 融点 |
115–120 °C(分解) |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
(ジクロロヨード)ベンゼン (英: (dichloroiodo)benzene) は、ヨードベンゼンの塩素錯体である。酸化剤として使われる。
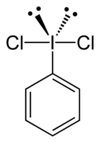
単結晶X線回折が構造決定のために使われた。VSEPR則によって予測されるように、中央のヨウ素原子はT字形構造をとっている[2][3]。
性質[編集]
(ジクロロヨード)ベンゼンは安定でなく、一般には商業利用可能でない。これはヨードベンゼンのクロロホルム溶液に塩素を通じることによって、沈殿として得られる[4]。同じ反応がパイロットプラントスケール (20 kg) で報告された[5]。
- PhI + Cl2 → PhICl2
塩酸中の次亜塩素酸ナトリウムの作用によって、in situ に生成する塩素による代替合成法も記述された[6]。
反応[編集]
(ジクロロヨード)ベンゼンは塩基性溶液で加水分解され、ヨードシルベンゼン (PhIO) を与える[7]。また、次亜塩素酸ナトリウムによって酸化され、ヨードキシベンゼン (PhIO2) を与える[8]。
有機合成において、(ジクロロヨード)ベンゼンはアルケン[1]やアルキン[9]の選択的塩素化の試薬として用いられる。
出典[編集]
- ^ a b Phenyliodine(III) Dichloride, David W. Knight and Glen A. Russell, in Encyclopedia of Reagents for Organic Synthesis, 2001, John Wiley & Sons, Ltd doi:10.1002/047084289X.rp071
- ^ E. M. Archer and T. G. van Schalkwy (1953), “The crystal structure of benzene iododichloride”, Acta Cryst. 6: 88–92, doi:10.1107/S0365110X53000193
- ^ J. V. Carey, P. A. Chaloner, P. B. Hitchcock, T. Neugebauer, K. R. Seddon (1996), J. Chem. Res. 358: 2031–
- ^ H. J. Lucas and E. R. Kennedy. "Iodobenzene dichloride". Organic Syntheses (英語).; Collective Volume, vol. 3, p. 482
- ^ Zanka, Atsuhiko; Takeuchi, Hiroki; Kubota, Ariyoshi (1998), “Large-Scale Preparation of Iodobenzene Dichloride and Efficient Monochlorination of 4-Aminoacetophenone”, Organic Process Research & Development 2: 270, doi:10.1021/op980024e
- ^ Zhao, Xue-Fei; Zhang, Chi (2007), “Iodobenzene Dichloride as a Stoichiometric Oxidant for the Conversion of Alcohols into Carbonyl Compounds; Two Facile Methods for Its Preparation”, Synthesis 2007: 551, doi:10.1055/s-2007-965889
- ^ H. J. Lucas, E. R. Kennedy, and M. W. Formo (1955). "Iodosobenzene". Organic Syntheses (英語).; Collective Volume, vol. 3, p. 483
- ^ M. W. Formo and John R. Johnson (1955). "Iodoxybenzene: B. Hypochlorite oxidation of iodobenzene dichloride". Organic Syntheses (英語).; Collective Volume, vol. 3, p. 485
- ^ Michael E. Jung and Michael H. Parker (1997), “Synthesis of Several Naturally Occurring Polyhalogenated Monoterpenes of the Halomon Class”, Journal of Organic Chemistry 62 (21): 7094–7095, doi:10.1021/jo971371, PMID 11671809
参考文献[編集]
- Tanner, Dennis D; Van Bostelen, P. B. (1967), “Free-radical chlorination reactions of iodobenzene dichloride”, Journal of Organic Chemistry 32: 1517–1521, doi:10.1021/jo01280a047
