カルボニルジイミダゾール
| カルボニルジイミダゾール | |
|---|---|
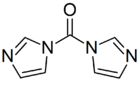 | |
| IUPAC名 | 1,1'-カルボニルジイミダゾール ジ(1H-イミダゾール-1-イル)メタノン |
| 分子式 | C7H6N4O |
| 分子量 | 162.15 |
| CAS登録番号 | 530-62-1 |
| 形状 | 白色微粉末 |
| 融点 | 119 °C |
| SMILES | C(=O)(N1C=NC=C1)N2C= CN=C2 |
カルボニルジイミダゾール (carbonyldiimidazole) はペプチド合成におけるアミノ酸のカップリング剤など、有機合成に用いられる試薬である。CDIと略称される。イミダゾール環をImと略記し、Im2C=Oと表されることもある。
調製[編集]
ホスゲンと4当量のイミダゾールの反応で得られる。副生物の塩化イミダゾリウムと溶媒を除去すると、およそ 90% の収率で結晶性の生成物として得られる[1]。1-(トリメチルシリル)イミダゾールを用いても同様に調製できるが、原料の入手が煩雑になるだけで、特に利点は無い[2]。
- 4 ImH + Cl2C=O → Im2C=O + 2 ImH·HCl
容易に加水分解されてイミダゾールと二酸化炭素を生じる。
- Im2C=O + H2O → 2 ImH + CO2
この反応で発生する二酸化炭素は CDI と等物質量なので、これを定量することによって CDI の純度を決定できる[3]。
有機合成での利用[編集]
イミダゾールの脱離能の高さを生かし、アルコールやアミンをカルバメート、エステル、尿素、炭酸エステルに変換するのに用いられる[1]。
- Im2C=O + HX → ImC(=O)X + ImH (X = OR, NRR')
カルボン酸誘導体[編集]
上記の反応の一般的な利用法はカルボン酸誘導体のアシル基移動である。CDI の反応性はカルボン酸クロリドと近いが、取り扱いがより簡便で適用範囲も広い[3]。初期の適用例として、ペプチドやカルボン酸のイミダゾール誘導体合成がある。二酸化炭素の生成がこの反応の駆動力である。
- Im2C=O + RC(=O)OH → RC(=O)Im + ImH + CO2
- RC(=O)Im + XH → RC(C=O)X + ImH
ペプチド合成の分野では、生成物 RC(=O)Im をアミノ酸やペプチドエステルで処理してカップリングを行う。副生物の二酸化炭素とイミダゾールは比較的無害である[4]。反応条件が穏やかなため、アミノ酸のラセミ化はほとんど起こらない。
エステル化に用いることもできるが、アルコールとの反応は加熱かナトリウムエトキシドのような求核剤を必要とする[1][3]。一般的に収率は高く、適用範囲も広い。グリコシド結合を形成するのにも使える[5]。ただし、比較的 α プロトンの酸性度が高いカルボン酸を三級アルコールでエステル化するのは困難で、クライゼン縮合が起こりやすい(この目的に CDI が利用されることもある)[1]。同様な反応はチオールやセレノールでも起こり、対応するエステルを与える[6]。
アルコールの代わりにカルボン酸を用いると酸無水物が得られる。反応の平衡は、2当量のトリフルオロ酢酸やトリクロロ酢酸を共存させて副生するイミダゾールを塩として沈殿させることにより、生成物側に大きく偏らせることができる。対称な酸無水物はトリフルオロアセチル基(またはトリクロロアセチル基)を望むカルボン酸で置換することで得られる。
また、ギ酸と反応させればイミダゾール環のホルミル化が起こる。この生成物はホルミル化試薬として用いられ、加熱によってイミダゾールが再生する。
トリフェニルアルケニルホスホラン(リンイリド)とは以下の様な反応を起こす。
- Ph3P=CHR + R'C(=O)Im → Ph3P+−CHR−C(=O)R' + Im−
- Ph3P+−CHR−C(=O)R + Ph3P=CHR → Ph3P=CR−C(=O)R' + Ph3P+−CH2R
これはウィッティヒ反応で α,β-不飽和ケトンやアルデヒドを合成するのに使うことができる。
ペルオキシドとの反応により過カルボン酸を与え、さらに反応を行えばジアシルペルオキシドが得られる。イミダゾール環は水素化アルミニウムリチウムで還元でき、カルボン酸をアルデヒドに変換できる。グリニャール試薬と反応させればケトンが得られる[1]。
マロン酸エステル類とは以下のような反応を起こす。これはマクロライド系抗生物質の合成に有用である[7]。
- ImC(=O)R + Mg(OC(=O)CHR'C(=O)R'')2 → RC(=O)CHR'C(=O)R
その他の反応[編集]
N-フェニルイミノ誘導体がアザ-ウィッティヒ反応によって得られる[1]。
- Im2C=O + Ph3P=NPh → Im2C=NPh + Ph3P=O
塩基性条件下にカルボニル等価体として働き、ヒドロキシケトンやジケトンからテトロン酸骨格を合成できる[8]。
CDI の存在下、アルコールを3当量以上の活性ハライドと反応させると、対応するハライドに良好な収率で変換される。ブロミドやヨージドの場合に良い結果が得られ、アルコール上の立体化学を変化させない。同様に脱水に用いることもできる[3]。
脚注[編集]
- ^ a b c d e f Staab, H. A.; Wendel, K. "1,1'-Carbonyldiimidazole." Org. Synth. 1968, 48, 44; Org. Synth. Coll. Vol. 1973, 5, 201. オンライン版
- ^ Staab, H. A. "Syntheses using heterocyclic amides (azolides)." Angew. Chem. Int. Ed. Engl. 1962, 1, 351–367. doi:10.1002/anie.196203511
- ^ a b c d Armstrong, A. "N,N'-Carbonyldiimidazole" in Encyclopedia of Reagents for Organic Synthesis; Paquette, L. A. ed.; John Wiley & Sons: New Jersey, 2003.
- ^ Paul, R.; Anderson, G. W. "N,N'-Carbonyldiimidazole, a new peptide forming reagent." J. Am. Chem. Soc. 1960, 82, 4596–4600. doi:10.1021/ja01502a038
- ^ Ford, M. J.; Ley, S. V. "A Simple, one-pot, glycosidation procedure via (1-imidazolylcaronyl) glycosides and zinc bromide." Synlett 1990, 255–256. doi:10.1055/s-1990-21053
- ^ Gais, H.-J. "Synthesis of thiol and selenol esters from carboxylic acids and thiols or selenols, respectively." Angew. Chem. Int. Ed. Engl. 1977, 16, 244–246. doi:10.1002/anie.197702441
- ^ Brooks, D. W.; Lu, L. D.-L.; Masamune, S. "C-Acylation under virtually neutral conditions." Angew. Chem. Int. Ed. Engl. 1979, 18, 72–74. doi:10.1002/anie.197900722
- ^ Jerris, P. J.; Wovkulich, P. M.; Smith, A. B., III. "A facile synthesis of simple tetronic acids and pulvinones." Tetrahedron Lett. 1979, 47, 4517–4520. doi:10.1016/S0040-4039(01)86637-5
