フォンダパリヌクス
 | |
| 臨床データ | |
|---|---|
| 販売名 | Arixtra |
| Drugs.com | monograph |
| ライセンス | EMA:リンク、US FDA:リンク |
| 法的規制 | |
| 薬物動態データ | |
| 生物学的利用能 | N/A |
| 血漿タンパク結合 | 94% |
| 代謝 | renally excreted unchanged |
| 半減期 | 17-21 hours |
| 識別 | |
| CAS番号 |
114870-03-0 |
| ATCコード | B01AX05 (WHO) |
| PubChem | CID: 636380 |
| DrugBank | DB00569en:Template:drugbankcite |
| ChemSpider |
552174 |
| UNII |
J177FOW5JL |
| ChEMBL | CHEMBL1201202en:Template:ebicite |
| 化学的データ | |
| 化学式 | C31H43N3Na10O49S8 |
| 分子量 | 1726.77 g/mol |
| |
フォンダパリヌクス(Fondaparinux)は低分子ヘパリン(LMWH)様の抗凝固薬である。血小板第4因子への親和性がほとんどないのでLMWHよりもヘパリン起因性血小板減少症(HIT)の危険が少ないが、腎排泄型の薬剤であるので腎不全の患者には使えない。ヘパリンと異なり、効果は第Xa因子選択的である[1]。直接第Xa因子阻害薬とは異なり、アンチトロンビンIIIを介して間接的に第Xa因子を阻害する。商品名アリクストラ。
効能・効果
[編集]添付文書に記載されている効能・効果は、1.5mg・2.5mg製剤が「静脈血栓塞栓症の発現リスクの高い、下肢整形外科手術施行患者または腹部手術施行患者における静脈血栓塞栓症の発症抑制」[2]、5mg・7.5mg製剤が「急性肺血栓塞栓症および急性深部静脈血栓症の治療」[3]である。
フォンダパリヌクスはエノキサパリン等と同じく9日以内の虚血性イベントを抑制し、加えてその後の大出血[注 1]ならびに塞栓症罹患率および死亡率を低減させる[4]。当初、ストレプトキナーゼとの併用について研究されていた[5]。
臨床的には、整形外科手術等を受けた患者の深部静脈血栓症の予防または治療、あるいは肺塞栓症の治療に用いられる。
血小板第4因子への親和性がほとんどなく、LMWHでヘパリン起因性血小板減少症(HIT)を起こした患者に使用できた例がある。
用法・用量
[編集]フォンダパリヌクスは1日1回皮下投与で使用する。腎機能の低下により全身クリアランスが低下し、血中濃度が増加する。
静脈血栓塞栓症の発症抑制に用いる場合には1回2.5mgを基本とし、クレアチニンクリアランス20〜30mL/minの患者または出血リスクの高い患者に対しては1回1.5mgを用いる。
急性血栓症の治療に用いる場合には、患者の体重に応じて用量を調節する必要がある。体重50kg未満:5mg、体重50以上・100kg以下:7.5mg、体重100kg超:10mgである。ただし、日本での臨床試験で10mgを投与した例はなく、体重40kg未満の患者に投与した例はほとんどない。
薬物動態
[編集]フォンダパリヌクスを1日1回反復皮下投与すると、3日目には定常状態に達し[6]:18、用量1.5mg・2.5mgの場合の血中半減期(7日目)は約18.1時間であった。CmaxおよびAUC0-24は用量0.75mg〜3.0mgの範囲で線形であったが、それ以上の用量については資料に言及されていない。Cmaxが体重による影響を受けるとされているが明確な資料はない。ただし、体重別に用量を調節(体重50kg未満:5mg、体重50以上・100kg以下:7.5mg、体重100kg超:10mg)した臨床試験では、定常状態での投与後1〜3時間後の血中濃度は平均で 体重50kg未満群:1.00〜1.20mg/L、体重50以上・100kg以下群:1.21〜1.31mg/L、体重100kg超群:1.14〜1.15mg/L と概ね一定であった[6]:19。
腎機能(クレアチニンクリアランス:CCr)別にAUC0-24を比較すると、腎機能正常(90<CCr≦140):7.6mg・hr/L、軽度低下(60<CCr≦90):11.5mg・hr/L、中等度低下(30<CCr≦60):18.3mg・hr/L、重度低下(10≦CCr≦30):43.8mg・hr/L であった[6]:20。
禁忌
[編集]下記の患者には、フォンダパリヌクスは禁忌である。
- 過敏症の既往歴のある患者
- 出血している患者
- 急性細菌性心内膜炎の患者
- 重度の腎障害(クレアチニンクリアランス20mL/min未満)のある患者(血栓症治療に用いる場合は30mL/min未満が禁忌)
副作用
[編集]添付文書に記載されている重大な副作用は、出血、肝機能障害、黄疸、ショック、アナフィラキシーである。血小板の減少・増加が起こることがある。
注射針カバーに天然ゴムラテックスを含むので、アレルギー反応を起こす事がある。
構造および作用機序
[編集]- 「ヘパリンの作用機序」も参照
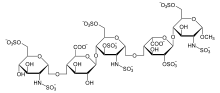
フォンダパリヌクスは合成五糖類であり、第Xa因子を阻害する。分子末端のO-メチル基を除き、加水分解で生成される5つの単糖の配列は、グリコサミノグリカンポリマー(ヘパリンやヘパラン硫酸(HS))を加水分解して得られる単糖の配列と同一である。この5つの糖配列は、抗凝固因子アンチトロンビンIII(AT III)に対する高親和性に必須の配列であると考えられる。ヘパリンやHSがAT IIIに結合すると、AT IIIの抗凝固活性が1,000倍になる。ヘパリンと異なり、フォンダパリヌクスはトロンビン活性を阻害しない。
化学式
[編集]- GlcNS6S = 2-deoxy-6-O-sulfo-2-(sulfoamino)-α-D-glucopyranoside
- GlcA = β-D-glucopyranuronoside
- GlcNS3,6S = 2-deoxy-3,6-di-O-sulfo-2-(sulfoamino)-α-D-glucopyranosyl
- IdoA2S = 2-O-sulfo-α-L-idopyranuronoside
- GlcNS6S-OMe = methyl-O-2-deoxy-6-O-sulfo-2-(sulfoamino)-α-D-glucopyranoside
上記の5つの糖がD-GlcNS6S-α-(1,4)-D-GlcA-β-(1,4)-D-GlcNS3,6S-α-(1,4)-L-IdoA2S-α-(1,4)-D-GlcNS6S-OMeの順に結合している。

注
[編集]- ^ 以下のいずれかに該当する臨床的に異常と考えられる出血
・死亡に至った出血
・頭蓋内、後腹膜、眼球、副腎、心膜、脊椎等の重要部位からの明らかな出血
・ヘモグロビン値が出血発現前の値に比較して、2g/dL(1.6nmol/L)以上減少している臨床的に明らかな出血
・2単位(900mL)以上の全血輸血または相当量以上の赤血球輸血を要した出血
出典
[編集]- ^ “Medscape.com”. 2009年1月23日閲覧。
- ^ “アリクストラ皮下注1.5mg/ アリクストラ皮下注2.5mg 添付文書” (2015年7月). 2016年6月27日閲覧。[リンク切れ]
- ^ “アリクストラ皮下注5mg/ アリクストラ皮下注7.5mg 添付文書” (2015年7月). 2016年6月27日閲覧。[リンク切れ]
- ^ “NEJM -- Comparison of Fondaparinux and Enoxaparin in Acute Coronary Syndromes”. 2009年1月23日閲覧。
- ^ Peters RJ, Joyner C, Bassand JP, et al. (February 2008). “The role of fondaparinux as an adjunct to thrombolytic therapy in acute myocardial infarction: a subgroup analysis of the OASIS-6 trial”. Eur. Heart J. 29 (3): 324–31. doi:10.1093/eurheartj/ehm616. PMID 18245119.
- ^ a b c “アリクストラ皮下注5mg/アリクストラ皮下注7.5mg インタビューフォーム” (PDF) (2013年9月). 2015年2月27日閲覧。
