酒石酸
| 酒石酸 | |
|---|---|
| |
| 一般情報 | |
| IUPAC名 | 2,3-ジヒドロキシブタン二酸 |
| 分子式 | C4H6O6 |
| 分子量 | 150.09 |
| 形状 | 無色固体 |
| CAS登録番号 | [147-71-7](D体) [87-69-4](L体) [133-37-9](ラセミ体) [526-83-0](立体不定) |
| SMILES | C(C(C(=O)O)O)(C(=O)O)O |
| 性質 | |
| 水への溶解度 | 20.6g/100mL(20℃、ラセミ体) |
| 融点 | 168–170 °C(L体、D体) 151℃(メソ体) 206℃(ラセミ体) |
| 比旋光度 [α]D | +12.0(L体、c=20、水中、20℃) |
| 出典 | ICSC(ラセミ体) |
酒石酸(しゅせきさん Tartaric acid)は酸味のある果実、特に葡萄、ワインに多く含まれる有機化合物で、示性式が HOOC−CH(OH)−CH(OH)−COOH と表されるヒドロキシ酸である。IUPAC命名法では 2,3-ジヒドロキシブタン二酸(2,3-dihydroxy butanedioic acid)となる。ワインの樽にたまる沈殿(酒石、tartar)から、カリウム塩(酒石酸水素カリウム)として発見されたためこの名がある。常温常圧で無色の固体。極性溶媒によく溶ける。水への溶解は、L体、D体、メソ体はよく溶けるが、ラセミ体は比較的溶けにくい。分子量は 150.09。英語のTartaric acidからタルタル酸とも呼ばれる。
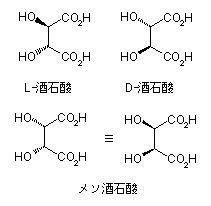
不斉炭素
酒石酸は2つの不斉炭素を持つため、L-(+)-酒石酸(2R,3R)、D-(−)-酒石酸(2S,3S)、メソ酒石酸(2R,3S)の3種類の異性体が存在する。フランスのルイ・パスツールがラセミ体(DL体)の酒石酸塩(酒石酸ナトリウムアンモニウム)を、その結晶の形をもとに光学分割することに成功し、光学異性体の概念を史上初めて示したことで知られる。天然に比較的多く存在するのはL体である。右のメソ酒石酸は天然には存在せず、キラリティを持たない。また、ラセミ体はブドウ酸と呼ばれる。
用途
酒石酸は食品添加物としての使用が認められており、酸味料などとして食品に添加される。医薬においては水溶性を改善するため、酒石酸の塩として供給されているものがある。有機合成化学の分野では光学分割剤として用いられる他、誘導体が不斉触媒などとして使われている(酒石酸ジエチルを用いるシャープレス酸化が有名)。
相撲部屋ではちゃんこに使うポン酢は市販のものを買うのではなく、酒石酸に醤油を混ぜたものを使い、香りづけに柑橘類を絞ったものを入れる。
「疲労を回復する」、「整腸作用がある」などといわれているが、ヒトでの有効性・安全性については科学的に信頼できる十分なデータが無い。
