「インダカテロール」の版間の差分
en:Indacaterol oldid=640540717 を翻訳、加筆。 |
(相違点なし)
|
2015年1月20日 (火) 00:02時点における版
 | |
 | |
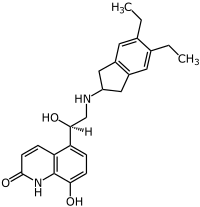
| IUPAC命名法による物質名 | |
|---|---|
| |
| 臨床データ | |
| 販売名 | Onbrez, Arcapta |
| Drugs.com |
国別販売名(英語) International Drug Names |
| ライセンス | EMA:リンク、US FDA:リンク |
| 胎児危険度分類 |
|
| 法的規制 | |
| 投与経路 | Inhalation |
| 識別 | |
| CAS番号 |
312753-06-3 |
| ATCコード | R03AC18 (WHO) |
| PubChem | CID: 6433117 |
| ChemSpider |
5293751 |
| UNII |
8OR09251MQ |
| KEGG | D09318 en:Template:keggcite |
| ChEBI | CHEBI:68575en:Template:ebicite |
| ChEMBL | CHEMBL1095777en:Template:ebicite |
| 化学的データ | |
| 化学式 | C24H28N2O3 |
| 分子量 | 392.490 g/mol |
| |
インダカテロール(Indacaterol、商品名:オンブレス)は超長時間作用性[[交感神経β2受容体作動薬 |アドレナリンβ2受容体作動薬]]の一つである[1]。EMAに2009年11月30日に承認[2]された後、FA[3]と厚生労働省[4]に2011年7月1日に承認された。類薬のホルモテロールやサルメテロールと異なり、1日1回の吸入で用いられる[5]。慢性閉塞性肺疾患(COPD)の治療に用いれる。(気管支喘息についてはデータがない。)ドライパウダー吸入器に充填した形で市販されている。
臨床試験
2010年3月に公表された第III相臨床試験の結果、COPD患者に対するインダカテロールの有効性と安全性が確認された[6]。この試験は米国、ニュージーランド、ベルギーで実施され、416名の重症(平均FEV1=1.5L)COPD患者にインダカテロールと偽薬を割り付けた。インダカテロールは偽薬と比べて統計学的に FEV1及びAUCを改善し、救急薬の使用回数を低減させたが、安全性及び忍容性は偽薬と同程度であった。
2010年に発表された1年間の偽薬対照臨床試験では、1日2回のホルモテロール吸入よりも統計学的に有意にFEV1を改善する事が示された。救急薬の使用回数も減少させたが、有意差は付かなかった。又、インダカテロール群とホルモテロール群で再増悪率には差が付かなかった[7]。
2011年には、インダカテロールとチオトロピウムを12週間に渡り比較した臨床試験の結果が欧州呼吸器雑誌(European Respiratory Journal)に掲載された。その試験では両薬剤でのFEV1改善効果に有意差は見られなかった。インダカテロールは息切れスコア(Transition Dyspnoea Index、TDI)のトータル並びに呼吸器QOLスコア(St. George’s Respiratory Questionnaire、SGRQ)のトータルを大きく改善した[8]。
副作用
添付文書に記載されている重大な副作用は、重篤な血清カリウム値の低下である。他に咳嗽が5%以上に見られる副作用である。その他、5%未満又は頻度不明とされている副作用は、上気道感染、副鼻腔炎、鼻咽頭炎、糖尿病・高血糖、眩暈、錯感覚、頭痛、虚血性心疾患、頻脈、心房細動、動悸、鼻漏、気管支痙攣、口腔咽頭痛、血管浮腫、掻痒症、発疹、蕁麻疹、筋肉痛、筋骨格痛、筋痙縮、胸痛、胸部不快感、口渇、末梢性浮腫である。
参考資料
- ^ Cazzola M, Matera MG, Lötvall J (July 2005). “Ultra long-acting beta 2-agonists in development for asthma and chronic obstructive pulmonary disease”. Expert Opin Investig Drugs 14 (7): 775–83. doi:10.1517/13543784.14.7.775. PMID 16022567.
- ^ European Public Assessment Report for Onbrez Breezhaler
- ^ "FDA approves Arcapta Neohaler to treat chronic obstructive pulmonary disease" (Press release). U.S. Food and Drug Administration. 1 July 2011. 2011年7月2日閲覧。[1]
- ^ “慢性閉塞性肺疾患(COPD)治療薬「オンブレス®吸入用カプセル150 μg」製造販売承認を取得”. ノバルティスファーマ (2011--07-01). 2015年1月20日閲覧。
- ^ Beeh KM, Derom E, Kanniess F, Cameron R, Higgins M, van As A (May 2007). “Indacaterol, a novel inhaled beta2-agonist, provides sustained 24-h bronchodilation in asthma”. Eur. Respir. J. 29 (5): 871–8. doi:10.1183/09031936.00060006. PMID 17251236.
- ^ Feldman, G; Siler, T; Prasad, N; Jack, D; Piggott, S; Owen, R; Higgins, M; Kramer, B et al. (2010). “Efficacy and safety of indacaterol 150 mcg once-daily in COPD: a double-blind, randomised, 12-week study”. BMC pulmonary medicine 10: 11. doi:10.1186/1471-2466-10-11. PMC 2848004. PMID 20211002.
- ^ Dahl R Chung KF Buhl R and others (June 2010). “Efficacy of a new once-daily long-acting inhaled beta2-agonist indacaterol versus twice-daily formoterol in COPD”. Thorax 65 (6): 473–9. doi:10.1136/thx.2009.125435. PMID 20522841.
- ^ R. Buhl L.J. Dunn C. Disdier and others (October 2011). “Blinded 12-week comparison of once-daily indacaterol and tiotropium in COPD”. European Respiratory Journal 38 (4): 797–803. doi:10.1183/09031936.00191810. PMID 21622587.
