ヒドロニウム
| ヒドロニウム | |
|---|---|
|

|
|

|
| 識別情報 | |
| CAS登録番号 | 13968-08-6 |
| 特性 | |
| 化学式 | H3O+ |
| モル質量 | 19.02 g/mol |
| 酸解離定数 pKa | −1.74 |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
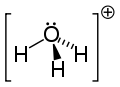
ヒドロニウム (英: hydronium) とは化学式 H3O+ と表されるカチオンおよびその塩である。H3O+ はオキソニウムイオンの一種であり、オニウムイオンの一種でもある。水やアルコールなどプロトン受容性酸素原子を持つ分子からなる溶液中では酸としてはたらく。溶媒和されたプロトンという見方もでき、実際にはさらに水和された H9O4+ として水溶液中に存在していると考えられている。
ヒドロニウム塩の例には過塩素酸一水和物 (HClO4·H2O / H3O+·ClO4−) などがある[1]。
水溶液中におけるヒドロニウムイオン
水溶液中においては、自己解離または溶媒よりも強酸を加えることによって生じる
- 2H2O → H3O+ + OH− または HA + H2O → A− + H3O+
H3O+はリオニウムとしてはたらき、リエイトである水酸化物イオン濃度とは25 °Cにおいて以下の関係が成り立つ[2]。
- Kw = [H3O+][OH−] = 10−14 mol2 L−2
水溶液の酸性度を表すpHは H3O+ の活量により定義される。
- pH = − log (H3O)
希薄水溶液中では近似的に活量は濃度に等しく、計算を簡単にするために通常は下記のように活量の代わりにモル濃度を用いることが多い。
- pH = − log (H3O)
酸塩基平衡に関する化学反応式においては便宜的に H+(水素イオン、プロトン)で表されることが多い。


