細胞内膜系
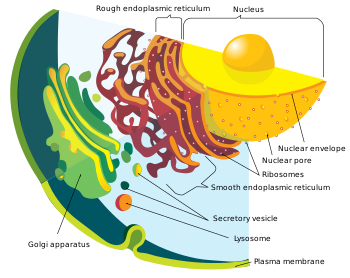
細胞内膜系 (さいぼうないまくけい、英: Endomembrane system)は、細胞に存在する様々な膜から構成される。これらの膜は、細胞内を機能的・構造的区画(細胞小器官)へ分割している。膜に含まれるタンパク質や構成する脂質に違いは見られるものの、全ての膜は脂質二重層でできている。
概要

細胞内膜系は、より正確には、細胞内膜系は単一の機能上・発生上の構成単位を形成し、直接連結されているか小胞輸送によって物質交換を行う膜一式として定義される[1]。
真核生物では、細胞内膜系の細胞小器官には核膜、小胞体、ゴルジ装置、リソソーム、小胞、エンドソーム、そして細胞膜が含まれる。重要なことに、葉緑体やミトコンドリアの膜は細胞内膜系に含まれないものの、細胞内膜系はミトコンドリアの膜から進化したものである可能性があるとされている。
核膜は、核の内容物を取り囲むんでおり[2]、一見、外膜と内膜の2枚の脂質二重層でできているようにも見えるものの、外膜と内膜は連続した脂質二重層で、さらに、小胞体とも連続している。小胞体は合成と輸送のための細胞小器官で、細胞質において分枝している[3]。ゴルジ装置は、ゴルジ体とも呼ばれ、他の構成要素への輸送や細胞からの分泌のために分子が梱包される細胞小器官で、一連の複数の区画から構成される[4]。液胞は細胞の形状と構造の維持、不要物の貯蔵を担い、植物細胞と動物細胞の双方に存在するが、植物細胞の物の方がかなり大きい[5]。小胞は物質の貯蔵や輸送を行う、膜で閉じた比較的小さな袋状構造である[6]。細胞膜は細胞への出入りを調節する防護壁である[7]。
また、菌類には先端小体(Spitzenkörper、スピッツェンケルパー)と呼ばれる細胞小器官が存在し、菌糸の先端の成長と関連している[8]。
原核生物では、内膜系は稀であるが、多くの光合成細菌では細胞膜は高度に折り畳まれており、細胞質の大部分が光捕集を行う膜の層で満たされている[9]。さらに緑色硫黄細菌では、この膜が閉じたクロロソームとよばれる構造が形成されることもある[10]。
細胞内膜系の細胞小器官は、直接的な接触、または膜の一部を小胞として輸送することによって互いに関係している。この関連性の一方で、様々な膜の構造や機能は同一ではない。膜の厚さ、構成分子の組成、代謝挙動は固定されたものではなく、膜の一生を通じて変化する。これらの膜に共通する統一的な特徴の1つは、それらが脂質の二重層であり、タンパク質がどちらかの側に接着したり、二重層を貫通したりしている、ということである[11]。
概念の歴史
酵母では、脂質のほとんどは小胞体、脂肪滴、ミトコンドリアのいずれかで合成され、細胞膜や核膜ではほとんどまたは全く合成されない[12][13]。スフィンゴリン脂質の生合成は小胞体で開始され、ゴルジ装置で完了する[14]。状況は哺乳類でも類似しているが、例外的にアルキルグリセロールの生合成の最初の数段階はペルオキシソームで行われる[15]。そのため、他の細胞小器官を閉じる様々な膜は、これらの合成部位から脂質を輸送して構築される必要がある[16]。脂質輸送が細胞小器官の生合成の中心的過程であることは明らかである一方、脂質輸送のメカニズムは未だあまり解明されていない[17]。
細胞内の膜が構成要素間で物質交換を行う単一の系であるという考えは、1974年に Morré と Mollenhauer によって初めて提唱された[18]。この考えは、様々な脂質膜が細胞内でどのように組み立てられるかを説明する方法として提唱され、これらの膜は脂質合成部位からの「脂質の流れ」によって組み立てられるとされた[19]。膜と小胞の連続的な系による脂質の流れという考えは、脂肪酸やステロールといった遊離した脂質要素は細胞質を通って輸送され、様々な膜はそれぞれ独自に形成される、という考えに代わるものだった。重要なことであるが、細胞質での脂質輸送と連続的な細胞内膜系による脂質の流れとは互いに排他的な過程ではなく、その両方が細胞内で起こっている可能性がある[16]。
構成要素
核膜
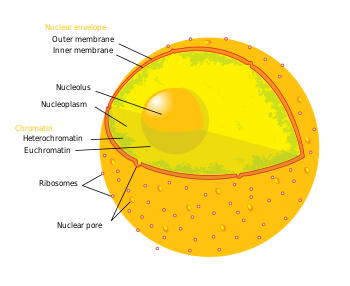
核膜は核を取り囲み、その内容物を細胞質から分離している。核膜は2層の膜 (外膜と内膜) から構成され、どちらもタンパク質が結合した脂質二重層である[20]。核の外膜は粗面小胞体の膜と連続しており、粗面小胞体膜と同じく表面にはリボソームが付着している。また、外膜は内膜とも連続しており、核膜孔と呼ばれる、核膜を貫通する無数の小さな穴の部分で2つの脂質二重層は融合している。核膜孔の直径は約 120 nmで、核と細胞質との間の物質の交通を調節しており、ある物質は膜を通過させるが、他のものは通さない[21]。核と細胞質との間の物質輸送量は多く、そのため核膜孔は細胞の生理に重要な役割を果たしている。外膜と内膜の間の空間は核膜腔 (perinuclear space) と呼ばれ、粗面小胞体の内腔とつながっている。
核膜の構造は中間径フィラメントのネットワークによって決定される。このネットワークは核の内側の面に沿って核ラミナと呼ばれる網目状の裏打ち構造を組織し、クロマチン、核膜の膜貫通タンパク質や他の核の構成要素と結合している。核ラミナは、核内の物質の核膜孔への移動や、有糸分裂中の核膜の解体とその後の再構築を助けていると考えられている[2]。
核膜は相当量の輸送を担っているため、核膜孔での物質の出入りの調節は極めて効率的に行われている。RNAとリボソームのサブユニットは絶えず核から細胞質へ輸送されなければならない。ヒストン、遺伝子調節タンパク質、DNAポリメラーゼとRNAポリメラーゼ、そして核の活動に必須な他の物質は細胞質から核へ輸送されなければならない。典型的な哺乳類細胞の核膜には、3000個から4000個の核膜孔複合体が存在する。細胞がDNAを合成している時、核膜孔複合体1個当たり毎分約100個のヒストン分子を細胞質から核へ輸送する必要がある。細胞が迅速に成長している時には、新しく組み立てられたリボソームの大サブユニットと小サブユニットを毎分約6個、核からタンパク質合成が行われる細胞質へ輸送する必要がある[22]。
小胞体

小胞体は、膜に囲まれた合成と輸送のための細胞小器官である。核膜と連続性があり、核膜が拡張されたものと見なすこともできる。小胞体膜は核膜と連結されているため、核と細胞質の間の物質受け渡しの場ともなっている[23]。
真核細胞においては、膜の総量の半分以上が小胞体のものである。小胞体は扁平な嚢と分枝した小管から構成されている。これらは相互に連結されており、小胞体の膜は単一の内部空間を閉じる連続的なシートとなっていると考えられている。この高度に畳み込まれた空間は小胞体内腔 (ER lumen または ER cisternal space) と呼ばれる。細胞の種類にもよるものの、小胞体内腔は細胞の総体積の約10%を占めるとされる。小胞体膜は物質の小胞体内腔と細胞質との間の選択的透過を行っている。
小胞体は、細胞の内外で利用される化合物の産生、加工、輸送に中心的な役割を果たす。小胞体膜は全ての膜貫通タンパク質の合成部位であり、小胞体自身、ゴルジ装置、リソソーム、エンドソーム、ミトコンドリア、ペルオキシソーム、分泌小胞、そして細胞膜を含む細胞小器官の脂質のほとんどを合成している。さらに、細胞外へ出るタンパク質のほとんど全てと、小胞体内腔、ゴルジ装置、リソソームへ送られるタンパク質は、最初に小胞体内腔へ輸送される。したがって、小胞体内腔に見つかるタンパク質の多くは、他の部位へ輸送される途上で一時的に存在しているだけである。しかし、一部のタンパク質は常に内腔に留まり、それらは小胞体タンパク質 (ER resident protein) として知られる。これらの特別なタンパク質は、特定のアミノ酸配列で構成される小胞体保留シグナル (ER retention signal) によって小胞体に保持される。小胞体タンパク質の重要な例はBiPとして知られるシャペロンタンパク質で、不適切な組み立てや加工を受けたタンパク質を特定し、それらが最終目的地へ送られるのを防いでいる[24]。
小胞体は翻訳と共役したタンパク質の選別に関与している。小胞体シグナル配列を含むポリペプチドはシグナル認識粒子 (signal recognition particle、SRP) によって認識され、タンパク質の合成が停止される。SRPはポリペプチドを小胞体膜へ輸送し、ポリペプチドは膜孔内へ放出されて翻訳が再開される[25]。
小胞体には滑面小胞体 (smooth ER) と粗面小胞体 (rough ER) という2つの領域が存在する。これらは構造と機能は異なるが、連結されている。粗面小胞体の細胞質側の表面はリボソームで覆われており、電子顕微鏡で観察すると細胞質側表面に凹凸があるように見えるため、その名が付けられた。これに対して、滑面小胞体の細胞質側表面にはリボソームが存在せず、滑らかな見た目をしている[26]。
滑面小胞体の機能
大多数の細胞では滑面小胞体領域は少なく、しばしば一部が滑面で一部が粗面という構造となっている。このような領域は移行型小胞体 (transitional ER) と呼ばれることもある。それはこの領域が、輸送小胞が新しく合成されたタンパク質や脂質をゴルジ装置へ輸送するために出芽する、小胞体の出口部分に相当するためである。
一方、特定の特殊化された細胞では滑面小胞体は豊富に存在し、別の機能を持っている。これらの細胞の滑面小胞体は、脂質合成、炭水化物の代謝、薬物や毒物の解毒など、代謝過程において多様な機能を果たす[23][26]。
滑面小胞体は、油脂、リン脂質、ステロイドといった脂質の合成に必須である。脊椎動物の性ホルモンや副腎から分泌されるステロイドホルモンは、動物細胞の滑面小胞体で産生されるステロイドの例である。これらのホルモンを合成する細胞は滑面小胞体に富んでいる[23][26]。
肝細胞も滑面小胞体を豊富に持つ特殊化された細胞であり、炭水化物の代謝における滑面小胞体の役割の例である。肝細胞は炭水化物をグリコーゲンの形態で保存する。グリコーゲンの分解は最終的に肝細胞からのグルコースの放出につながり、血糖濃度の調節に重要である。しかし、グリコーゲン分解の主要産物はグルコース-1-リン酸である。グルコース-1-リン酸はグルコース-6-リン酸に変換され、その後肝細胞の滑面小胞体の酵素によってリン酸が除去されてグルコースとなり、細胞から出ていけるようになる[23][26]。
また、滑面小胞体の酵素は、薬物や毒物の解毒、ステロイドホルモンのような脂溶性の高いホルモンの代謝を助けている。多くの場合、解毒は脂溶性の高い化合物にヒドロキシル基を付加し、化学物質の水溶性を上げて体外への排泄を容易にするという代謝過程である。よく研究されている解毒反応の例はシトクロムP450ファミリーの酵素によって行われるもので、脂溶性の化学物質や代謝産物に対して、酸化反応の触媒を行うことで、水溶性を高め、それらが細胞膜などに毒性レベルにまで蓄積されるのを防いでいる[23][26]。
筋細胞の滑面小胞体 (筋小胞体) は、異なる特殊な機能を持つ。小胞体膜は細胞質から内腔へカルシウムイオンを汲み上げて蓄える。筋細胞が神経インパルスによって刺激されると、カルシウムは小胞体膜を越えて細胞質へ移動し、筋細胞の収縮を引き起こす[23][26]。
粗面小胞体の機能
多くの細胞種では、粗面小胞体に結合したリボソームで合成されたタンパク質は外部へ輸送される。リボソームがアミノ酸をタンパク質の単位へ組み立て、タンパク質は粗面小胞体へ送られてさらなる調整がなされる。これらのタンパク質は小胞体膜へ埋め込まれる膜タンパク質か、膜を通過して内腔へ入ることのできる水溶性タンパク質のどちらかである。小胞体の内側に到達したタンパク質は、そこで正しい立体構造へ折りたたまれる。小胞体は炭水化物や糖などの化学物質を付加し、完成したタンパク質 (分泌タンパク質と呼ばれる) はそれらが必要とされる細胞領域へ輸送されるか、さらなる加工と修飾のためにゴルジ装置へ送られる[23][26]。
分泌タンパク質が形成されると、小胞体膜はそれらと小胞体に残るタンパク質を分離する。分泌タンパク質は、移行型小胞体から泡のように出芽する小胞の膜に包まれ、小胞体から離れる。細胞の異なる部分へ移動するこれらの小胞は、輸送小胞と呼ばれる[23][26]。脂質やタンパク質が小胞体から輸送される他のメカニズムとしては、膜接触部位 (membrane contact site) と呼ばれる、小胞体が細胞膜やゴルジ装置、リソソームなどの他の細胞小器官の膜と近接して安定に結合している領域において、脂質輸送タンパク質によって行われるものがある[27]。
分泌タンパク質を作ることに加えて、粗面小胞体はタンパク質とリン脂質の付加していくことで、成長する膜をその場で作り上げる。リボソームから伸長してきた、膜タンパク質となるべきポリペプチドは小胞体の膜へ挿入され、その疎水的な部分によってその場に保たれる。また、粗面小胞体は自身の膜のリン脂質の合成を行い、小胞体膜に組み込まれた酵素によってリン脂質が組み立てられる。これによって小胞体膜は拡大し、輸送小胞によって細胞内膜系の他の構成要素へ転移する[23][26]。
ゴルジ装置
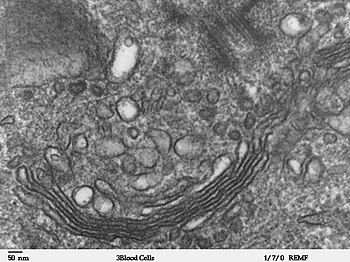
ゴルジ装置は cistaenae (ゴルジ体、ゴルジ嚢、ゴルジ槽などとも訳される) と呼ばれる個別の袋状構造から構成される。その形は積み重なったパンケーキに似ている。これらの積み重ねの数は細胞の機能によって変化する。ゴルジ装置はさらなるタンパク質修飾のために用いられる。小胞体から小胞を受け取る面はシス面として知られ、通常小胞体のそばに位置する。反対側の面はトランス面と呼ばれ、修飾された化合物が出ていく場所である。トランス面は通常細胞膜と向かい合っており、ゴルジ装置で修飾された物質のほとんどは細胞膜へ送られる[28]。
小胞体から送られてきたタンパク質を含む小胞は、ゴルジ装置で修飾された後、細胞からの分泌や細胞の他の部分への輸送のための準備がなされる。酵素で覆われたゴルジ装置内の空間を通過する過程で、タンパク質には様々なことが起こる。糖タンパク質の炭水化物部分の修飾と合成は、タンパク質の加工に共通の過程である。ゴルジ装置は単糖を除去して置換し、さまざまな種類のオリゴ糖を作り出す。タンパク質の修飾に加え、ゴルジ装置自身も高分子の製造を行う。植物細胞では、ゴルジ装置は植物の構造に必要なペクチンや他の多糖を産生する[29]。
修飾過程が完了すると、ゴルジ装置はそれらを選別し、細胞の様々な部分へ送り出す。分子を同定するためのラベルやタグがゴルジ装置の酵素によって付加されており、選別過程を助けている。全ての準備が整うと、ゴルジ装置はトランス面からの小胞の出芽によって輸送を行う[30]。
液胞
液胞は、細胞内に存在する膜結合性の袋構造で、小胞よりも大きく、その機能は多岐にわたる。液胞の働きは、植物と動物では異なる。
植物細胞では、液胞は細胞の総体積の30%から90%を占める[31]。成熟した植物細胞のほとんどには、1つの巨大な中央液胞 (central vacuole) が存在し、液胞膜 (tonoplast) と呼ばれる膜に包まれている。植物細胞の液胞は、細胞の栄養素や廃棄物を貯蔵する区画として機能する。これらの分子が貯蔵されている液体は細胞液 (cell sap) と呼ばれる。細胞を彩る色素が細胞液に存在していることもある。液胞は細胞のサイズを増大させることもでき、水が加えられると伸長する。液胞は膨圧 (細胞壁が陥没しないようにしている浸透圧) を調節する。動物細胞におけるリソソームのように、液胞のpHは酸性で加水分解酵素を含んでいる。液胞のpHは、細胞の恒常性の維持に寄与している。例えば、細胞環境のpHが低下すると、細胞質へ流入する水素イオン (H+) は液胞へ移され、細胞質のpHは一定に保たれる[32]。
動物細胞では、液胞はエキソサイトーシスやエンドサイトーシスの過程に関与する。エンドサイトーシスは物質が細胞内へ取り込まれる過程であり、エキソサイトーシスは物質が細胞から細胞外空間へ除去される過程である。エンドサイトーシスにおいて、取り込まれる物質はまず細胞膜に囲まれ、その後液胞へ移される。エンドサイトーシスには、食作用 (ファゴサイトーシス) と 飲作用 (ピノサイトーシス) という2つのタイプがある。食作用では、細胞は細菌のような巨大な粒子を飲み込む。飲作用も同様の過程で、液状の物質などが取り込まれる[33]。
小胞
小胞は、異なる構成要素の間の分子輸送を行う、膜で閉じた小さな輸送単位である。ほとんどの小胞は、小胞体で組み立てられた膜をゴルジ装置へ輸送し、その後ゴルジ装置から様々な場所へ輸送を行う[34]。
小胞には、タンパク質構成が異なる様々なタイプが存在する。そのほとんどは膜の特定の領域で形成される。小胞が膜から出芽する時、その細胞質側表面には特定のタンパク質が含まれている。小胞が向かう膜にはそれぞれ細胞質側表面にマーカーが存在しており、膜へ向かう小胞表面のタンパク質と対応する。小胞が対応する膜を見つけると、小胞は膜と融合する[35]。
小胞には、クラスリン被覆小胞、COPI被覆小胞、COPII被覆小胞という良く知られた3つのタイプが存在し、それぞれが細胞内で異なる機能を持っている。例えば、クラスリン被覆小胞はゴルジ装置と細胞膜の間の物質輸送を行う。COPIとCOPIIは、小胞体とゴルジ装置の間の輸送に頻繁に用いられる[35]。
リソソーム
リソソームは、細胞内消化に用いられる、加水分解酵素を含む細胞小器官である。リソソームの主要な機能は、細胞内に取り込まれた分子を加工することと、細胞の老化部分をリサイクルすることである。リソソーム内の酵素は酸性加水分解酵素であり、その至適pHは一般的な細胞の細胞質のpHである中性付近ではなく、加水分解反応を効率良く触媒するためには酸性環境を必要とする。リソソーム内部のpHは5.0に保たれており、最適な環境が提供されている[36]。仮にリソソームが破裂したとしても、細胞質のpHは中性であるため、放出された酵素は高い活性を持たないため、無秩序に細胞質を構成する物質が加水分解されるようなことは起こりにくい。ただ、それでも多数のリソソームからの酵素の漏出があれば、細胞は自己消化によって破壊され得る。
リソソームは食作用と呼ばれる細胞内消化過程に関与する。リソソームは液胞と融合し、酵素を液胞内へ放出する。酵素によって分解されて生じた、糖やアミノ酸、他の単量体は、細胞質へ拡散し細胞の栄養素となる。また、リソソームは加水分解酵素を利用して、老化した細胞小器官を分解することで、分解産物を細胞小器官の材料などとしてリサイクルする。この過程はオートファジーと呼ばれる。リソソームは他の細胞小器官を飲み込み、その酵素を使って取り込んだ物質の分解を行う。リソソームの最後の機能は、細胞自体を分解する自己分解 (autolysis) である[37]。
先端小体 (スピッツェンケルパー)
先端小体 (Spitzenkörper、スピッツェンケルパー) は菌類のみに見つかる細胞内膜系の構成要素であり、菌糸の先端の成長と関連している。細胞壁の構成要素を含む小胞が凝集した暗色の構造体で、ゴルジ装置と細胞膜の中間点として機能し、細胞壁の構成要素の集合と放出が行われる。先端小体は運動性で、前進するにつれて新たな先端が作り出される[8]。
細胞膜

細胞膜はリン脂質の二重層からなる膜で、細胞を環境から分離し、細胞内外への分子やシグナルの輸送の調節を行っている。細胞膜の機能を果たしているのは、主に膜に埋め込まれたタンパク質である。細胞膜は固定されているわけでも強固な構造を持っているわけでもなく、膜を構成する分子は横方向に自由に動くことができる。この動的性質と複数の要素から構成されることとが、細胞膜が「流動モザイク」と呼ばれる理由である。二酸化炭素や水、酸素といった小さな分子は、拡散または浸透によって細胞膜を自由に通過することができる。より大きな分子は、タンパク質の補助のもと、促進拡散や能動輸送によって膜を通過する[38]。
細胞膜は複数の機能を持っている。細胞膜は、細胞内へ栄養素を輸送し、不要物を排出し、物質の細胞内への進入を防ぎ、必要な物質が細胞から出ていくのを防ぎ、細胞質のpHと浸透圧を維持する。これらの機能のために用いられる輸送タンパク質は、いくつかの物質を通過させるのに対して、他の物質は通さない。これらのタンパク質は、濃度勾配に逆らって物質をくみ上げる場合には、ATPの加水分解のエネルギーを利用する[38]。
これらの普遍的機能に加えて、多細胞生物の細胞膜はより特殊な機能も持つ。細胞膜上の糖タンパク質は、代謝産物の交換や組織形成のために他の細胞を認識するのを助ける。他の細胞膜のタンパク質は、細胞骨格と細胞外マトリックスを連結し、細胞の形状の維持や膜タンパク質の位置の固定を行っている。酵素の中には、細胞膜上に存在しているものもある。膜の受容体タンパク質は、その受容体がメッセンジャーとして利用している物質にマッチする形状をしており、メッセンジャーが結合することによって細胞に様々な応答を引き起こす[39]。
進化
細胞内膜系の起源は真核生物自体の起源と関連しており、真核生物の起源はミトコンドリアの細胞内共生の起源と関連している。細胞内膜系の起源を説明するモデルは多数提唱されている[40]。2016年に提唱された、あるモデルでは「細胞内膜系は共生したミトコンドリアが分泌した外膜の小胞から進化した」とされている[41]。このミトコンドリア外膜小胞由来モデルは、今のところ、真核生物の起源の時点で新規に作り出すものが最も少なく済むモデルで、ミトコンドリアが細胞の他の構成要素と多くの連結を持つことも無理なく説明できる[42]。
出典
- ^ Smith, A. L. (1997). Oxford dictionary of biochemistry and molecular biology. Oxford [Oxfordshire]: Oxford University Press. pp. 206. ISBN 0-19-854768-4
- ^ a b Davidson, Michael (2005年). “The Nuclear Envelope”. Molecular Expressions. Florida State University. 2008年12月9日閲覧。
- ^ Davidson, Michael (2005年). “The Endoplasmic Reticulum”. Molecular Expressions. Florida State University. 2008年12月9日閲覧。
- ^ Graham, Todd R. (2000). Eurekah Bioscience Collection Cell Biology. University of New South Wales and Landes Bioscience. ISBN 0-7334-2108-3
- ^ Lodish, Harvey (2000年). “Section 5.4 Organelles of the Eukaryotic Cell”. Molecular Cell Biology. W. H. Freeman and Company. 2008年12月9日閲覧。
- ^ Cooper, Geoffrey (2000年). “The Mechanism of Vesicular Transport”. The Cell: A Molecular Approach. Sinauer Associates, Inc. 2008年12月9日閲覧。
- ^ Davidson, Michael (2005年). “Plasma Membrane”. Molecular Expressions. Florida State University. 2008年12月9日閲覧。
- ^ a b Steinberg, G. (2007). “Hyphal Growth: a Tale of Motors, Lipids, and the Spitzenkörper”. Eukaryotic Cell 6 (3): 351–360. doi:10.1128/EC.00381-06. PMC 1828937. PMID 17259546.
- ^ “Prokaryotic photosynthesis and phototrophy illuminated”. Trends Microbiol. 14 (11): 488–96. (2006). doi:10.1016/j.tim.2006.09.001. PMID 16997562.
- ^ “Lamellar Organization of Pigments in Chlorosomes, the Light Harvesting Complexes of Green Photosynthetic Bacteria”. Biophys. J. 87 (2): 1165–72. (August 2004). doi:10.1529/biophysj.104.040956. PMC 1304455. PMID 15298919.
- ^ Campbell, Neil A.; Reece, Jane B. (2002). Biology (6th ed.). Benjamin Cummings. ISBN 0-8053-6624-5
- ^ “Phospholipid synthesis and lipid composition of subcellular membranes in the unicellular eukaryote Saccharomyces cerevisiae”. J. Bacteriol. 173 (6): 2026–34. (March 1991). PMC 207737. PMID 2002005.
- ^ “Synthesis, storage and degradation of neutral lipids in yeast”. Biochim. Biophys. Acta 1771 (3): 299–309. (March 2007). doi:10.1016/j.bbalip.2006.07.001. PMID 16916618.
- ^ Futerman AH (December 2006). “Intracellular trafficking of sphingolipids: relationship to biosynthesis”. Biochim. Biophys. Acta 1758 (12): 1885–92. doi:10.1016/j.bbamem.2006.08.004. PMID 16996025.
- ^ “Biochemistry of mammalian peroxisomes revisited”. Annu. Rev. Biochem. 75: 295–332. (2006). doi:10.1146/annurev.biochem.74.082803.133329. PMID 16756494.
- ^ a b Voelker DR (1 December 1991). “Organelle biogenesis and intracellular lipid transport in eukaryotes”. Microbiol. Rev. 55 (4): 543–60. PMC 372837. PMID 1779926.
- ^ Voelker DR (July 2005). “Bridging gaps in phospholipid transport”. Trends Biochem. Sci. 30 (7): 396–404. doi:10.1016/j.tibs.2005.05.008. PMID 15951180.
- ^ Morré DJ, Mollenhauer HH. (1974). The endomembrane concept: a functional integration of endoplasmic reticulum and Golgi apparatus. In Dynamic Aspects of Plant infrastructure (ed. A. W. Robards), pp. 84–137. London, New York, etc.: McGraw-Hill.
- ^ Morre, D.J. (1975). “Membrane Biogenesis”. Annual Review of Plant Physiology 26 (1): 441–481. doi:10.1146/annurev.pp.26.060175.002301.
- ^ Childs, Gwen V. (2003年). “Nuclear Envelope”. UTMB. 2006年6月20日時点のオリジナルよりアーカイブ。2008年9月28日閲覧。
- ^ Cooper, Geoffrey (2000年). “The Nuclear Envelope and Traffic between the Nucleus and Cytoplasm”. The Cell: A Molecular Approach. Sinauer Associates, Inc. 2008年12月9日閲覧。
- ^ Alberts, Walter (2002年). “Nuclear Pore Complexes Perforate the Nuclear Envelope”. Molecular Biology of the Cell 4th edition. Garland Science. 2008年12月9日閲覧。
- ^ a b c d e f g h i Cooper, Geoffrey (2000年). “The Endoplasmic Reticulum”. The Cell: A Molecular Approach. Sinauer Associates, Inc. 2008年12月9日閲覧。
- ^ Bertolotti, Anne; Zhang, Yuhong; Hendershot, Linda M.; Harding, Heather P.; Ron, David (2000). “Dynamic interaction of BiP and ER stress transducers in the unfolded-protein response”. Nature Cell Biology 2 (6): 326–333. doi:10.1038/35014014. PMID 10854322 2008年10月3日閲覧。.
- ^ Biology. McGraw Hill education. pp. 89
- ^ a b c d e f g h i Alberts, Walter (2002年). “Membrane-bound Ribosomes Define the Rough ER”. Molecular Biology of the Cell 4th edition. Garland Science. 2008年12月9日閲覧。
- ^ “Inter-organelle membrane contact sites: through a glass, darkly”. Curr. Opin. Cell Biol. 18 (4): 371–8. (August 2006). doi:10.1016/j.ceb.2006.06.011. PMID 16806880.
- ^ Rothman, J. (1981). “The golgi apparatus: two organelles in tandem”. Science 213 (4513): 1212–1219. doi:10.1126/science.7268428. PMID 7268428 2008年10月4日閲覧。.
- ^ Alberts, Walter (2002年). “Transport from the ER through the Golgi Apparatus”. Molecular Biology of the Cell 4th edition. Garland Science. 2008年12月9日閲覧。
- ^ Cooper, Geoffrey (2000年). “The Golgi Apparatus”. The Cell: A Molecular Approach. Sinauer Associates, Inc. 2008年12月9日閲覧。
- ^ Alberts, Walter (2002年). “Plant and Fungal Vacuoles Are Remarkably Versatile Lysosomes”. Molecular Biology of the Cell 4th edition. Garland Science. 2008年12月9日閲覧。
- ^ Lodish, Harvey (2000年). “Plant Vacuoles Store Small Molecules and Enable the Cell to Elongate Rapidly”. Molecular Cell Biology. W. H. Freeman and Company. 2008年12月9日閲覧。
- ^ Cooper, Geoffrey (2000年). “Endocytosis”. The Cell: A Molecular Approach. Sinauer Associates, Inc. 2008年12月9日閲覧。
- ^ Lodish, Harvey (2000年). “Section 17.10 Molecular Mechanisms of Vesicular Traffic”. Molecular Cell Biology. W. H. Freeman and Company. 2008年12月9日閲覧。
- ^ a b Alberts, Walter (2002年). “The Molecular Mechanisms of Membrane Transport and the Maintenance of Compartmental Diversity”. Molecular Biology of the Cell 4th edition. Garland Science. 2008年12月9日閲覧。
- ^ Alberts, Walter (2002年). “Transport from the Trans Golgi Network to Lysosomes”. Molecular Biology of the Cell 4th edition. Garland Science. 2008年12月9日閲覧。
- ^ Cooper, Geoffrey (2000年). “Lysosomes”. The Cell: A Molecular Approach. Sinauer Associates, Inc. 2008年12月9日閲覧。
- ^ a b Cooper, Geoffrey (2000年). “Structure of the Plasma Membrane”. The Cell: A Molecular Approach. Sinauer Associates, Inc. 2008年12月9日閲覧。
- ^ Lodish, Harvey (2000年). “Section 5.3. Biomembranes: Structural Organization and Basic Functions”. Molecular Cell Biology. W. H. Freeman and Company. 2008年12月9日閲覧。
- ^ Martin WF (6 May 2014). “Endosymbiotic theories for eukaryote origin”. Philos. Trans. R. Soc. B 370: 20140330-18. doi:10.1098/rstb.2014.0330. PMC 4571569. PMID 26323761.
- ^ Gould SB (31 March 2016). “Bacterial Vesicle Secretion and the Evolutionary Origin of the Eukaryotic Endomembrane System”. Trends Microbiol. 24: 525–34. doi:10.1016/j.tim.2016.03.005. PMID 27040918.
- ^ Murley, A.; Nunnari, J. (3 March 2016). “The emerging network of mitochondria-organelle contacts”. Mol. Cell 61: 648–653. doi:10.1016/j.molcel.2016.01.031. PMID 26942669.
