酸感受性イオンチャネル
| Acid-sensing sodium channel | |||||||||
|---|---|---|---|---|---|---|---|---|---|
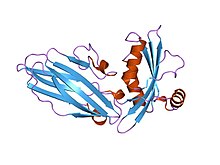 ASIC1の構造[1] | |||||||||
| 識別子 | |||||||||
| 略号 | ASC | ||||||||
| Pfam | PF00858 | ||||||||
| InterPro | IPR001873 | ||||||||
| PROSITE | PDOC00926 | ||||||||
| SCOP | 2qts | ||||||||
| SUPERFAMILY | 2qts | ||||||||
| TCDB | 1.A.6 | ||||||||
| OPM superfamily | 181 | ||||||||
| OPM protein | 4fz1 | ||||||||
| |||||||||
酸感受性イオンチャネル(さんかんじゅせいイオンチャネル、英: acid-sensing ion channel、略称: ASIC)は、神経に存在する電位非依存性ナトリウムチャネルである。ASICは細胞外のプロトンによって活性化され、Na+を透過させる。ASIC1は低いCa2+透過性も示す[2]。ASICタンパク質は、イオンチャネルのENaC/Degスーパーファミリーのサブファミリーを構成する。ASICは哺乳類では5つの遺伝子によってコードされており、ASIC1、ASIC2、ASIC3、ASIC4、ASIC5のサブユニットが産生される[3]。さらに、選択的スプライシングによるアイソフォームが存在し、末尾のアルファベットで区別される。ASICはこれらのタンパク質サブユニットのうちの3つから組み立てられてられ、中枢神経系と末梢神経系の双方でホモ三量体またはヘテロ三量体として存在する[2]。最も一般的なASICはASIC1a、ASIC1a/2a、ASIC3である。ASIC2bは自身では機能を持たないが、ヘテロ三量体に加わることでチャネル活性を調節する。ASIC4の機能は不明である。ASICは網膜の損傷、けいれん発作、虚血性脳損傷などの病態に関与しており、創薬の標的としても期待されている[4][5]。
構造[編集]
ASICの各サブユニットは500–560アミノ酸の配列からなり、2つの膜貫通セグメント(TMD1、TMD2)、細胞質側に位置するN末端とC末端、そして巨大な細胞外ドメインから構成される[3]。細胞内のN末端・C末端ドメインはチャネルの細胞内でのタンパク質間相互作用とその調節、イオンの透過性、ゲート機能に不可欠である。各ASICのゲート機能と作動機構は、構造を形成するサブユニットの組み合わせによって決定される[3]。
ポア[編集]
イオンチャネルのポアの作動機構は、イオンチャネルの機能の基礎をなしている。細胞外ドメインの上部から細胞内領域まで、ポアはチャネルの中央部、ASICの3つのサブユニットの間を通過しており、チャネルの状態によって大きさや形が変化する狭窄部が存在する[3]。
各サブユニットの2つの膜貫通ドメイン(TMD1とTMD2)がチャネルのポアの形成を担っている。TMD2が主にポアの内壁とチャネルの不活性化ゲートの形成に関与している一方、TMD1はタンパク質を細胞の脂質二重層内に保持する役割を担っている[6]。TMD1は細胞外ドメインのβシートに連結されており、このβシートはイオンがチャネルを通過できるよう、細胞外ドメインを屈曲させて広げる[3]。TMD2セグメントにはポアの最も狭い部分を形成する選択性フィルターが位置し、ASICの主にNa+に対する透過性を担う。ASIC1では、各サブユニットの3つのアミノ酸残基(Gly443、Ala444、Ser445)からなる計9つのアミノ酸残基が選択性フィルターを形成している。この選択性フィルターは「GASベルト」とも呼ばれ、各アミノ酸のカルボニル酸素は全てポアに並び、負電位を形成してカチオンの透過に寄与している[3]。ASIC1では、TMD2の内壁の細胞外側部分に位置する特定のアスパラギン酸残基がこのチャネルの低いCa2+透過性と関連づけられている。さらに、膜貫通領域の末端部分の残基の変異によってチャネルの機能やNa+の透過性が変化するため、この領域もNa+に対する選択性に寄与していると考えられる[3]。
細胞外領域[編集]
ASICの大きな、拳に似た形状をした細胞外領域は、タンパク質の構造の大部分を占めている。この拳に似た構造には、wrist(手首)、palm(掌)、finger(指)、knuckle(指関節)、thumb(親指)、β-ballと名付けられたドメインが存在する。細胞外ドメインの大部分を構成するpalmは7本のβシートから形成されるが、他の二次構造は主にαヘリックスから構成される[3]。細胞外領域はその特異なアミノ酸配列によって特徴づけられ、pHによるゲート機能とともに活性化・不活性化の誘導に不可欠である。細胞外ドメインから膜貫通領域へのシグナル伝達にはpalmとthumbの間のβシートループ領域が関与しており、開状態へのコンフォメーション変化を引き起こす[3]。しかしながら、どの残基がプロトンと相互作用してチャネルを活性化させるのかについてはいまだに結論が出ていない。2009年には、Tyr72、Pro287、Trp288の芳香性残基とASICのプロトンゲート機能との関係が確立された[3]。これらの残基は酸性のポケットを形成し、チャネルの活性化や調節のpH依存性を担う静電ポテンシャルを形成する[7]。この細胞外ドメインのポケットはカチオンを濃縮する貯蔵庫として機能し、Na+の流入をさらに補助する。また、細胞外領域のグリコシル化も顕著であり、膜表面へのチャネルの輸送やpH感受性の確立にも重要な役割を果たしている。さらに、ASICのゲートのプロトン親和性の調節には、ポアの内部と細胞外ドメインの双方においてCa2+が重要な役割を果たしている可能性が実験的に示されている[3]。
機能[編集]
ASICの役割は細胞外のpHの低下を検知し、神経細胞の反応やシグナルを引き起こすことである。活性化部位に結合するリガンドはプロトンのみであると長らく考えられてきたが、近年の研究ではASIC4とASIC1は正常なpHでも活性化されうることが示され、他のタイプのリガンドの存在が示唆されている[8]。酸性度が高くなるとプロトンがチャネルの細胞外領域に結合し、コンフォメーション変化、すなわちTMD2の開口によってイオンチャネルを活性化する。その結果、TMD2の内側を通ってナトリウムイオンが流入する。すべてのASICがナトリウムイオンを特異的に透過させ、ASIC1aのみはさらにカルシウムイオンに対しても低い透過性を有する。これらのカチオンの流入は膜の脱分極を引き起こし、電位依存性カルシウムチャネルが活性化されてカルシウムイオンが細胞内に流入する。その結果、神経細胞の脱分極が引き起こされ、興奮反応が引き起こされる。ASIC1aの場合、細胞内のCa2+の増加は直接チャネルを介して流入したものでもある[8]。
いったんASICが活性化されると、多数の異なるエフェクタータンパク質やシグナル伝達分子によってさまざまな反応が引き起こされる。α-アクチニンはpH感受性を高めてチャネルの脱感作状態からの回復を引き起こすとともに、チャネル電流の増大ももたらす[8]。リン酸化によってASICの機能を調節するプロテインキナーゼも多く存在し、プロテインキナーゼA(PKA)やプロテインキナーゼC(PKC)などが含まれる。さらに多数の調節因子が存在すると考えられているが、それらの影響に関しては実験的結論はまだ得られていない[8]。
他の因子もASICの調節に関与する。ASIC1aとASIC2aにはN-グリコシル化部位がより多く存在し、チャネル表面の成熟型N-結合型糖鎖の存在によって膜へのASIC1aの選択的輸送が行われると考えられている[8]。また、ASIC2の表面にはグリセロール(タンパク質の成熟を促進することが知られている)が多く含まれおり、これらのチャネルの機能の調節はタンパク質の成熟に依存していると考えられる。また、酸化が膜への輸送に関与しているという仮説も立てられている[8]。
位置[編集]
大部分のASICは神経系に発現している。ASIC1、ASIC2、ASIC2b、ASIC4は中枢神経系と末梢神経系の双方で広く発現しているが、ASIC1bとASIC3は末梢神経系のみに位置しているのが一般的である。
末梢神経系では、ASICはシナプス後膜と細胞体の膜に位置している。さらに、ASICは皮膚、筋肉、関節、内臓の求心性神経線維に位置し、そこで痛覚、味覚、胃腸機能と関係していることが明らかにされている[9]。
中枢神経系では、ASICは脊髄の後角に存在する[4]。ASIC1は扁桃体に特に多く存在し、不安行動に関与していることが示されている。ASIC3はコルチ器と蝸牛神経節に存在し、聴覚と視覚に関与しているチャネルであることが示されている[6]。ASIC1a、ASIC2a、ASIC2bサブユニットは海馬にも存在する[10]。
生理学[編集]
ASICは、中枢神経系や末梢神経系と関係した広範囲の疾患の治療の薬物標的としての可能性がある[4][5]。痛覚の分野で特に注目されているのは、侵害受容器で特異的に発現しているASIC3サブタイプの受容体である。このサブタイプの受容体は、プロトンによる活性化に伴って二相性の電流、すなわち最初の内向きのNa+電流に続いて持続的なカチオン電流が生じる。
ASICは網膜の機能に重要であり、明るい光に応答して保護を行う。ASIC2遺伝子を欠失すると、網膜の損傷感受性が増大する。野生型と比較してASIC2−/−網膜では、明るい光に応答したアポトーシスが増加する[8]。
また、ASIC1aチャネルは、発作を防ぐ役割も果たしている。発作によって脳内の神経細胞の活動は増大して制御不能となり、大量の酸性小胞が放出される[5]。これに応答してASIC1aチャネルが開き、発作の進行を抑えて保護を行うことが示されている。ASIC1aの遺伝子を欠失させると、発作が増幅することが明らかにされている[8]。
ASIC1aチャネルはpH 5.0–6.9の範囲で応答して特異的に開き、その活性化によってCa2+透過性がわずかに上昇してCa2+の流入が生じるため、虚血性脳損傷の病態に寄与する。また、ASIC1aチャネルは脱分極時に電位依存性Ca2+チャネルやNMDA受容体チャネルの活性化を促進し、細胞内のカルシウムの大幅な増加に寄与することで、細胞死が引き起こされる[11]。ASIC1aチャネルを介した細胞死の機構としては、ASIC1aが他のチャネルの活性化することでCa2+濃度が上昇し、細胞内にアポトーシスや壊死のシグナル伝達経路が形成されるという機構が考えられている[5]。遺伝子のノックアウトやASICの遮断によって脳梗塞の影響を受ける体積が60%も減少することが示されており、ASICチャネルがアシドーシスや虚血による神経細胞の損傷を原因とする病態の発生に主要な役割を果たしていることが示唆されている[11]。Ca2+毒性に対するASICとNMDAチャネルの役割を明らかにし、各チャネルの寄与を評価するため、双方のチャネルの遮断の影響の研究が行われている。双方のチャネルを遮断することで一方のチャネルだけの遮断よりも神経保護効果は高くなり、ASICの遮断はNMDAの遮断の効果の持続をもたらすことが明らかにされている[11]。
薬理[編集]
ASICは痛覚やいくつかの病理過程に関与しているため、薬剤による阻害標的として薬理学的重要性が存在する。ASICは中枢と末梢の双方の神経に存在する。ASIC活性の調節によって、慢性疼痛の不安や抑うつなどの行動・情動性症状を制御できる可能性がある。
ASICは、チャネルの種類や位置によって異なるものの、pHがおよそ6以下となると活性化することが観察されている。pHの低下は、組織の炎症や虚血性脳卒中、細胞の代謝の亢進による乳酸の蓄積など、さまざまな原因で引き起こされる。チャネルが活性化されるとナトリウムイオンの透過性が高まり、細胞は脱分極して活動電位の発火が誘導される。この活動電位は、低分子阻害剤によって調節することができる。
アミロライドはASIC阻害剤の一例であり、IC50はμMの範囲であるため極めて強力なものとは考えられていないものの、片頭痛に対するASICの阻害の影響の研究に利用されている。片頭痛の際には皮質拡延性抑制が観察され、イオンバランスの乱れとASICを活性化する荷電分子の放出が引き起こされる。齧歯類へのアミロライドの投与では片頭痛時の皮質拡延性抑制の減少が確認され、アミロライドはASICの競合阻害剤として作用することが示された。また、齧歯類ではアミロライドの使用により、ナトリウム-カルシウム交換輸送体の阻害による副作用がみられた。これらの交換輸送体が阻害されると細胞内のカルシウムの恒常性が乱れて細胞内のカルシウム濃度が高くなることから、アミロライドを使用した際の神経保護効果の低下が説明される。アミロライドによるASICの阻害で得られた知見は有望なものであり、治療の可能性を支持するものである。しかしながら、アミロライドは特異性と効力が低いため、薬剤として発売するためにはさらなる開発が必要である[11][12]。
低分子阻害剤A-317567はASICチャネルに対してアミロライドよりも高い特異性と効力を持ち、治療薬としてより高い可能性を示している。A-317567はASICチャネルの種類に対してほとんど選択性を示さず、in vivoではASIC特異的に作用し、アミロライド使用時にみられる副作用が回避されることが示された。また、A-317567は持続性電流の抑制を維持する能力を持ち、アシドーシスによる慢性症状に特に期待される[11]。
最も効果的で最もよく知られているASIC阻害剤はPcTX1である。PcTX1はASIC1aを特異的に阻害し、IC50はnMの範囲であり、他の既知のASIC阻害剤(μM範囲)よりも小さい。さらに、PcTX1は他の電位依存性イオンチャネルやリガンド依存性イオンチャネルを阻害しない。この阻害剤の構造は40個のアミノ酸からなり、ジスルフィド結合で連結されている。PcTX1は南米のタランチュラPsalmopoeus cambridgei由来のペプチド毒素として同定されたものである[11]。PcTX1をラットの扁桃体基底外側核に投与したところ、痛みと関係した情動や不安に関連する症状が大きく減少した[13]。
一般的に使用されている非ステロイド性抗炎症薬(NSAID)は、ASICの阻害に関与して痛みの調節に寄与していることが判明している。NSAIDの良く知られた作用機序は、主要な炎症性化合物であるプロスタグランジンの合成の阻害である。一方でNSAIDのイブプロフェンとアスピリンは、それぞれIC50値350 μMと260 μMでASICを阻害することが示されている。NSAIDは、急性疼痛、特に組織の炎症によって引き起こされる痛みの際のASIC電流を阻害し、痛みを検知する神経細胞へのシグナルを抑制すると考えられている[11]。
さらなるASIC阻害の薬理学的研究によって、慢性疼痛やアシドーシスを伴うさまざまな病態の患者に対する治療の選択肢が広がる可能性がある。さらに、ASICに対する創薬研究はチャネル自体の機能とその生理的意義に関してさらなる知識をもたらすと考えられる。
出典[編集]
- ^ “Structure of acid-sensing ion channel 1 at 1.9 Å resolution and low pH”. Nature 449 (7160): 316–322. (2007). doi:10.1038/nature06163. PMID 17882215.
- ^ a b “Biophysical properties of acid-sensing ion channels (ASICs)”. Neuropharmacology 94: 9–18. (July 2015). doi:10.1016/j.neuropharm.2014.12.016. PMID 25585135.
- ^ a b c d e f g h i j k “ASIC and ENaC type sodium channels: conformational states and the structures of the ion selectivity filters”. The FEBS Journal 284 (4): 525–545. (February 2017). doi:10.1111/febs.13840. PMID 27580245.
- ^ a b c “Acid-sensing ion channels: A new target for pain and CNS diseases”. Current Opinion in Drug Discovery & Development 12 (5): 693–704. (September 2009). PMC 3494879. PMID 19736627.
- ^ a b c d “Acidosis, acid-sensing ion channels, and neuronal cell death”. Molecular Neurobiology 44 (3): 350–8. (December 2011). doi:10.1007/s12035-011-8204-2. PMID 21932071.
- ^ a b “Acid-sensing ion channels and their modulators”. Biochemistry. Biokhimiia 79 (13): 1528–45. (2014). doi:10.1134/S0006297914130069. PMID 25749163.
- ^ “Structure and activity of the acid-sensing ion channels”. American Journal of Physiology. Cell Physiology 303 (7): C699–710. (October 2012). doi:10.1152/ajpcell.00188.2012. PMC 3469599. PMID 22843794.
- ^ a b c d e f g h “Acid-sensing ion channels: trafficking and synaptic function”. Molecular Brain 6: 1. (January 2013). doi:10.1186/1756-6606-6-1. PMC 3562204. PMID 23281934.
- ^ “Acid-sensing ion channels and their modulators”. Biochemistry. Biokhimiia 79 (13): 1528–45. (2014). doi:10.1134/S0006297914130069. PMID 25749163.
- ^ Baron, A.; Waldmann, R.; Lazdunski, M. (2002). “ASIC-like, proton-activated currents in rat hippocampal neurons. The Journal of Physiology, 539(2), 485–494 | 10.1113/jphysiol.2001.014837”. The Journal of Physiology 539 (Pt 2): 485–494. doi:10.1113/jphysiol.2001.014837. PMC 2290154. PMID 11882680.
- ^ a b c d e f g “Acid-sensing ion channels (ASICs) as pharmacological targets for neurodegenerative diseases”. Current Opinion in Pharmacology. Neurosciences 8 (1): 25–32. (February 2008). doi:10.1016/j.coph.2007.09.001. PMC 2267925. PMID 17945532.
- ^ “Pharmacology of acid-sensing ion channels - Physiological and therapeutical perspectives”. Neuropharmacology. Acid-Sensing Ion Channels in the Nervous System 94: 19–35. (July 2015). doi:10.1016/j.neuropharm.2015.01.005. PMID 25613302.
- ^ Aissouni, Youssef; El Guerrab, Abderrahim; Hamieh, Al Mahdy; Ferrier, Jérémy; Chalus, Maryse; Lemaire, Diane; Grégoire, Stéphanie; Etienne, Monique et al. (2017-03-02). “Acid-Sensing Ion Channel 1a in the amygdala is involved in pain and anxiety-related behaviours associated with arthritis”. Scientific Reports 7: 43617. doi:10.1038/srep43617. ISSN 2045-2322. PMC 5340794. PMID 28321113.
