クロロメタン
| クロロメタン | |
|---|---|

|
|
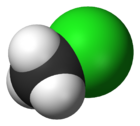
クロロメタン | |
別称 モノクロロメタン, 塩化メチル, Artic, フロン40, R 40, UN 1063 | |
| 識別情報 | |
| CAS登録番号 | 74-87-3 |
| PubChem | 6327 |
| EC番号 | 200-817-4 |
| KEGG | C19446 |
| ChEBI | |
| RTECS番号 | PA6300000 |
| |
| |
| 特性 | |
| 化学式 | CH3Cl |
| モル質量 | 50.49 g/mol |
| 外観 | 甘い芳香を持つ無色の気体 |
| 密度 | 2.22 kg/m3 (0 °C) |
| 融点 |
−97.7 °C (176 K) |
| 沸点 |
-24.2 °C (249 K) |
| 水への溶解度 | 5.325 g/l |
| log POW | 0.91 |
| 蒸気圧 | 490 kPa (20 °C) |
| 構造 | |
| 分子の形 | 四面体形 |
| 危険性 | |
| EU分類 | 非常に強い可燃性(F+), 有害(Xn), 発癌性 |
| NFPA 704 | |
| Rフレーズ | R10, R40, R48/20 |
| Sフレーズ | S9, S16, S33 |
| 引火点 | -46 °C |
| 発火点 | 625 °C |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
クロロメタンは、化学式がCH3Clで表されるハロメタンである。塩化メチル、R-40、HCC 40、フロン40とも呼ばれる可燃性の無色気体である。広義には、メタンの水素原子をいくつかの塩素原子で置換した化合物全般を指す。広義の意味で用いる場合には、1置換体と区別する意味でクロロメタン類とも呼ばれる。
かつて冷媒として用いられたが、発癌性、毒性があるため用いられなくなり、既に消費者の身近に存在していることはほとんどない。
日本では毒物及び劇物取締法により劇物に、PRTR法により第一種指定化学物質に指定されている。
歴史[編集]
1835年にフランスの化学者ジャン=バティスト・デュマとウジェーヌ=メルシオール・ペリゴーがメタノール、硫酸、塩化ナトリウムを加熱することにより得られることを発見した。現在でも似たような方法が用いられる。
宇宙では、チュリュモフ・ゲラシメンコ彗星や原始連星系IRAS 16293-2422から発見されている[1]。
生産[編集]
海中では微生物が日光と塩素を利用して、大量のクロロメタンを生産しているが、人によって使われるクロロメタンは全量が工業的に生産されている。
ほとんどのクロロメタンはメタノールと塩酸を反応させることにより得られている。
具体的には加熱したメタノール中に塩化水素を通すか、350℃に加熱したメタノールガスと塩化水素を酸化アルミニウム触媒中で反応させることで得られている。前者の方法では塩化亜鉛が触媒として用いられることがある。
一部ではメタンと塩素を400℃以上に加熱することで生産されている。しかしながら、この方法では多塩素化反応が起こってしまい、クロロメタンと同時にジクロロメタンやクロロホルム、四塩化炭素が副生成物として生産されてしまう。
利用[編集]
以前はエアコン[2]や冷蔵庫の冷媒として広く使われていたが、毒性のために利用されなくなった。また一時期ガソリンの添加剤となる鉛化合物の製造にも用いられていたが、環境保護の観点から鉛添加自体が減少していったため、利用もされなくなった。
その後重要な利用法として台頭してきたのは、シリコンポリマーの製造中間体としての利用である。また人工ゴムの製造にも用いられることがある。
有機化学においては、メチル化剤、あるいは塩素化剤として用いられる。他には油脂・石油・樹脂などの抽出剤として、またポリスチレン発泡体製造の際の発泡剤として用いられる。他にも局所麻酔剤、薬剤製造の際の中間体、低温重合の際の触媒担体、温度測定機材や恒温機材などに用いられる流動体、除草剤など様々な場所で用いられている。
安全性[編集]
ガスを吸入すると、中枢神経系が中毒に陥る。眠気、目まい、息切れと息詰まりを伴う呼吸困難、歩行困難、会話困難などの症状が出ることが多い。高濃度になると麻痺、発作、昏睡などを起こす。経口摂取した場合、吐き気と嘔吐が症状に表れる。冷媒などに用いられている液体を皮膚に直接接触させた場合は凍傷になる。目に接触した場合は視界がかすむ。
慢性的な暴露では変異原性があることが、マウスを用いた実験で確認されている。人間の場合では、胎児の脊椎、骨盤、足が正常に発育しない原因になると考えられているが、今のところ完全に証明されているわけではない。国際がん研究機関の発がん性調査では、グループ3の発がん性の評価ができない物質に分類されている。
可燃性の気体であり、引火性も持っている。1942年11月28日、ボストンのナイトクラブCocoanut Groveで起きた大火事(英語版)は、冷蔵庫から冷媒に用いられていたクロロメタンが漏れ、それに引火したことが原因であると、1997年に結論付けられた。
脚注[編集]
- ^ 地球外生命の指標として不適格か、赤ちゃん星にもクロロメタンが存在、アストロアーツ、2017年10月11日、2017年10月15日閲覧
- ^ 冷房食堂車が試運転『大阪毎日新聞』昭和11年8月16日夕刊(『昭和ニュース事典第5巻 昭和10年-昭和11年』本編p426 昭和ニュース事典編纂委員会 毎日コミュニケーションズ刊 1994年)



