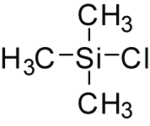
クロロトリメチルシラン
| クロロトリメチルシラン | |
|---|---|
| |

|

|
クロロトリメチルシラン | |
別称 TMSCl TMCS | |
| 識別情報 | |
| CAS登録番号 | 75-77-4 |
| PubChem | 6397 |
| ChemSpider | 6157 |
| RTECS番号 | VV2710000 |
| |
| |
| 特性 | |
| 化学式 | C3H9SiCl |
| モル質量 | 108.64 g/mol |
| 外観 | 無色液体、湿った空気中で揮発 |
| 密度 | 0.856 g/cm3, 液体 |
| 融点 |
-40 °C (233.2 K) |
| 沸点 |
57 °C (330.2 K) |
| 水への溶解度 | 反応 |
| 構造 | |
| 分子の形 | ケイ素中心の四面体 |
| 危険性 | |
| EU分類 | 可燃性 (F) 腐食性 (C) |
| NFPA 704 | |
| Rフレーズ | R11, R14, R20, R21, R35, R37 |
| Sフレーズ | S16, S26, S36, S37, S39, S45 |
| 引火点 | -28 °C |
| 発火点 | 400 °C |
| 関連する物質 | |
| 関連するハロシラン | フルオロトリメチルシラン ブロモトリメチルシラン ヨードトリメチルシラン |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
クロロトリメチルシラン (Trimethylsilyl chloride) は、化学において色々な目的で使われる有機ケイ素化合物である。(CH3)3SiClという化学式を持ち、標準状態では、水分の非存在下で安定な無色の液体である。四塩化ケイ素の3つの塩素原子をメチルリチウム等の求核性のメチル源で求核置換反応することで得られる。市販もされている。消防法に定める第4類危険物 第1石油類に該当する[1]。
利用[編集]
クロロトリメチルシランは、トリメチルシリル基の供給源としてや塩素の無水供給源として様々に利用される。アルコールやアミン等の官能基は、クロロトリメチルシランと容易に反応し、トリメチルシリルエーテルやトリメチルシリルアミンを形成する。新しく導入された官能基は、保護基として働くが、トリメチルシリル基の不安定性のため、その利用は制限される。
トリメチルシリル化は、化合物の揮発性を上げるためにも導入される。これにより、グルコース等の不揮発性の物質をガスクロマトグラフィーで分析できるようになる。クロロトリメチルシランは、金属アセチリドとも反応し、トリメチルシリルアルキンを形成する。これはアルキンの保護として有用である。
クロロトリメチルシランをアルコールと反応させると、塩化水素を生成し、この反応は、アルコール中での無水塩酸の製造に利用される。またカルボン酸、ケトンを、それぞれエステル、アセタールへと変換するのに用いられる。
アルファ位に水素原子を持つアルデヒド、ケトン、エステルは、トリエチルアミンやリチウムジイソプロピルアミドの存在下でクロロトリメチルシランを反応させることでトリメチルシリルエノールエーテルになる。これらの化合物は有機化学において広範な用途を持つ。エポキシ化やジヒドロキシ化による二重結合の酸化は、元のカルボニル基のアルファ位にヒドロキシ基を導入するのに用いられる。マスクされたエノール剤として向山アルドール反応にも用いられる。
クロロトリメチルシランはまた、次のようなトリメチルシリルハロゲンや擬ハロゲンの合成の出発物質として用いられる。
これらの化合物は、クロロトリメチルシランと(擬)ハロゲン塩 (MX)の置換反応によって合成される。
クロロトリメチルシランは、ガラス器具をシラン化し、表面の親油性を向上させるためにも用いられる[3]。
出典[編集]
- ^ 法規情報 (東京化成工業株式会社)
- ^ L. Birkofer and P. Wegner (1988). "Trimethylsilyl azide". Organic Syntheses (英語).; Collective Volume, vol. 6, p. 1030
- ^ Such as in Norbert Zander and Ronald Frank (2005). "The use of polystyrylsulfonyl chloride resin as a solid supported condensation reagent for the formation of esters: Synthesis of N-[(9-fluorenylmethoxy)carbonyl]-L-aspartic acid; α tert-butyl ester, β-(2-ethyl[(1E)-(4-nitrophenyl)azo]phenyl]amino]ethyl ester". Organic Syntheses (英語). 81: 235.


