カルニチンパルミトイルトランスフェラーゼI
カルニチンパルミトイルトランスフェラーゼI(英: carnitine palmitoyltransferase I、略称: CPT1、CPTI)は、長鎖アシルCoAのアシル基のL-カルニチンへの転移を触媒し、アシルカルニチンの形成を担うミトコンドリアの酵素である。カルニチンアシルトランスフェラーゼI(carnitine acyltransferase I, CAT1)、CoA:カルニチンアシルトランスフェラーゼ(CoA:carnitine acyl transferase, CCAT)、パルミトイルCoAトランスフェラーゼI(palmitoyl-CoA transferase I)などの名称でも知られ、カルニチンアシルトランスフェラーゼと呼ばれる酵素ファミリーに属する[1]。多くの場合、反応産物はパルミトイルカルニチンである(名称はこのことに由来する)が、他の脂肪酸も基質となる可能性がある[2][3]。この反応によって、その後のアシルカルニチンの細胞質基質からミトコンドリア膜間腔への移動が可能となる。
CPT1には、CPT1A、CPT1B、CPT1Cという3つのアイソザイムの存在が現在知られている。CPT1はミトコンドリア外膜に結合している。この酵素は、脂肪酸合成の方向決定段階の中間体であるマロニルCoAによって阻害される。脂肪酸代謝における役割のため、CPT1は糖尿病など多くの代謝疾患において重要である。結晶構造は未知であり、正確な作用機序は不明である。
構造[編集]

CPT1は、哺乳類の組織ではCPT1A、CPT1B、CPT1Cの3種類のアイソザイムが存在する膜内在性タンパク質である。CPT1AとCPT1Bは大部分の組織においてミトコンドリア外膜に発現しているが、これらの相対的比率は組織によって異なる。肝臓などの脂質生成組織ではCPT1Aが優勢である一方、心臓や骨格筋など高い脂肪酸酸化能を持つ組織や褐色脂肪細胞ではCPT1Bが優勢である[4][5]。どちらもペプチド鎖中の2つの膜貫通領域によってミトコンドリア外膜に内在しており、CPT1Aに関してはトポロジーの記載がなされている[6]。複数回膜貫通タンパク質であり、N末端とC末端はミトコンドリア外膜の細胞質基質側に露出し、2つの膜貫通ドメインをつなぐ短いループがミトコンドリア膜間腔へ突出している。
3つ目のアイソザイムであるCTP1Cは2002年に同定され、ミトコンドリアと小胞体の双方で発現している[7]。通常は神経(脳)でのみ発現しているが、特定のがんでは発現が変化している[8][9]。
CPT1の正確な構造はどのアイソザイムも未決定であるが、カルニチンアセチルトランスフェラーゼ(CRAT)など密接に関連したカルニチンアシルトランスフェラーゼの構造をもとにさまざまなin silicoモデルが作成されている[10]。
CPT1とCPT2、CRAT、カルニチンオクタノイルトランスフェラーゼ(COT)の間の重要な構造的差異は、CPT1には約160アミノ酸からなるN末端ドメインが存在するという点である。このN末端ドメインはCPT1の重要な阻害分子であるマロニルCoAにとって大きな意味を持ち、CPT1AのマロニルCoAによる阻害感受性を高くしたり低くしたりするスイッチのような作用を果たす[11]。
CPT1AとCPT1Bには2つの異なる結合部位が存在することが提唱されている。1つは「A部位」(A site)または「CoA部位」(CoA site)と呼ばれ、マロニルCoAとパルミトイルCoAの双方に加え、CoAを含む他の分子も結合できるようである。そのため、酵素はこれらの分子のCoA部分との相互作用によって結合を行っていることが示唆されている。マロニルCoAはこの部位でCPT1Aの競合的阻害剤として作用している可能性が示唆されている。2つ目の「O部位」(O site)は、A部位よりも強固にマロニルCoAを結合することが提唱されている。A部位とは異なり、O部位はマロニルCoAのマロン酸部分のジカルボニル基を介してマロニルCoAを結合する。A部位とO部位のいずれかへマロニルCoAが結合することで、カルニチンはCPT1Aに結合できなくなり、CPT1Aの作用は阻害される[12]。
機能[編集]
酵素反応機構[編集]
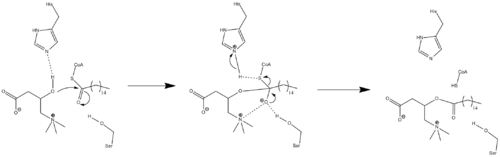
現時点では結晶構造は得られていないため、CPT1の正確な反応機構は不明である。反応機構として2つの異なる可能性が提唱されているが、その双方でヒスチジン473番残基が重要な触媒残基として関与している。カルニチンアセチルトランスフェラーゼに基づくモデルの1つが下に示されており、His473はカルニチンを脱プロトン化し、近接するセリン残基は四面体型オキシアニオン中間体を安定化する[1]。異なるモデルでは、Cys305、His473、Asp454からなる触媒三残基が触媒反応のアシル基転移段階を担うことが提唱されている[13]。この触媒機構には、Cys305を介したチオアシル-酵素共有結合中間体の形成が関与する。
生物学的機能[編集]
カルニチンパルミトイルトランスフェラーゼ系は、長鎖脂肪酸のβ酸化に必要不可欠な段階である。脂肪酸はミトコンドリア外膜上で(CoAとのチオエステル結合の形成という形で)活性化されるが、活性化された脂肪酸の酸化はミトコンドリアマトリックス内で行われる必要があるため、この転移系が必要となる。パルミトイルCoAなどの長鎖脂肪酸は、短鎖・中鎖脂肪酸とは異なり、ミトコンドリア内膜を通って自由に拡散することはできず、ミトコンドリアマトリックスへの輸送のためのシャトル系が必要である[14]。

カルニチンパルミトイルトランスフェラーゼIはカルニチンパルミトイルトランスフェラーゼ系の最初の構成要素かつ律速段階であり、パルミトイルCoA(アシルCoA)のパルミトイル基(アシル基)のカルニチンへの転移を触媒してパルミトイルカルニチン(アシルカルニチン)を形成する。その後、トランスロカーゼがパルミトイルカルニチン(アシルカルニチン)をミトコンドリア内膜を越えて輸送し、そこでパルミトイルCoA(アシルCoA)へ再変換される。
カルニチンはアシル基の受容体として作用することで、細胞内のCoA:アシルCoA比の調節に関与している可能性もある[15]。
調節[編集]
CPT1はマロニルCoAによって阻害されるが、その正確な阻害機構は不明である。CPT1の骨格筋・心臓型のアイソザイムであるCPT1Bは、CPT1Aと比較してマロニルCoAによる阻害に対する感受性が30–100倍高いことが示されている。この阻害は、将来的な代謝疾患治療を目的としたCPT1の調節の試みの際の良い標的となる[16]。
アセチルCoAカルボキシラーゼ(ACC)はアセチルCoAからマロニルCoAの形成を触媒する酵素であり、脂肪酸代謝の調節に重要である。ACC2のノックアウトマウスは野生型マウスと比較して体脂肪と体重が減少することが示されている。これはACC活性の低下に伴うマロニルCoA濃度の低下による効果である。マロニルCoA濃度の低下はCPT1の阻害を減弱し、最終的には脂肪酸酸化の増加を引き起こす[17]。心臓や骨格筋の細胞は脂肪酸合成能力が低いため、これらの細胞ではACCは純粋に調節酵素として作用する。
臨床的意義[編集]
CPT1AはカルニチンパルミトイルトランスフェラーゼI欠損症と関係している[18]。この希少疾患は、肝性脳症、低ケトン性低血糖、発作、乳児期の突然死のリスクを高める[19]。
CPT1は2型糖尿病、インスリン抵抗性と関係している。こうした疾患では、他の多くの健康問題とともに、遊離脂肪酸(FFA)濃度の上昇、骨格筋への脂肪の蓄積、筋肉の脂肪酸酸化能力の低下が引き起こされる。CPT1はこれらの症状への寄与が示唆されている。高血糖や高インスリン血症によるマロニルCoA濃度の上昇はCPT1を阻害し、筋肉や心臓のミトコンドリアへの長鎖脂肪酸の輸送を低下させ、これらの細胞での脂肪酸酸化が低下する。ミトコンドリアへの長鎖脂肪酸の輸送の低下はFFA濃度の上昇として観察され、骨格筋への脂肪の蓄積をもたらす[20][21]。
CPT1は脂肪酸代謝において重要であるため、他の多くの代謝疾患の治療法の開発においても着目すべき有用な酵素である可能性がある[22]。
HIVとの関係[編集]
HIVのVprタンパク質は、PPARβ/δを介してPDK4やCPT1のmRNAの発現を亢進させる[23]。培養Jurkat細胞でにおけるshRNAライブラリによるスクリーニングからは、CPT1AのノックダウンによってHIV-1の複製が阻害されることが示されている[24]。
出典[編集]
- ^ a b “Crystal structure of carnitine acetyltransferase and implications for the catalytic mechanism and fatty acid transport”. Cell 112 (1): 113–22. (Jan 2003). doi:10.1016/S0092-8674(02)01228-X. PMID 12526798.
- ^ “Genomics of the human carnitine acyltransferase genes”. Molecular Genetics and Metabolism 71 (1–2): 139–53. (2000). doi:10.1006/mgme.2000.3055. PMID 11001805.
- ^ “Carnitine palmitoyltransferases 1 and 2: biochemical, molecular and medical aspects”. Molecular Aspects of Medicine 25 (5–6): 495–520. (2004). doi:10.1016/j.mam.2004.06.004. PMID 15363638.
- ^ “Mouse white adipocytes and 3T3-L1 cells display an anomalous pattern of carnitine palmitoyltransferase (CPT) I isoform expression during differentiation. Inter-tissue and inter-species expression of CPT I and CPT II enzymes”. The Biochemical Journal 327 (1): 225–31. (Oct 1997). doi:10.1042/bj3270225. PMC 1218784. PMID 9355756.
- ^ “Adipose fatty acid oxidation is required for thermogenesis and potentiates oxidative stress-induced inflammation”. Cell Reports 10 (2): 266–279. (Jan 2015). doi:10.1016/j.celrep.2014.12.023. PMC 4359063. PMID 25578732.
- ^ “Topology of carnitine palmitoyltransferase I in the mitochondrial outer membrane.”. Biochemical Journal 323 (3): 711–718. (May 1997). doi:10.1042/bj3230711. PMC 1218374. PMID 1218374.
- ^ “A novel brain-expressed protein related to carnitine palmitoyltransferase I”. Genomics 80 (4): 433–442. (Oct 2002). doi:10.1006/geno.2002.6845. PMID 12376098.
- ^ “Carnitine palmitoyltransferase 1C: From Cognition to Cancer”. Progr Lipid Res 61: 134–148. (Dec 2016). doi:10.1016/j.plipres.2015.11.004. PMID 26708865.
- ^ “Downregulation of fatty acid oxidation by involvement of HIF-1α and PPARγ in human gastric adenocarcinoma and its related clinical significance”. Journal of Physiology and Biochemistry 77 (2): 249–260. (May 2021). doi:10.1007/s13105-021-00791-3. PMID 33730333.
- ^ “Structural model of carnitine palmitoyltransferase I based on the carnitine acetyltransferase crystal”. The Biochemical Journal 379 (Pt 3): 777–784. (May 2004). doi:10.1042/BJ20031373. PMC 1224103. PMID 14711372.
- ^ “An environment-dependent structural switch underlies the regulation of carnitine palmitoyltransferase 1A”. J Biol Chem 286 (49): 42545–42554. (2011). doi:10.1074/jbc.M111.306951. PMC 3234983. PMID 21990363.
- ^ “Definition by functional and structural analysis of two malonyl-CoA sites in carnitine palmitoyltransferase 1A”. The Journal of Biological Chemistry 282 (25): 18212–24. (Jun 2007). doi:10.1074/jbc.M700885200. PMID 17452323.
- ^ “Cysteine-scanning mutagenesis of muscle carnitine palmitoyltransferase I reveals a single cysteine residue (Cys-305) is important for catalysis”. The Journal of Biological Chemistry 280 (6): 4524–4531. (Feb 2005). doi:10.1074/jbc.M400893200. PMID 15579906.
- ^ Berg, Jeremy M. (2007). Biochemistry. John L. Tymoczko, Lubert Stryer, Lubert Stryer (6th ed ed.). New York: W.H. Freeman. ISBN 0-7167-8724-5. OCLC 61500079
- ^ “Structure and function of carnitine acyltransferases”. Annals of the New York Academy of Sciences 1033 (1): 17–29. (Nov 2004). Bibcode: 2004NYASA1033...17J. doi:10.1196/annals.1320.002. PMID 15591000.
- ^ “The first 28 N-terminal amino acid residues of human heart muscle carnitine palmitoyltransferase I are essential for malonyl CoA sensitivity and high-affinity binding”. Biochemistry 39 (4): 712–717. (Feb 2000). doi:10.1021/bi9918700. PMID 10651636.
- ^ “Acetyl-CoA carboxylase 2 mutant mice are protected against obesity and diabetes induced by high-fat/high-carbohydrate diets”. Proceedings of the National Academy of Sciences of the United States of America 100 (18): 10207–10212. (Sep 2003). Bibcode: 2003PNAS..10010207A. doi:10.1073/pnas.1733877100. PMC 193540. PMID 12920182.
- ^ “Expression analysis of two mutations in carnitine palmitoyltransferase IA deficiency”. Journal of Human Genetics 47 (7): 342–7. (2002). doi:10.1007/s100380200047. PMID 12111367.
- ^ “Carnitine palmitoyltransferase 1A (CPT1A) P479L prevalence in live newborns in Yukon, Northwest Territories, and Nunavut”. Molecular Genetics and Metabolism 101 (2–3): 200–204. (2010). doi:10.1016/j.ymgme.2010.07.013. PMID 20696606.
- ^ “Malonyl coenzyme A and the regulation of functional carnitine palmitoyltransferase-1 activity and fat oxidation in human skeletal muscle”. The Journal of Clinical Investigation 110 (11): 1687–93. (Dec 2002). doi:10.1172/JCI15715. PMC 151631. PMID 12464674.
- ^ “Observations on the affinity for carnitine, and malonyl-CoA sensitivity, of carnitine palmitoyltransferase I in animal and human tissues. Demonstration of the presence of malonyl-CoA in non-hepatic tissues of the rat”. The Biochemical Journal 214 (1): 21–8. (Jul 1983). doi:10.1042/bj2140021. PMC 1152205. PMID 6615466.
- ^ “Regulatory enzymes of mitochondrial beta-oxidation as targets for treatment of the metabolic syndrome”. Obesity Reviews 11 (5): 380–8. (2010). doi:10.1111/j.1467-789X.2009.00642.x. PMID 19694967.
- ^ “HIV-1 Vpr enhances PPARβ/δ-mediated transcription, increases PDK4 expression, and reduces PDC activity”. Molecular Endocrinology 27 (9): 1564–76. (Sep 2013). doi:10.1210/me.2012-1370. PMC 3753422. PMID 23842279.
- ^ “A genome-wide short hairpin RNA screening of jurkat T-cells for human proteins contributing to productive HIV-1 replication”. The Journal of Biological Chemistry 284 (29): 19463–73. (Jul 2009). doi:10.1074/jbc.M109.010033. PMC 2740572. PMID 19460752.
