アルゴンフッ素水素化物
| アルゴンフッ素水素化物 | |
|---|---|
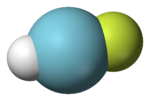
| |
| IUPAC名 | ? |
| 別名 | Argon fluoride hydride |
| 組成式 | HArF |
| 式量 | 59.954 g/mol |
| 形状 | 不明 |
| CAS登録番号 | [163731-16-6] |
| 密度と相 | 不明 g/cm3, |
| 水への溶解度 | 不明 g/100 mL ( °C) |
| 融点 | (分解) −256 °C |
アルゴンフッ素水素化物(アルゴンフッそすいそかぶつ、argon fluorohydride)とは知られている唯一のアルゴン(Ar)化合物(2006年現在)である。低温マトリックス中で生成される。
2000年8月24日、フィンランドの科学者 Markku Räsänen によりネイチャー誌上で合成法とその赤外スペクトルが報告された[1]。 分子式は HArF。
合成法[編集]
アルゴンとフッ化水素の混合気体を、低温(およそ −265.5 ℃、7.5 K)まで冷却したヨウ化セシウムの基盤上に吹き付け固化させた後、127-160 nm の紫外線を照射してフッ化水素を光解離させ、その後わずかに温度を上げながら(およそ −255 ℃、18 K)アルゴンと反応させる。
- 紫外光
アルゴンが水素やフッ素と結合していることは赤外分光法により確認された。40Ar を基質とした生成系からは Ar-H、Ar-Fの伸縮、および H-Ar-F の変角振動に対応した新しい吸収がそれぞれ 1969.4, 435.7, 687.0 cm−1 に観測された。一方、36Ar からの系ではそれらが 1972.3, 442.9, 689.3 cm−1 に動いており、アルゴンの同位体効果が現れていることが確認された。
また、このネイチャー誌の報告では、これらの赤外吸収のうちAr-H伸縮振動、H-Ar-F の変角振動は、27 K 以上にマトリックスの温度を上げると観測されなくなることが報告されている。その後の研究で、昇温によるそれらの吸収の消滅に伴い高波数側 (それぞれ2016.3, 2020.8 cm−1 および 693.5,697.0 cm−1) に新たな吸収が出現することが報告され、これらの変化は結晶中での安定化が起こったものであると結論づけられた[2]。
この化学結合は物質が17 K(-256℃)以下の温度に保たれている場合にのみ安定であり、それ以上ではフッ化水素とアルゴンに分解する。
関連項目[編集]
参考文献[編集]
- ^ Leonid Khriachtchev, Mika Pettersson, Nino Runeberg, Jan Lundell and Markku Räsänen,"A stable argon compound" Nature, 406, 874-876 (2000). DOI: 10.1038/35022551
- ^ Leonid Khriachtchev, Mika Pettersson, Antti Lignell, and Markku Räsänen, "A More Stable Configuration of HArF in Solid Argon" J. Am. Chem. Soc.; 2001; 123(35) pp 8610, doi:10.1021/ja016197s


