「全身麻酔」の版間の差分
話題別に段落分けしました。 |
Anesth Earth (会話 | 投稿記録) →歴史: 一部改訳。仮リンク変更 |
||
| (9人の利用者による、間の116版が非表示) | |||
| 1行目: | 1行目: | ||
{| class="infobox" |
|||
[[ファイル:Ana arbeitsplatz.JPG|thumb|right|250px|全身麻酔にて使われる器具の一例]] |
|||
! colspan="2" class="infobox-above" style="background-color: lightblue" |全身麻酔 |
|||
|- |
|||
| colspan="2" class="infobox-image" |[[File:Ana_arbeitsplatz.JPG|フレームなし]]<div class="infobox-caption">全身麻酔にて使われる器具の一例</div> |
|||
|- |
|||
! class="infobox-label" scope="row" |[[MeSH]] |
|||
| class="infobox-data" |<span class="reflink plainlinks nourlexpansion">[https://www.nlm.nih.gov/cgi/mesh/2016/MB_cgi?field=uid&term=D000768 D000768]</span> |
|||
|- |
|||
! class="infobox-label" scope="row" |[[MedlinePlus]] |
|||
| class="infobox-data" |<span class="reflink plainlinks nourlexpansion">[https://medlineplus.gov/ency/article/007410.htm 007410]</span> |
|||
|- class="noprint" |
|||
| colspan="2" class="infobox-full-data" |<div style="text-align: right;">[[[wikidata:Q166543|edit on Wikidata]]]</div> |
|||
|} |
|||
'''全身麻酔'''(ぜんしんますい、{{lang-en-short|General anesthesia}})は、痛覚刺激を与えても患者が覚醒しないように、人為的に誘発される[[意識]]喪失である<ref name=":10">{{Cite web |website=American Society of Anesthesiologists. |title=Position on Monitored Anesthesia Care |quote=Approved by the House of Delegates on October 25, 2005, and last amended on October 17, 2018 |url=http://www.asahq.org/~/media/Sites/ASAHQ/Files/Public/Resources/standards-guidelines/position-on-monitored-anesthesia-care.pdf |access-date=6 November 2022}}</ref>。この効果は、静脈内または吸入の[[全身麻酔薬]]を投与することで得られ、しばしば[[鎮痛剤]]および{{仮リンク|神経筋遮断薬|en|neuromuscular blocking agent}}が併用される。手術中は[[自発呼吸]]が十分でないことが多く、気道を保護するための介入が必要となることが多い<ref name=":10" />。全身麻酔は一般に、[[手術室]]では患者にとって耐え難い痛みを伴う外科手術を可能にするために、[[集中治療室]]や[[救急救命室]]では、重症患者の[[気管挿管]]や[[機械換気 (医学)|機械換気]]を容易にするために実施される。 |
|||
日本では、全身麻酔の目標は「'''麻酔の3要素'''」、すなわち鎮静・鎮痛・筋弛緩とされることが多い<ref>{{Citation|title=特集 麻酔 Part 1 麻酔総論(生理学)麻酔科医による術中管理の目的と実際 2.鎮痛薬総論-薬理作用,使用方法,使用上の注意点|last=佐倉|first=考信|date=2021-10-01|url=https://doi.org/10.11477/mf.3102200904|publisher=株式会社医学書院|doi=10.11477/mf.3102200904|access-date=2023-02-23}}</ref>。有害反射の抑制も加えて'''麻酔の4要素'''とされることもあるが、これは元はWoodbridgeらが1957年に提唱した麻酔深度の概念に遡ることができる<ref>{{Cite journal|last=Woodbridge|first=Philip D.|date=1957-07-01|title=CHANGING CONCEPTS CONCERNING DEPTH OF ANESTHESIAE|url=https://doi.org/10.1097/00000542-195707000-00002|journal=Anesthesiology|volume=18|issue=4|pages=536–550|doi=10.1097/00000542-195707000-00002|issn=0003-3022}}</ref>。英語圏では、{{仮リンク|無意識状態|en|unconsciousness}}、[[健忘]]、[[鎮痛]]、[[自律神経系]]の反射消失、場合によっては[[骨格筋]]の[[麻痺]]を達成することが全体目標とされることも多い。すなわち、4要素ないしは5要素となっており、鎮静において無意識状態と健忘が別個の評価項目となっていることによる。 |
|||
'''全身麻酔'''(ぜんしんますい、{{lang-en-short|General anesthesia}})は、[[麻酔]]方法の一つ。[[手術]]する部位のみを麻酔する[[局所麻酔]]に対し、全身麻酔は脳を含めた全身を麻酔するため意識が消失する。 |
|||
患者や処置に最適な麻酔薬の組み合わせは、通常、[[麻酔科医]]が、患者、[[外科医]]、歯科医師、または手術処置を行う他の施術者と相談しながら選択する<ref name=":11">{{Cite book |title=Miller's anesthesia |date=2020 |publisher=Elsevier |editor=Michael A. Gropper |isbn=978-0-323-61264-7 |edition=Ninth |location=Philadelphia, PA |oclc=1124935549}}</ref>{{Rp|page=58|pages=000–000}}。 |
|||
全身麻酔が薄れるまでの間、患者は異変を訴えることができないため、[[麻酔科医]]が患者のそばで注意深く監視・観察する必要がある。全身麻酔の長所は、あらゆる部位の手術に用いることが出来、麻酔の目的として鎮静(意識消失)、筋弛緩、鎮痛、有害な[[副交感神経系|副交感神経]]反射の抑制が挙げられる。局所麻酔と異なり、全身麻酔はこれらの条件を全て満たすことができる。 |
|||
== 歴史 == |
== 歴史 == |
||
2世紀から3世紀に書かれた『[[三国志 (歴史書)|三国志]]』には、中国[[後漢]]末期に[[華陀]]が「麻沸散」という麻酔薬を用いて手術を行ったと記載されている。この「麻沸散」は全身麻酔薬であろうと考えられているが、どのようなものであったかは明らかではない。 |
全身麻酔の試みは、古代[[シュメール]]人、[[バビロニア]]人、[[アッシリア人]]、[[エジプト|エジプト人]]、[[ギリシャ人]]、[[ローマ人]]、[[インド人]]、[[中国人]]の書物から、歴史的にたどることができる。2世紀から3世紀に書かれた『[[三国志 (歴史書)|三国志]]』には、中国[[後漢]]末期に[[華陀]]が「麻沸散」という麻酔薬を用いて手術を行ったと記載されている。この「麻沸散」は全身麻酔薬であろうと考えられているが、どのようなものであったかは明らかではない。 |
||
[[中世]]には、[[東洋]]においてもヨーロッパにおいても科学は医学的に大きな進歩を遂げた。 |
|||
正確に確認できる全身麻酔の記録としては、文化元年10月13日(1804年11月14日)に[[華岡青洲]]が行った[[乳癌]]の手術が初出である。このとき用いられた麻酔薬「[[通仙散]]」は[[チョウセンアサガオ]]に[[トリカブト]]や[[トウキ]]などを配合した薬品であった。西洋では、[[1846年]]に[[アメリカ合衆国|アメリカ]]で[[ウィリアム・T・G・モートン]]が行った[[ジエチルエーテル]]による手術が初の全身麻酔手術となる。エーテルは取り回しに難があったため、すぐに[[クロロホルム]]に取って代わられた。 |
|||
[[ルネサンス|ルネッサンス期]]には、[[解剖学]]と[[手術|外科学]]に大きな進歩があった。しかし、このような進歩にもかかわらず、手術は依然として最後の治療法であった。手術は[[痛み]]を伴うため、多くの患者は手術を受けるよりも死を選んだ。全身麻酔の発見については、誰が最も功績を残したかについて定説は無いが、18世紀後半から19世紀初頭にかけてのいくつかの科学的発見が、近代的麻酔技術の導入と発展に不可欠であった<ref>{{Cite journal|date=June 2015|title=Medical Renaissance|journal=Journal of Investigative Surgery|volume=28|issue=3|pages=127–130|DOI=10.3109/08941939.2015.1054747|PMID=26065591}}</ref>。 |
|||
[[1934年]]に、アメリカの{{仮リンク|アーネスト・ヴォルワイラー|en|Ernest H. Volwiler}}によって開発された[[チオペンタール]]は、現在に至るまで全身麻酔薬として使用されており、[[世界保健機関|WHO]]のエッセンシャル・ドラッグにも指定されている。 |
|||
正確に確認できる全身麻酔の記録としては、文化元年10月13日(1804年11月14日)に[[華岡青洲]]が行った[[乳癌]]の手術が初出である<ref>{{Cite journal|date=January 2017|title=Two Japanese Pioneers in Anesthesiology: Seishū Hanaoka and Gendai Kamada|journal=Journal of Anesthesia History|volume=3|issue=1|pages=19–23|DOI=10.1016/j.janh.2016.12.002|PMID=28160985}}</ref>。このとき用いられた麻酔薬「[[通仙散]]」は[[チョウセンアサガオ]]に[[トリカブト]]や[[トウキ]]などを配合した薬品であった。西洋では、[[1846年]]に[[アメリカ合衆国|アメリカ]]で[[ウィリアム・T・G・モートン]]が行った[[ジエチルエーテル]]による手術が初の全身麻酔手術となる。エーテルは引火性が問題であり、すぐに[[クロロホルム]]に取って代わられたが、クロロホルムも毒性のために死者が相次ぎ、使われなくなるのに時間はかからなかった。 |
|||
なお全身麻酔のうち、なぜ吸入麻酔が効くのかについては、[[21世紀]]に入った今でも作用機序が分からないままである。 |
|||
19世紀後半には、近代外科学への移行を可能にする二つの大きな飛躍があった。{{仮リンク|病原菌説|en|Germ theory of disease}}の理解により、外科手術における感染予防技術の開発と応用が急速に進んだのである。防腐法({{Lang-en|antisepsis}})はやがて無菌法({{Lang-en|asepsis}})に変わり、外科手術の[[合併症]]と[[死亡率]]は、以前の時代よりはるかに低くなった<ref>{{Cite journal|date=July 2012|title=Asepsis and bacteriology: a realignment of surgery and laboratory science|journal=Medical History|volume=56|issue=3|pages=308–334|DOI=10.1017/mdh.2012.22|PMID=23002302|PMC=3426977}}</ref>。 |
|||
== 手順 == |
|||
以下、典型的な[[開腹手術]]を想定して概略を述べる。ただし術前の合併症や、年齢・性別・体重など、患者の状態に応じ、異なる手順が用いられる。 |
|||
{{Seealso|無菌}} |
|||
まず、円滑に麻酔を行うために、[[手術室]]入室前に薬剤投与を行う(前投薬と呼ばれる)。現在は[[麻酔薬]]そのものの有害作用が軽減したため、成人では前投薬が行われないことも多い。 |
|||
同時に、[[薬理学]]や[[生理学]]の分野でも大きな進歩があり、全身麻酔や痛みのコントロールが可能になった。 |
|||
前投薬には、唾液分泌、気道内分泌の抑制、有害な反射の抑制のために、[[アトロピン]]や[[スコポラミン]]といった[[抗コリン薬]]を用いる。また不安の除去、鎮静、催眠の目的に[[ジアゼパム]]などを投与する。これらは以前、病室にて投与を済ませておくことが多かったが、近年は疼痛や合併症を伴う筋肉注射による[[副作用]]を避けるため、手術室入室後に投与することもある。 |
|||
[[1934年]]に、アメリカの{{仮リンク|アーネスト・ヴォルワイラー|en|Ernest H. Volwiler}}によって開発された[[チオペンタール]]は、現在に至るまで[[全身麻酔薬]]として使用されており、[[WHO必須医薬品モデル・リスト|WHOの必須医薬品リスト]]にも指定されている。 |
|||
手術室に入室し、末梢静脈ルート確保ののち、[[硬膜外麻酔]]を実施する。硬膜外麻酔用の[[カテーテル]]は術中だけでなく、術後の鎮痛にも用いることができる。そして十分な[[酸素]]投与を行う。 |
|||
20世紀には、[[気管挿管]]やその他の{{仮リンク|高度な気道確保|en|advanced airway management}}技術を日常的に使用することにより、全身麻酔の安全性と有効性が改善された。また、[[生体情報モニタ|モニタリング]]の大幅な進歩や、[[薬物動態学]]的および[[薬力学]]的特性が改善された新しい[[麻酔薬]]も、この傾向に貢献した。最終的には、麻酔科医のための標準化されたトレーニングプログラムが、この時期に出現した。 |
|||
次に、患者を入眠させるために、おもに静脈麻酔薬である[[バルビツール酸系]]や[[プロポフォール]]と、合成[[麻薬]]である[[フェンタニル]]や[[レミフェンタニル]]を組み合わせて用いる。患者の入眠後はマスクにより気道確保、人工呼吸ができることを目視で確認し、[[筋弛緩剤|筋弛緩薬]]を投与する。筋弛緩薬としては[[ロクロニウム]]が用いられることが多い。 |
|||
== 目的 == |
|||
筋弛緩薬の効果が得られたら、よりいっそう確実な気道確保のため、[[気管挿管]]を行う。その後は[[人工呼吸]]関連機器を作動させる。 |
|||
全身麻酔には多くの目的があり、あらゆる外科手術に日常的に使用されている。適切な手術時の麻酔には、以下のような目標が求められる。 |
|||
# 催眠・無意識(意識の喪失) |
|||
導入後は、[[吸入麻酔薬]]であるセボフルランやデスフルラン、または[[静脈麻酔薬]]であるプロポフォールを持続的に投与し、麻酔の効果維持を行う。かつては[[亜酸化窒素]](笑気)が用いられたが、近年では環境への影響([[温室効果]])や、術後に嘔気[[嘔吐]]を招くことから、敬遠されることが多い。 |
|||
# 鎮痛(痛みに対する反応の喪失) |
|||
# 健忘(記憶の喪失) |
|||
# 不動(運動反射の消失) |
|||
# 麻痺(骨格筋の弛緩)<ref name="Hewer_1937">{{Cite journal|date=August 1937|title=The Stages and Signs of General Anaesthesia|journal=British Medical Journal|volume=2|issue=3996|pages=274–276|DOI=10.1136/bmj.2.3996.274|PMID=20780832|PMC=2087073}}</ref> |
|||
== 生化学的作用機序 == |
|||
手術終了予定時刻もしくは、その進捗が終わりに近づくと、それに合わせて麻酔薬を徐々に減量し、施行者が手術終了を宣言することで、その量を完全に止める。その結果患者の意識が次第に回復するため、手を握ることができる、深呼吸ができる、目線を動かすことが出来るなど、筋弛緩薬の効果の消失、麻酔薬による呼吸抑制の有無などを確認し、条件を満たすなら[[気管チューブ]]を抜去する(抜管)。そして十分な確認ののち、病棟へ帰室させる。 |
|||
全身麻酔薬の[[生化学|生化学的]]な{{仮リンク|全身麻酔の作用機序|en|Theories of general anaesthetic action|label=作用機序}}はよく分かっていない<ref>{{Cite journal|date=September 2016|title=General Anesthetics and Neurotoxicity: How Much Do We Know?|journal=Anesthesiology Clinics|volume=34|issue=3|pages=439–451|DOI=10.1016/j.anclin.2016.04.001|PMID=27521190|PMC=5477636}}</ref>。植物も動物同様に麻酔薬による作用をうけることは分かっている<ref>{{Cite news |title=Plants, Like People, Succumb to Anesthesia |url=https://blogs.scientificamerican.com/artful-amoeba/plants-like-people-succumb-to-anesthesia-video/ |access-date=26 January 2018 |newspaper=[[Scientific American]] |date=26 January 2018}}</ref>。意識を失わせるために、麻酔薬は無数の作用部位を持ち、[[中枢神経系]](CNS)に複数のレベルで作用する。全身麻酔は、[[大脳皮質]]、[[視床]]、[[網様体|網様体賦活系]]、[[脊髄]]を含む中枢神経系構成要素の機能を抑制・変化させるのが一般的である。麻酔状態に関する現在の理論では、中枢神経系における標的部位だけでなく、無意識と関連した{{仮リンク|神経ネットワーク|en|Neural network}}や覚醒回路も特定されており、一部の麻酔薬は特定の睡眠活性部位を活性化する可能性があることが分かっている<ref>{{Cite journal|last=Moody|first=Olivia A.|last2=Zhang|first2=Edlyn R.|last3=Vincent|first3=Kathleen F.|last4=Kato|first4=Risako|last5=Melonakos|first5=Eric D.|last6=Nehs|first6=Christa J.|last7=Solt|first7=Ken|date=2021-05-01|title=The Neural Circuits Underlying General Anesthesia and Sleep|journal=Anesthesia and Analgesia|volume=132|issue=5|pages=1254–1264|DOI=10.1213/ANE.0000000000005361|ISSN=1526-7598|PMID=33857967|PMC=8054915}}</ref>。全身麻酔薬の分子薬理学的標的は、[[GABAA受容体|GABA<sub>A</sub>]]と[[NMDA型グルタミン酸受容体|NMDAグルタミン酸受容体]]であると考えられている。全身麻酔は、神経信号の抑制性伝達を増強するか、あるいは興奮性伝達を減少させるという仮説が立てられた<ref>{{Cite journal|last=Lambert|first=David G.|date=2020-05-01|title=Mechanisms of action of general anaesthetic drugs|url=https://www.anaesthesiajournal.co.uk/article/S1472-0299(20)30028-X/abstract|journal=Anaesthesia & Intensive Care Medicine|volume=21|issue=5|pages=235–237|language=English|DOI=10.1016/j.mpaic.2020.02.006|ISSN=1472-0299}}</ref>。ほとんどの揮発性麻酔薬はGABA<sub>A</sub>[[アゴニスト]]であることが判明しているが、受容体への作用部位は不明なままである<ref>{{Cite journal|last=Woll|first=Kellie A.|last2=Zhou|first2=Xiaojuan|last3=Bhanu|first3=Natarajan V.|last4=Garcia|first4=Benjamin A.|last5=Covarrubias|first5=Manuel|last6=Miller|first6=Keith W.|last7=Eckenhoff|first7=Roderic G.|date=August 2018|title=Identification of binding sites contributing to volatile anesthetic effects on GABA type A receptors|journal=The FASEB Journal|volume=32|issue=8|pages=4172–4189|DOI=10.1096/fj.201701347R|ISSN=0892-6638|PMID=29505303|PMC=6044061}}</ref>。[[ケタミン]]は非競合的な{{仮リンク|NMDA受容体拮抗薬|en|NMDA receptor antagonist}}である<ref>{{Cite journal|last=Zhang|first=Youyi|last2=Ye|first2=Fei|last3=Zhang|first3=Tongtong|last4=Lv|first4=Shiyun|last5=Zhou|first5=Liping|last6=Du|first6=Daohai|last7=Lin|first7=He|last8=Guo|first8=Fei|last9=Luo|first9=Cheng|date=August 2021|title=Structural basis of ketamine action on human NMDA receptors|url=https://pubmed.ncbi.nlm.nih.gov/34321660|journal=Nature|volume=596|issue=7871|pages=301–305|bibcode=2021Natur.596..301Z|DOI=10.1038/s41586-021-03769-9|ISSN=1476-4687|PMID=34321660}}</ref>。 |
|||
[[吸入麻酔薬]]は、化学構造と特性から、[[細胞膜]]を標的とすることが示唆されているが、その正確なメカニズムは100年以上謎のままであった。2020年の研究では、吸入麻酔薬([[クロロホルム]]と[[イソフルラン]])が[[脂質ラフト]]への{{仮リンク|ホスホリパーゼD|en|Phospholipase D|label=ホスホリパーゼD2}}の局在を乱し、シグナル伝達分子である[[ホスファチジン酸]]の産生につながることが実証された。シグナル伝達分子は{{仮リンク|カスケード反応|en|Biochemical cascade}}を引き起こし、最終的にはTWIK関連K+チャネル(TREK-1)を活性化させる。ホスホリパーゼD2遺伝子欠損 (PLDnull)ミバエは麻酔抵抗性であることが示されており、この結果により、吸入麻酔薬の標的が細胞膜介在性であることが確立された<ref>{{Cite journal|date=June 2020|title=Studies on the mechanism of general anesthesia|journal=Proceedings of the National Academy of Sciences of the United States of America|volume=117|issue=24|pages=13757–13766|bibcode=2020PNAS..11713757P|DOI=10.1073/pnas.2004259117|PMID=32467161|PMC=7306821}}</ref><ref>{{Cite web |title=全身麻酔薬(General Anesthetics) - 薬理学電子教科書 - Confluence |url=https://drugacademy.atlassian.net/wiki/spaces/PHARMACOLO/pages/458822/General+Anesthetics |website=drugacademy.atlassian.net |access-date=2023-01-17}}</ref>。 |
|||
== 術前評価 == |
== 術前評価 == |
||
{{Seealso|麻酔前評価}} |
|||
患者の状態、手術の内容を吟味し最適な麻酔方法を検討する。 |
|||
予定手術の前に、麻酔科医はカルテを調べたり、患者の問診をしたりして、病歴に関する情報を入手し、周術期のリスクを判断する。問診に基づき、麻酔科医は麻酔計画を立て、手術に最適な薬剤の組み合わせと投与量を決定する。また、安全で効果的な手術を行うために、[[生体情報モニタ|モニタリング機器]]を追加する必要がある場合もある。この評価で重要なのは、患者の年齢、性別、[[ボディマス指数]](BMI)、病歴、手術歴、現在服用している薬、絶食時間などである<ref>{{Cite journal|date=August 2019|title=Anesthetic considerations for lung resection: preoperative assessment, intraoperative challenges and postoperative analgesia|journal=Annals of Translational Medicine|volume=7|issue=15|pages=356|DOI=10.21037/atm.2019.03.67|PMID=31516902|PMC=6712248}}</ref><ref>{{Cite journal|date=December 2019|title=Evaluation of preoperative risk factors for postpancreatectomy hemorrhage|journal=Langenbeck's Archives of Surgery|volume=404|issue=8|pages=967–974|DOI=10.1007/s00423-019-01830-w|PMID=31650216|PMC=6935390}}</ref> 。術前の徹底的かつ正確な評価は、麻酔計画の効果的な安全性を確保するために極めて重要である。例えば、アルコールや{{仮リンク|レクリエーショナルドラッグ|en|Recreational drug use|label=違法薬物|redirect=1}}を大量に摂取している患者が、その事実を開示しなかった場合、手術中に薬物投与量が不足し、{{仮リンク|術中覚醒|en|anaesthesia awareness}}や術中[[高血圧]]の原因となる可能性がある<ref>{{Cite journal|date=2019-02-04|title=Preoperative Interventions for Alcohol and Other Recreational Substance Use: A Systematic Review and Meta-Analysis|journal=Frontiers in Psychology|volume=10|pages=34|DOI=10.3389/fpsyg.2019.00034|PMID=30778307|PMC=6369879}}</ref><ref>{{Cite journal|date=2018-10-18|title=Incidences and factors associated with perioperative cardiac arrest in trauma patients receiving anesthesia|journal=Risk Management and Healthcare Policy|volume=11|pages=177–187|DOI=10.2147/rmhp.s178950|PMID=30425598|PMC=6201994}}</ref>。また、一般的に使用されている薬剤は麻酔薬と相互作用する可能性があり、そのような使用状況を開示しないと、手術中のリスクが高まる可能性がある。また、最後の食事のタイミングが正確でないと、食物の[[誤嚥]]の危険性が高まり、重篤な合併症につながる可能性がある<ref name=":112">{{Cite book |title=Miller's anesthesia |date=2020 |publisher=Elsevier |editor=Michael A. Gropper |isbn=978-0-323-61264-7 |edition=Ninth |location=Philadelphia, PA |oclc=1124935549}}</ref>。 |
|||
麻酔前の評価で重要なのは、開口状況の確認と[[咽頭]]の軟部組織の観察を含む患者の気道の評価である<ref>{{Cite journal|date=June 2016|title=Airway management and training in obstetric anaesthesia|journal=Current Opinion in Anesthesiology|volume=29|issue=3|pages=261–267|DOI=10.1097/ACO.0000000000000309|PMID=26844863}}</ref>。歯の状態や[[歯冠]]の位置を確認し、頸部の柔軟性と伸展性を観察する<ref>{{Cite journal|date=June 2020|title=Institutional preparedness to prevent and manage anaesthesia-related 'can't intubate, can't oxygenate' events in Australian and New Zealand teaching hospitals|journal=Anaesthesia|volume=75|issue=6|pages=767–774|DOI=10.1111/anae.14909|PMID=31709522}}</ref><ref>{{Cite journal|date=December 2019|title=Comparison of forces acting on maxillary incisors during tracheal intubation with different laryngoscopy techniques: a blinded manikin study|journal=Anaesthesia|volume=74|issue=12|pages=1563–1571|DOI=10.1111/anae.14815|PMID=31448404|postscript=6}}</ref>。最も一般的に行われている気道評価は{{仮リンク|マランパチ分類|en|Mallampati score}}で、口を開けて舌を出した状態で軟口蓋の構造を見ることができるかどうかで気道を評価するものである。マランパチテストだけでは精度が低いため、マランパチテストに加え、開口度、甲状頤間距離、頸部可動域、下顎骨突出などの評価も日常的に行われている。また、気道の形態異常が疑われる患者には、内視鏡検査や[[超音波検査]]で気道の評価を行った上で、[[気道確保]]を計画することもある<ref>{{Cite journal|last=Roth|first=Dominik|last2=Pace|first2=Nathan L.|last3=Lee|first3=Anna|last4=Hovhannisyan|first4=Karen|last5=Warenits|first5=Alexandra-Maria|last6=Arrich|first6=Jasmin|last7=Herkner|first7=Harald|date=2018-05-15|title=Airway physical examination tests for detection of difficult airway management in apparently normal adult patients|journal=The Cochrane Database of Systematic Reviews|volume=5|issue=5|pages=CD008874|DOI=10.1002/14651858.CD008874.pub2|ISSN=1469-493X|PMID=29761867|PMC=6404686}}</ref>。 |
|||
=== 患者のあらゆる状態の評価 === |
|||
手術対象の疾患のみならず、これまでの病歴、合併症、基礎疾患についても家族などに聞き込んで評価し、投薬する麻酔の種類を選出するための判断材料として定めていく。 |
|||
{{仮リンク|アメリカ麻酔科学会|en|American Society of Anesthesiologists}}では全身状態を6つに分類しており、[[ASA-PS]](ASA physical status)と呼んでいる。手術前の[[ASA-PS]]と予後は相関する。 |
|||
* [[虚血性心疾患]]、[[不整脈]]などの[[循環器疾患]]の有無。 |
|||
* [[気管支喘息]]、[[慢性閉塞性肺疾患]]などの[[呼吸器疾患]]の有無。 |
|||
* [[高血圧]]、[[糖尿病]]、[[高脂血症]]をはじめとする[[生活習慣病]]や、[[喫煙]]歴、[[医薬品]]、[[酒]]、薬物の使用歴。 |
|||
* 体型。特に極度の[[肥満]]。 |
|||
* [[気道確保]]は容易であるか。 |
|||
* [[アレルギー]]はないか。 |
|||
* 最終飲食は何日の何時頃か。これは'''緊急手術の場合重要'''である。 |
|||
* 各種検査データ([[血液検査]]、[[心電図]])および画像検査([[X線写真]]、[[コンピュータ断層撮影|CT]]画像、[[核磁気共鳴画像法|MRI]]画像)など。 |
|||
* 過去に手術や麻酔を受けて、異常が生じた血縁者はいないか。 |
|||
* 過去の麻酔歴、手術の記録があれば、それも参考にする。 |
|||
* 手術の方法や手順に不明な点があれば、主治医・術者に確認する。 |
|||
アメリカ麻酔科学会([[:en:American Society of Anesthesiologists]])では全身状態を6つに分類しており、[[ASA-PS]](ASA physical status)と呼んでいる。手術前の[[ASA-PS]]と予後は相関することが分かっている。 |
|||
通常の待機手術であれば十分な時間をかけた術前評価が可能だが、緊急手術では不十分になってしまうことが多い。 |
|||
=== 麻酔方法の選択 === |
|||
実施する予定の手術方式や患者の状態に応じ、適切な麻酔方法を選択する。全身麻酔単独ではなく[[硬膜外麻酔]]や[[局所麻酔|伝達麻酔]]など、ほかの麻酔方法を併用することもある。合併症、基礎疾患によっては使用できない薬剤もあるためよく検討する。 |
|||
=== 術前訪問 === |
|||
患者を訪問し、診察や問診、実際に行う予定である麻酔方法の説明などを行う。手術前の患者はいろいろな疑問、不安を抱えている。これらに真摯に耳を傾け、的確な説明をし不安を取り除く。術前訪問は患者の状態を自分の目で確認し情報を得ることのみならず、良好な医師と患者の関係を築く第一歩となる。 |
|||
{| class="wikitable" style="float:right" |
|||
|+ 麻酔の併発症による死亡率など |
|||
! 麻酔が原因と思われる死亡率 |
|||
| 麻酔10万件に約1件 |
|||
|- |
|||
! 麻酔が原因と思われる心停止 |
|||
| 麻酔10万件に約5件 |
|||
|- |
|||
! 重大な血圧低下 |
|||
| 麻酔1万件に約1件 |
|||
|- |
|||
! 重大な低酸素状態 |
|||
| 麻酔1万件に約2件 |
|||
|} |
|||
日本の麻酔説明パンフレットをドイツのものと比較した報告があり<ref> |
|||
{{Cite journal |
|||
|author=嶋田文彦, 野坂修一 |
|||
|year=2008 |
|||
|title=麻酔説明関連文書の比較 |
|||
|journal=日本臨床麻酔学会誌 |
|||
|volume=28 |
|||
|issue=7 |
|||
|pages=993-999 |
|||
|url=https://doi.org/10.2199/jjsca.28.993 |
|||
|doi=10.2199/jjsca.28.993 |
|||
}}</ref>、それによると日本の場合は麻酔の併発症による死亡率について記載されている。同文献に例として挙げられている表は、下記のように患者が記憶しやすい1桁の数値を表として自然に注意がいく形になっている。 |
|||
予定手術であれば十分な時間をかけた[[麻酔前評価|術前評価]]が可能だが、緊急手術の術前評価は時間的な制限が多い。 |
|||
しかし、日本の麻酔説明パンフレットは、病院によって、頁数やどれだけ多くの数値が記載されているかにばらつきがみられる<ref> |
|||
{{Cite web |
|||
|author=日本医科大学附属病院 麻酔科 |
|||
|url=http://www.nms.ac.jp/NMS/anesth/anesthguide.pdf |
|||
|title=麻酔を受ける患者さんへ |
|||
|language=日本語 |
|||
|date=2006年4月1日 |
|||
|accessdate=2010年3月1日 |
|||
}}</ref><ref> |
|||
{{Cite web |
|||
|author=広島大学病院 麻酔・疼痛治療科 |
|||
|url=http://home.hiroshima-u.ac.jp/anesth/exp_file/masuisetumeisho7.pdf |
|||
|title=麻酔を受けられる皆様に―第7版― |
|||
|language=日本語 |
|||
|accessdate=2010年3月1日 |
|||
}}</ref>。 |
|||
== 前投薬 == |
== 前投薬 == |
||
{{Seealso|麻酔前投薬}} |
|||
* 術前の不安を取り除いたり、術中の有害な自律神経反射を抑制したりする目的で行われる投薬のことである。 |
|||
* 古典的な方法は[[鎮静薬]]と抗コリン薬を入室30分前程度に投与する。鎮静には[[ヒドロキシジン]](アタラックスP)などを用い、鎮痛にはペンタゾシン(ソセゴン、ペンタジン)などを用いる。これらは[[筋肉注射]]されることが多い。場合によっては胃酸分泌抑制薬も前投与する。また、[[硫酸アトロピン]]は筋肉注射を避けたり、使用されない傾向がある。 |
|||
* 近年では疼痛や合併症を伴う筋肉注射を避けるため、内服の[[ベンゾジアゼピン]]を用いたり、[[アトロピン]]などは手術室入室後に投与することが好まれる。抗コリン薬は入室後、静脈ルートから投与しても術中の有害反射を抑制する十分な効果は得られるとされている。 |
|||
全身麻酔を行う前に、麻酔科医は麻酔の質や安全性を補ったり向上させたりするために、1種類以上の薬剤を投与することがある。これを[[麻酔前投薬|前投薬]]という。[[麻酔前投薬|前投薬]]の多くには弱い鎮静効果があり、手術中に使用する麻酔薬の量を減らすことができる場合が多い<ref name=":113">{{Cite book |title=Miller's anesthesia |date=2020 |publisher=Elsevier |editor=Michael A. Gropper |isbn=978-0-323-61264-7 |edition=Ninth |location=Philadelphia, PA |oclc=1124935549}}</ref>{{Rp|pages=643,646,1057}}。 |
|||
== 導入 == |
|||
もっぱら用いられるのは以下の3種類の方法である。静脈麻酔薬としては、プロポフォールや、チアミラール、[[チオペンタール]]などの[[バルビツール酸系]]、[[ミダゾラム]]などの[[ベンゾジアゼピン]]が用いられる。 |
|||
海外でよく使われる前投薬に{{仮リンク|αアドレナリン作動薬|en|Alpha-adrenergic agonist|label=α2アドレナリン作動薬}}である[[クロニジン]]がある<ref>{{Cite journal|date=February 2006|title=Clonidine in paediatric anaesthesia: review of the literature and comparison with benzodiazepines for premedication|url=http://www3.interscience.wiley.com/cgi-bin/fulltext/118557949/HTMLSTART|journal=Acta Anaesthesiologica Scandinavica|volume=50|issue=2|pages=135–143|DOI=10.1111/j.1399-6576.2006.00940.x|PMID=16430532}}</ref><ref>{{Cite journal|date=April 2010|title=Premedication with clonidine is superior to benzodiazepines. A meta analysis of published studies|journal=Acta Anaesthesiologica Scandinavica|volume=54|issue=4|pages=397–402|DOI=10.1111/j.1399-6576.2009.02207.x|PMID=20085541|postscript=6}}</ref>。{{仮リンク|術後シバリング|en|Postanesthetic shivering}}<ref>{{Cite journal|last=Vanderstappen|first=I.|last2=Vandermeersch|first2=E.|last3=Vanacker|first3=B.|last4=Mattheussen|first4=M.|last5=Herijgers|first5=P.|last6=Van Aken|first6=H.|date=1996-04|title=The effect of prophylactic clonidine on postoperative shivering. A large prospective double-blind study|url=https://pubmed.ncbi.nlm.nih.gov/8686824/|journal=Anaesthesia|volume=51|issue=4|pages=351–355|doi=10.1111/j.1365-2044.1996.tb07747.x|issn=0003-2409|pmid=8686824}}</ref>、[[術後嘔気嘔吐|術後の悪心・嘔吐]]<ref>{{Cite journal|last=Oddby-Muhrbeck|first=Eva|last2=Eksborg|first2=Staffan|last3=Bergendahl|first3=Henrik T. G.|last4=Muhrbeck|first4=Olle|last5=Lönnqvist|first5=Per Arne|date=2002-05|title=Effects of clonidine on postoperative nausea and vomiting in breast cancer surgery|url=https://pubmed.ncbi.nlm.nih.gov/11981150/|journal=Anesthesiology|volume=96|issue=5|pages=1109–1114|doi=10.1097/00000542-200205000-00013|issn=0003-3022|pmid=11981150}}</ref>、{{仮リンク|覚醒時せん妄|en|Emergence delirium}}を軽減する<ref name=":113" />{{Rp|page=2259|pages=000–000}}。しかし、2021年の無作為化比較試験で、クロニジンは就学前の子どもには[[抗不安薬|抗不安]]作用が少なく、[[鎮静]]作用が強いことが実証された。経口クロニジンは最大効果発現には45分ほどかかる<ref>{{Cite journal|last=Bromfalk|first=Åsa|last2=Myrberg|first2=Tomi|last3=Walldén|first3=Jakob|last4=Engström|first4=Åsa|last5=Hultin|first5=Magnus|editor-last=Cravero|editor-first=Joseph|date=November 2021|title=Preoperative anxiety in preschool children: A randomized clinical trial comparing midazolam, clonidine, and dexmedetomidine|url=https://onlinelibrary.wiley.com/doi/10.1111/pan.14279|journal=Pediatric Anesthesia|volume=31|issue=11|pages=1225–1233|language=en|DOI=10.1111/pan.14279|ISSN=1155-5645|PMID=34403548}}</ref>。クロニジンの欠点は低血圧と徐脈であるが、[[高血圧]]と[[頻脈]]の患者には有利に働く可能性がある<ref>{{Cite journal|date=March 2018|title=Clonidine as a preoperative sedative|journal=Special Care in Dentistry|volume=38|issue=2|pages=80–88|DOI=10.1111/scd.12269|PMID=29364538}}</ref>。もう一つのα-2アドレナリン作動薬である[[デクスメデトミジン]]は、短期間の鎮静効果(24時間以内)のためによく使用される。デクスメデトミジンとある種の非定型抗精神病薬は、非協力的な子供にも使用されることがある<ref>{{Cite journal|last=Manning|first=Alexander N.|last2=Bezzo|first2=Leah K.|last3=Hobson|first3=Jamie K.|last4=Zoeller|first4=Justine E.|last5=Brown|first5=Courtney A.|last6=Henderson|first6=Kristin J.|date=October 2020|title=Dexmedetomidine Dosing to Prevent Pediatric Emergence Delirium|url=https://pubmed.ncbi.nlm.nih.gov/32990204|journal=AANA Journal|volume=88|issue=5|pages=359–364|ISSN=2162-5239|PMID=32990204}}</ref>。日本では2023年現在、クロニジンもデクスメデトミジンも前投薬としては[[適応外使用]]となる。 |
|||
;急速導入(Rapid Induction) |
|||
:静脈麻酔薬を用いて入眠させる、通常の麻酔導入方法。 |
|||
;緩徐導入(Slow Induction) |
|||
:吸入麻酔薬によりマスク換気で入眠させ、麻酔を深くしたあと、静脈路確保を行う麻酔導入方法。覚醒状態で静脈ラインの確保が困難な小児などに用いる。 |
|||
;迅速導入(Rapid sequence induction) |
|||
:以前はCrash Inductionとも呼ばれた。緊急時の手術の場合などで、胃内容物があるような場合([[フルストマック]])に誤嚥性肺炎の危険性が高いと考えられる場合に行う方法で、十分な酸素化と胃内容物吸引ののち、静脈麻酔薬と筋弛緩薬を一度に投与し、マスク換気を行わずに気管挿管を行う方法。入眠後は輪状軟骨を圧迫して食道を閉鎖して胃内容物の逆流を防ぐ。 |
|||
[[ベンゾジアゼピン|ベンゾジアゼピン系]]も前投薬としてよく使用される薬物である。ベンゾジアゼピン系で最もよく使用されるのは[[ミダゾラム]]であり、速効性と短時間作用が特徴である。ミダゾラムは、小児の[[分離不安障害|分離不安]]など{{仮リンク|術前不安|en|preoperative anxiety}}の軽減に効果的である<ref>{{Cite journal|last=El Batawi|first=Hisham Yehia|date=2015|title=Effect of preoperative oral midazolam sedation on separation anxiety and emergence delirium among children undergoing dental treatment under general anesthesia|journal=Journal of International Society of Preventive & Community Dentistry|volume=5|issue=2|pages=88–94|DOI=10.4103/2231-0762.155728|ISSN=2231-0762|PMID=25992332|PMC=4415335}}</ref>。また、[[術後嘔気嘔吐|術後の悪心・嘔吐]]の軽減、軽度の鎮静、交感神経抑制、[[前向性健忘]]をもたらす<ref name=":113" />{{Rp|page=657|pages=000–000}}。 |
|||
===導入時に用いられるテクニック=== |
|||
; Priming principle |
|||
: 一度に全量の筋弛緩薬を投与するのではなく、前もって少量を投与してから全量を投与し挿管する方法。[[アセチルコリン受容体]]の一部をあらかじめ少量の[[筋弛緩薬]]で占拠しておくことで、非脱分極性筋弛緩薬でも迅速な効果の出現が得られる。 |
|||
; Precurarization |
|||
: 脱分極性筋弛緩薬の線維束性攣縮による胃内容物の逆流などを防ぐために、あらかじめ少量の非脱分極性筋弛緩薬を投与しておく方法。 |
|||
[[メラトニン]]は、[[睡眠薬|催眠]]作用、[[抗不安薬|抗不安]]作用、[[鎮静薬|鎮静]]作用、[[鎮痛]]作用、[[抗てんかん薬|抗けいれん]]作用があるため、成人および小児の麻酔前投薬として有効であることが判明している。メラトニンの前投薬後は、ミダゾラムよりも回復が早く、術後の{{仮リンク|精神運動性興奮|en|Psychomotor agitation|label=興奮}}や{{仮リンク|覚醒時せん妄|en|Emergence delirium|label=せん妄}}の発生率も減少する<ref name="Naguib2007">{{Cite journal|date=January 2007|title=Melatonin and anesthesia: a clinical perspective|journal=Journal of Pineal Research|volume=42|issue=1|pages=12–21|DOI=10.1111/j.1600-079X.2006.00384.x|PMID=17198534}}</ref>。メラトニンは、ベンゾジアゼピンと比較して、成人患者の周術期不安の軽減に同様の効果があることが示されている<ref>{{Cite journal|date=December 2020|title=Melatonin for preoperative and postoperative anxiety in adults|journal=The Cochrane Database of Systematic Reviews|volume=2020|issue=12|pages=CD009861|DOI=10.1002/14651858.CD009861.pub3|PMID=33319916|PMC=8092422}}</ref>。メラトニンも日本では前投薬は適応外使用となる。 |
|||
== 維持 == |
|||
プロポフォール、あるいは吸入麻酔薬を持続投与して麻酔の維持が行われる。近年のバランス麻酔では良好な鎮痛と覚醒を得るために、吸入麻酔薬やプロポフォールなどの鎮静薬を少なめにして[[オピオイド]]を主体とした全身麻酔を行うことが好まれる。[[硬膜外麻酔]]を併用した場合、鎮痛薬も鎮静薬も少なくてすみ、自己調整鎮痛法のPCA)による鎮痛も非常に良好である。筋弛緩薬も減量できることが多い。2007年(平成19年)に日本で発売された[[レミフェンタニル]](アルチバ)は短時間で作用し、長時間多量に使ってもただちに効果が消失する、理想的なオピオイドであり、これにより麻酔維持がオピオイド主体に変わりつつある。しかし術後鎮痛が新たな問題となっている。基本的には術中はバイタルサインと手術の進行具合を見ながら、麻酔の深度が適切であるのか、鎮静、鎮痛は十分か、出血量はどうか、輸液の量や尿量は適切かといったところを考えながら全身管理をしていくこととなる。 |
|||
麻酔前投薬のもう一つの例として、[[交感神経β受容体遮断薬|βアドレナリン拮抗薬]]の術前投与があり、これは心臓手術後の頻脈性不整脈を軽減することが示されている<ref>{{Cite journal|date=March 2018|title=Perioperative beta-blockers for preventing surgery-related mortality and morbidity|journal=The Cochrane Database of Systematic Reviews|volume=2018|issue=3|pages=CD004476|DOI=10.1002/14651858.CD004476.pub3|PMID=29533470|PMC=6494407|postscript=6}}</ref>。しかし、心臓以外の手術では、β遮断薬による有害事象の増加との関連も指摘されている。麻酔科医は、術後の悪心・嘔吐を防ぐために、[[オンダンセトロン]]、[[ドロペリドール]]、[[デキサメタゾン]]などの[[制吐薬|制吐剤]]を少なくとも1種類は投与することがある<ref name=":113" />{{Rp|page=2260|pages=000–000}}。[[非ステロイド性抗炎症薬|NSAIDs]]も鎮痛前投薬として用いられることがあり、[[フェンタニル]]などの[[オピオイド]]の必要性をしばしば減少させる。また、[[メトクロプラミド]]のような[[消化管機能改善薬|消化管運動促進剤]]、[[ファモチジン]]のような[[抗ヒスタミン薬|ヒスタミン拮抗剤]]も使用される<ref name=":113" />{{Rp|page=2260|pages=000–000}}。 |
|||
; 吸入麻酔 |
|||
: よく利用されるのは[[亜酸化窒素]](笑気)、セボフルラン(セボフレン)、デスフルラン(スープレン)である。以前は鎮痛・鎮静・筋弛緩の万能薬と考えられていたこともあったようだが、現在は筋弛緩薬、オピオイドを適切に使い、吸入麻酔薬は鎮静目的でのみ用いる、バランス麻酔が主体である。 |
|||
; 静脈麻酔 |
|||
: 麻酔維持に利用できるのはプロポフォール(ディプリバン、プロポフォールマルイシ)である。 |
|||
; [[筋弛緩薬]] |
|||
: 体動を防いだり、筋緊張を取り除いて手術操作をしやすくする目的で用いるが、十分な麻酔深度があると判断するとこれ以上は投薬しないことも多い。高濃度の局所麻酔薬を用いて硬膜外麻酔を行えば、十分な腹壁の筋弛緩は得られる。 |
|||
; 直腸麻酔(注腸麻酔) |
|||
: 直腸に直接、注入する。麻酔はあまり効果がないので幼小児における検査や包帯交換、小手術などで用いられる。[[チオペンタール]]や[[抱水クロラール]]が使用される。 |
|||
非薬物的な麻酔前介入としては、[[認知行動療法]]、[[音楽療法]]、[[アロマテラピー|アロマセラピー]]、催眠[[マッサージ]]、術前説明ビデオ、誘導イメージによるリラックス療法などがある<ref>{{Cite journal|last=Wang|first=Rulin|last2=Huang|first2=Xin|last3=Wang|first3=Yuan|last4=Akbari|first4=Masod|date=2022-04-11|title=Non-pharmacologic Approaches in Preoperative Anxiety, a Comprehensive Review|journal=Frontiers in Public Health|volume=10|pages=854673|DOI=10.3389/fpubh.2022.854673|ISSN=2296-2565|PMID=35480569|PMC=9035831}}</ref>。これらの手法は、特に小児や[[知的障害]]のある患者に有効である。ビデオゲームによって、感覚刺激を最小限に抑えたり、気晴らしをすることは、全身麻酔の導入前または導入中の不安の軽減に役立つと考えられる。しかし、この種の不安の軽減に最も効果的な非薬物学的アプローチを確認するためには、より大規模で質の高い研究が必要である<ref name="Manyande2015">{{Cite journal|date=July 2015|title=Non-pharmacological interventions for assisting the induction of anaesthesia in children|journal=The Cochrane Database of Systematic Reviews|volume=2015|issue=7|pages=CD006447|DOI=10.1002/14651858.CD006447.pub3|PMID=26171895|PMC=8935979}}</ref>。[[麻酔前投薬|前投薬]]および麻酔導入時の両親の同席は、小児の不安を軽減することが示されていない。同席を希望する親を積極的に阻止すべきではなく、同席を希望しない親を無理強いすべきではないことが示唆されている<ref name="Manyande2015" />。 |
|||
== 体温 == |
|||
麻酔中は熱喪失の増大と熱産生の低下、および[[体温]]調節機構の[[閾値]]低下により[[低体温症]]になりやすい。[[周術期]]における低体温はよくみられる症状であるが、36℃以下になると、出血量・[[輸液]]量増加、[[止血]]・[[凝固系]]の異常、術創部[[感染]]率増加([[免疫]]能低下)、[[心筋]][[虚血]]発生率の有意な増加などをもたらす。例外として、急激な血圧低下時などでの低体温は[[脳]]保護的に作用するが、きわめて限定的である。 |
|||
== 麻酔深度 == |
|||
また、[[体温]]をモニターすることで、[[悪性高熱症]]を発症した場合、迅速に処置できる<ref name="周術期管理チームテキスト">周術期管理チームテキスト 第3版, 公益社団法人 日本麻酔科学会(発行), 2016年8月10日発行</ref>。 |
|||
{{仮リンク|ゲデルの麻酔深度分類|en|Guedel's classification}}は、1937年に{{仮リンク|アーサー・アーネスト・ゲデル|en|Arthur Ernest Guedel}}が発表したもので<ref name="Hewer_19372">{{Cite journal|date=August 1937|title=The Stages and Signs of General Anaesthesia|journal=British Medical Journal|volume=2|issue=3996|pages=274–276|DOI=10.1136/bmj.2.3996.274|PMID=20780832|PMC=2087073}}</ref>、 麻酔の4つの段階を表している。新しい麻酔薬や麻酔導入技術により、麻酔の開始と回復がより迅速に行われるようになったが(いくつかの段階は完全にスキップされることもある)、この原則は変わっていない。 |
|||
; 1期 |
|||
=== 体温管理法 === |
|||
: 1期は、導入期とも呼ばれ、導入剤を投与してから意識を失うまでの期間である。この段階で、患者は記憶喪失を伴わない鎮痛状態から記憶喪失を伴う鎮痛状態へと進行する。この時、患者は会話を続けることができ、視覚障害を訴えることがある。 |
|||
* 室温の維持:30℃以上にすると、体温低下予防に効果的だが、執刀医の不快感が増大することによる手術行為の中断や失敗の誘因になる可能性があるため、限界がある。 |
|||
; 2期 |
|||
* 輸液・輸血の加温:大量かつ急速に投与する必要がある場合に有効。 |
|||
: 第2期は、興奮期またはせん妄期とも呼ばれ、意識を失った後、興奮状態やせん妄状態が顕著になる時期である。この段階では、患者の[[呼吸]]と[[拍動|心拍]]が不規則になることがある。さらに、不随意運動、嘔吐、[[無呼吸|呼吸の中断]]、[[散瞳|瞳孔散大]]がみられることもある。痙性運動、嘔吐、不規則な呼吸の組み合わせは患者の気道を損なう可能性があるため、この段階の時間を最小限に抑え、できるだけ早く第3期に到達するためには、速効性の薬剤を用いる。 |
|||
* 温水ブランケット |
|||
; 3期 |
|||
* 温風ブランケット |
|||
: 第3期は外科的麻酔期とも呼ばれ、骨格筋が弛緩し、嘔吐は停止する。呼吸抑制と眼球運動の停止がこの段階の特徴である。患者は意識を失い、手術ができる状態になる。この段階は4つの局面に分けられる。 |
|||
* 送気の加温と加湿 |
|||
:# 眼球が上転し、その後固定され、眼瞼反射と嚥下反射が失われる。まだ規則的な自発呼吸がある。 |
|||
* [[人工心肺装置|体外循環]]:体温を急速に変化させることができる。 |
|||
:# 角膜反射と喉頭反射が失われる。 |
|||
* 体表のクーリング |
|||
:# 瞳孔反射が消失し、腹筋・肋間筋の完全弛緩が認められる。ほとんどの手術に対応できる理想的な麻酔レベル。 |
|||
* [[アミノ酸]]輸液:[[異化]]の亢進を防ぎ、熱産生を促す。 |
|||
:# 横隔膜の完全麻痺と不規則な浅い腹式呼吸が起こる<ref>{{Cite journal|date=September 2015|title=Effects of anesthesia on the respiratory system|journal=Best Practice & Research. Clinical Anaesthesiology|volume=29|issue=3|pages=273–284|DOI=10.1016/j.bpa.2015.08.008|PMID=26643094}}</ref>。 |
|||
; 4期 |
|||
: 第4期は、昏睡期とも呼ばれ、手術刺激量に対して麻酔薬の投与量が多すぎる場合に起こり、患者は重度の[[脳幹]]または[[延髄]]の抑制を受け、呼吸が停止し、[[心血管虚脱]]を生じる可能性がある。この段階は、心血管系と呼吸器系のサポートがなければ致死的である<ref name="Hewer_19372" />。 |
|||
== 麻酔の導入 == |
|||
麻酔科学においてよく用いられる用語の「'''導入'''」とは、麻酔薬投与から[[気道確保]]を完了して、手術可能な状態となるまでの全身麻酔の初期段階のことを指す。全身麻酔は、通常、[[手術室]]または手術室に隣接する麻酔専用室で行われる。他に、[[内視鏡]]室、[[集中治療室]]、[[放射線科]]、[[循環器学|循環器科]]、[[救急医療|救急外来]]、救急車などでも行われる。災害現場など、患者の救出が不可能または非現実的な場所でも行われることがある。 |
|||
[[中枢神経]]や重要[[臓器]]の温度(中枢温)は、体の中心部から[[血液]]を導体として運ばれ、さまざまな部位の温度変化が観察できる。いずれの部位も臓器の温度以外にさまざまな影響がある。 |
|||
* [[血液]]温:正確で感度がよいが、[[肺動脈カテーテル]]の挿入が必要で、挿入時は高度の技術が要求される。 |
|||
* [[食道]]温:食道下部3分の1に留置することで、[[心臓]]の温度(血液温)ときわめて高い相関を示す。 |
|||
* [[鼓膜]]温:非接触型の[[プローブ]]により非侵襲的かつ衛生的に、連続測定が可能であるが、プローブと装着部位に隙間があると、低く測定されてしまう。 |
|||
* [[膀胱]]温:[[サーミスタ]]つき膀胱[[カテーテル]]で測定する。 |
|||
* [[直腸]]温:排便の影響で中枢温よりも低く測定される場合がある。事前絶食を行っていれば、その影響は小さい。 |
|||
* [[気管]]温:[[吸気]]の影響で中枢温よりも低く測定される場合がある。 |
|||
* [[口腔]]温:[[唾液]]の影響で中枢温よりも低く測定される場合がある。 |
|||
* 前[[額]]深部温:[[血流]]が豊富な頭部で衛生的に測定できるが、特殊なモニター機器が必要である。 |
|||
* [[腋窩]]温:腋窩を3分以上閉鎖腔として測定する必要がある。 |
|||
麻酔薬は、[[吸入麻酔薬|吸入]]、[[注射]]([[注射|静脈内]]、[[筋肉内注射|筋肉内]]、{{仮リンク|皮下組織|en|Subcutaneous tissue|label=皮下}})、経口、直腸など、さまざまな経路で投与されることがある。麻酔薬は循環系に入ると、[[中枢神経系]]および自律神経系にある生化学的[[活性部位]]に到達する。 |
|||
== 麻酔における脳波 == |
|||
以下は特記のないものは『周術期管理チームテキスト』第3版(公益社団法人 日本麻酔科学会、2016年8月10日発行)より。 |
|||
ほとんどの全身麻酔は、静脈内または吸入により導入される。一般的に使用される静脈内導入剤には、[[プロポフォール]]、[[チオペンタール|チオペンタールナトリウム]]、[[エトミデート]]、{{仮リンク|メトヘキシタール|en|methohexital}}、[[ケタミン]]などがある。[[吸入麻酔薬|吸入麻酔]]は、静脈内投与が困難な場合(例、小児)、気道確保が困難と予想される場合、または患者が希望する場合に選択されることがある。[[セボフルラン]]は、他の薬剤に比べて{{仮リンク|気管気管支樹|en|tracheobronchial tree}}への刺激が少ないため、吸入麻酔での導入に最もよく使用される薬剤である<ref>{{Cite journal|date=July 1995|title=Neurocirculatory responses to sevoflurane in humans. A comparison to desflurane|journal=Anesthesiology|volume=83|issue=1|pages=88–95|DOI=10.1097/00000542-199507000-00011|PMID=7605024}}</ref>。 |
|||
* 脳細胞の電気活動を頭皮に設置した電極を通して記録する。 |
|||
* [[脳波]]は覚醒度に応じてさまざまな変化をきたすため、麻酔中の鎮静度の度具合を計る(知る)指標として活用されている。 |
|||
* 麻酔中は筋弛緩薬が投与されていることが多く、顔面筋の筋電図の混入が少ないことや、振幅が麻酔薬の影響で大きくなるなどにより比較的波形を読みやすい。 |
|||
導入に用いる薬剤の投与順序の一例 |
|||
=== 部位 === |
|||
前頭部から導出された[[脳波]]を利用することが多い。その理由としては、前頭部から導出された脳波は麻酔によって臨機応変に変化し、髪の毛がなく電極を配置しやすいことなどがあげられる。 |
|||
# 挿管中の無呼吸時間が長くなっても、血中酸素濃度に影響を与えないようにするために、肺を100%酸素で満たすために行う麻酔前の酸素吸入('''前酸素化'''と称する。'''脱窒素'''ともいう)。 |
|||
=== 脳波変化 === |
|||
# 挿管時の鎮痛のための[[レミフェンタニル]] |
|||
* 麻酔薬の種類によってその度具合が異なる。 |
|||
# 気管挿管のための鎮静剤としての[[プロポフォール]] |
|||
* 揮発性麻酔薬のセボフルランや[[イソフルラン]]、および静脈麻酔薬のプロポフォールなどによる脳波変化の度具合は類似している。これらは麻酔薬濃度を上昇させていくと、[[脳波]]の振幅は大きくなるとともに周波数は低くなる。つまり、ゆっくりした波が主体となる。さらに上昇させると、平坦な[[脳波]]と大きな振幅で速い波が交互に出現する特異的なパターン(burst and supression)となる。さらに上昇させると、平坦な脳波の部分が増加していき、やがて完全に平坦な脳波となる。 |
|||
# 開口や[[喉頭鏡]]操作を容易にするための[[筋弛緩剤|筋弛緩薬]]として、[[ロクロニウム]] |
|||
* 揮発性麻酔薬およびプロポフォール以外の麻酔薬としては、[[亜酸化窒素]]や[[ケタミン]]が挙げられる。亜酸化窒素は麻酔作用が弱いために単独で用いられることは少ないが、単独で用いると振幅が小さく通常のベータ波よりも周波数の速い波が見られる。さらに高い濃度では、振幅が大きく周波数も非常に遅いデルタ波なども出現する。 |
|||
# 挿管が完了したら、酸素から酸素と吸入麻酔薬の混合気体に変更する |
|||
* 現在、麻酔中のモニターとしで用いられている脳波モニターで麻酔薬の効果判定が可能なのは、前者のセボフルラン、[[イソフルラン]]、プロポフォールなどを用いた場合である。亜酸化窒素やケタミンを投与した麻酔の場合には効果判定が難しいため、慎重な判断が望まれる。 |
|||
[[喉頭鏡|喉頭展開]]と挿管は、どちらも非常に刺激が強いものである。上記の導入の過程では、これらの操作に対する血圧上昇などの反応を抑制すると同時に、挿管の間に意識がある、というような事が無いよう、昏睡に近い状態に誘導する。 |
|||
=== 脳波モニター === |
|||
# BISモニター(BIS: bispectral index):BIS値を見るモニター。BIS値は平坦な脳波の場合に0、もっとも覚醒している状態を100として表示する。一般的に、80以上の場合には「覚醒」、60から80の場合には「浅い鎮静」、40から60までの場合には「手術麻酔に適したレベル」、そして40未満は「深麻酔」とされている。 |
|||
# aepEXモニター(aep: auditory evoked potential):耳にイヤホンを通してクリック音を発生させ、頭部に数個の電極を貼付することによって検査し、麻酔深度を評価する機器。aepEXは、144msecまでのAEP波形を基本情報として算出した数値を表示する。AEPが完全に平坦な時に0、覚醒時には100に近い数値を示す。 |
|||
=== 導入方法 === |
|||
BIS値やAEP値は絶対値ではなく推定値であり、現時点での鎮静度の評価のひとつである。それゆえ、実際の鎮静度とは大小なりの乖離が認められることもある。その原因は以下の通り。 |
|||
[[ファイル:Physician anesthesiologists provide safe care in Afghanistan 141225-N-JY715-132.jpg|サムネイル|全身麻酔導入中の麻酔科医。下顎挙上による[[気道確保]]と[[麻酔マスク]]の患者の顔への密着を行っている。]] |
|||
以下の3種類の方法に大別される{{Efn|英語版からの訳者注。下記は日本語の麻酔科学成書における一般的な麻酔導入法の分類である、急速導入と緩徐導入について、英語版には明確な記載が無かったために英語翻訳版からの改稿時に、この記載を残している。吸入麻酔薬を用いれば緩徐導入、静脈麻酔薬を用いれば急速導入というのが少なくとも日本における一般的な麻酔導入法の区分であるが、投与速度を調節すれば、緩徐導入よりも時間のかかる急速導入も可能である。そういう意味で旧来のこの分類は不適切かも知れない。}}。 |
|||
==== |
==== 1. 急速導入(Rapid Induction) ==== |
||
:[[静脈麻酔薬]]を用いて入眠させる、最も頻用されている麻酔導入方法。 |
|||
* ノイズの混入:BISモニターは心臓からの電流を除去するフィルターを備えているが、しばしば起電力の大きい心筋電位の混入が問題となる。特に、新生児や心肥大患者で著明となる。また、筋弛緩薬を投与していないときは、筋電図の混入にも注意が必要である。 |
|||
* 年齢:新生児は、覚醒時から徐波が主体である。小児では振幅が大きく、基本周波数が高い傾向にあるため、BIS値は本来の鎮静度よりも高く表示される。 |
|||
* paradoxical arousal:麻酔深度が不十分なときに疼痛などの刺激が加わると巨大デルタ波が観察されるため、BIS値が低下する現象。 |
|||
* β activation:麻酔薬は浅い鎮静レベルではむしろ速波が増える(β activationする)ため、BIS値が覚醒時よりも高い傾向を認める。 |
|||
* 虚血、心停止、脳血流の低下では、脳波が徐波化する。鎮静レベルが一定にもかかわらずBIS値が急激な低下を認めた場合には、これらを疑う。 |
|||
==== 2. 緩徐導入(Slow Induction) ==== |
|||
== 覚醒・抜管 == |
|||
:吸入麻酔薬によりマスク換気で入眠させ、麻酔を深くしたあと、静脈路確保を行う麻酔導入方法。覚醒状態で[[末梢静脈カテーテル]]の確保が困難な小児などに用いる。 |
|||
麻酔薬を止め、意識が回復し、筋弛緩作用からの回復も十分で、一回換気量、呼吸回数、従命可能であるなどの条件を満たせば気管チューブを抜くことができる。これを抜管(ばっかん)という。ただし、この状態でも筋弛緩薬の効果はある程度残っているため、[[アセチルコリンエステラーゼ阻害剤|アセチルコリンエステラーゼ阻害薬]]である[[ネオスチグミン]]と、ムスカリン作用を抑制するための[[硫酸アトロピン]]を投与し、筋弛緩薬のリバース([[拮抗作用|拮抗]])を行う。リバースを行う場合、筋弛緩薬がある程度自然に消退していないと、再筋弛緩が発生するため危険である。抜管後、患者を観察し問題なければ帰室させる。 |
|||
==== 3. [[迅速導入]](Rapid sequence induction) ==== |
|||
=== 覚醒の準備 === |
|||
{{Main|迅速導入}} |
|||
麻酔覚醒により疼痛や[[低体温症|低体温]]などに対する血圧上昇、身震いなどによる体温調整を行う生理現象([[シバリング]])などの生体反応が顕在化してくる。覚醒させる前に、体温、疼痛管理、呼吸循環状態などが覚醒可能な状態に安定しているかどうかを評価する必要がある。全身麻酔中、体温の保持を積極的に努めないと次第に低下し続ける。それを防ぐために、手術終了に向けて通常の体温保持に加え、室温を上昇させ、さらなる体温上昇を目指す。 |
|||
:以前はCrash Inductionとも呼ばれた。緊急時の手術などで、胃内容物が多く([[フルストマック]])、[[誤嚥]]の危険性が高い状況で行われる導入方法で、十分な前酸素化のあと、静脈麻酔薬と筋弛緩薬を一度に投与し、マスク換気を行わずに気管挿管を行う方法。挿管前後に[[輪状軟骨圧迫|輪状軟骨を圧迫]]して食道を閉鎖して胃内容物の逆流を防ぐ。 |
|||
=== 生理学的モニタリング === |
|||
; 吸入麻酔 |
|||
[[生体情報モニタ|モニタリング機器]]により、全身麻酔の導入、維持、そして覚醒をコントロールすることができる。麻酔の基本的なモニタリングの基準は、{{仮リンク|アメリカ麻酔科学会|en|American Society of Anesthesiologists}}が発表したガイドラインで、麻酔中に患者の酸素化、換気、循環、体温を継続的に評価する必要があると記述されている<ref>{{Cite web |website=American Society of Anesthesiologists. |title=Standards for Basic Anesthetic Monitoring |quote=Approved by the ASA House of Delegates on October 21, 1986, last amended on October 20, 2010, and reaffirmed on December 13, 2020 |url=https://www.asahq.org/~/media/Sites/ASAHQ/Files/Public/Resources/standards-guidelines/standards-for-basic-anesthetic-monitoring.pdf |access-date=10 November 2022}}</ref>。 |
|||
: 吸入麻酔からの覚醒は、導入時の逆順序で、麻酔回路内の吸入麻酔薬供給量を0%にすることで、[[肺胞]]内の吸入麻酔薬分圧を血液中より低下させ、血液中、そして脳内から肺胞内への吸入麻酔薬排泄を促進する。脳内の吸入麻酔薬[[分圧]]が覚醒レベルに至れば自然に覚醒する。 |
|||
; 静脈麻酔 |
|||
: 全身麻酔維持に用いられる静脈麻酔薬は、おもにプロポフォールである。手術終了に合わせて、BIS値を参考にしながら投与量の加減を調節する。 |
|||
; 筋弛緩薬 |
|||
: かつては非脱分極性筋弛緩薬を麻酔科医の経験則に基づいて使用していた。覚醒時には、始発呼吸の出現を待って拮抗薬を使用する方法が一般的であった。しかしこの方法では、筋弛緩状態からの回復が不十分である可能性がある。神経刺激装置は、比較的安価で、それを用いて客観的に筋弛緩からの回復を確認して麻酔覚醒をはかることが望まれる。 |
|||
# '''連続心電図モニタ'''(ECGまたはEKG): [[電極]]を患者の皮膚に貼り付けて、心拍数と心拍リズムを監視する。これは、麻酔科医が[[虚血性心疾患|心臓の虚血]]の初期徴候を識別するのに役立つ場合がある。通常、不整脈はⅡ誘導、虚血はⅤ5誘導でモニターする。 |
|||
予想される濃度や時間を超えて意識や反応が回復しない状態を'''覚醒遅延'''という。 |
|||
# '''連続[[パルスオキシメーター|パルスオキシメトリー]]'''(SpO<sub>2</sub>): 患者の[[ヘモグロビン]][[酸素飽和度]]の低下([[低酸素症|低酸素血症]])を早期に発見するために、通常、指に装着する装置。 |
|||
# '''血圧モニタリング''': 患者の血圧を測定する方法は2つある。まず、最も一般的なのは、非侵襲的血圧(NIBP)モニタリングである。これは、患者の腕、前腕、または脚に[[血圧計]]を装着するものである。手術中は、あらかじめ設定された一定の間隔で、機械が血圧を測定する。2つ目の方法は、侵襲的血圧(IBP)モニタリングで、血圧の一拍ごとのモニタリングが可能である。この方法は、重症の心臓疾患や肺疾患のある患者、心臓手術や移植手術などの大きな手術を受ける患者、大量の出血が予想される患者に限られる。この方法では、通常、手首([[橈骨動脈]])または鼠径部([[大腿動脈]])の動脈に、特殊なプラスチック製のカニューレを挿入する。 |
|||
# '''薬剤濃度測定''':[[麻酔器]]には通常、吸入麻酔薬の使用割合や呼気濃度を測定するためのモニターがある。これらのモニターには、酸素、[[二酸化炭素]]、および[[吸入麻酔薬]]([[亜酸化窒素]]、[[セボフルラン]]など)の測定が含まれる。 |
|||
# '''酸素濃度計''': ほとんどすべての麻酔器の回路には、患者への酸素供給が損なわれた場合に備えてアラームが搭載されている。アラームは、吸入酸素の割合が設定された閾値を下回ると作動する。 |
|||
# '''回路外れアラーム'''(または'''低圧アラーム'''): [[機械換気 (医学)|機械換気]]中に麻酔器の回路内圧が、正常に陽圧換気が行われていれば到達するはずの圧力に達しないことを示す。 |
|||
# [[カプノグラフィ|'''カプノグラフィー''']]: 患者の呼気の[[二酸化炭素]]の量をパーセントまたはmmHgで表示し、麻酔科医が[[呼吸|換気]]の適切さを評価できるようにするものである。通常、麻酔科医はより繊細な変化を確認するためにmmHgを使用する。 |
|||
# '''体温測定''': [[低体温症|低体温]]や発熱の判別、[[悪性高熱症]]の早期発見のため |
|||
# '''[[バイスペクトラルインデックス|脳波]]、{{仮リンク|エントロピーモニター|en|entropy monitoring}}'''、その他の脳波測定システム: 麻酔の深さを確認するために用いられる。これにより、{{仮リンク|術中覚醒|en|anesthesia awareness}}や過剰投与の可能性を低減することができる。 |
|||
== |
=== 気道管理 === |
||
{{Main|気道確保}}麻酔中の患者は、麻酔薬、[[オピオイド]]、[[筋弛緩剤]]の影響により、気道保護反射(咳など)、[[気道確保|気道開存性]]、時には規則的な呼吸パターンが消失する。気道を確保し、呼吸を調節するために、患者が意識を失った後に何らかの[[気管チューブ|呼吸チューブ]]が挿入される。機械換気を可能にするために、気管チューブがしばしば使用されるが、フェイスマスクや[[ラリンジアルマスク]]など、呼吸を補助できる別の器具も存在する。一般に、完全な機械的換気は、侵襲度の高い処置のために非常に深い全身麻酔状態を引き起こす場合、および/または重症患者や負傷した患者に対してのみ使用される。とはいえ、全身麻酔を導入すると、通常は[[無呼吸]]になり、薬物が切れて自発呼吸が始まるまで換気が必要となる。つまり、全身麻酔の導入と維持の両方に換気が必要な場合と、導入時だけに換気が必要な場合がある。しかし、人工呼吸器による[[機械換気 (医学)|機械換気]]は、自発呼吸の間、十分なガス交換を確保するための換気補助を行うこともできる。 |
|||
; 喉頭痙攣 |
|||
: [[喉頭]]筋の収縮により[[声帯]]の閉塞が起こる生理現象である。全身麻酔の導入時や覚醒時起こりやすいと言われている。原因としては分泌物、異物、[[エーテル (化学)|エーテル]]やデスフルランといった[[吸入麻酔薬]]による気道刺激、低酸素状態、[[咽頭]]部の操作、バルビツール酸系の薬物などが考えられている。上気道の閉塞であるため吸気時に笛声音やシーソー呼吸が観察される。治療は酸素投与である。大抵は30秒ほどで軽快するが、改善傾向を認めない場合は[[筋弛緩薬]]の投与を行う。筋弛緩薬としては作用発現が早い[[スキサメトニウム]]がよいといわれている。 |
|||
全身麻酔は、患者が自発的に呼吸している状態でも行うことができ、その結果、患者自身の酸素濃度を維持することができる。よって、自発呼吸維持は特殊な状況(例:気道確保困難、非挿管下手術)において有益となることがある。自発呼吸は従来、吸入剤(ハロタンやセボフルランなど)で維持されてきたが、これは緩徐導入と呼ばれる。また、静脈麻酔(例:プロポフォール)を使用して自発呼吸を維持することも可能である。自発呼吸を維持するための静脈麻酔は、吸入麻酔薬に比べて一定の利点(喉頭反射の抑制など)があるが、慎重に[[滴定投与|滴定]]する必要がある。静脈麻酔と高流量鼻腔酸素を用いた自発呼吸(STRIVE Hi<sup>TM</sup>)は、困難気道で閉塞している場合に使用されてきた技術である<ref>{{Cite journal|date=March 2017|title=SponTaneous Respiration using IntraVEnous anaesthesia and Hi-flow nasal oxygen (STRIVE Hi) maintains oxygenation and airway patency during management of the obstructed airway: an observational study|journal=British Journal of Anaesthesia|volume=118|issue=3|pages=444–451|DOI=10.1093/bja/aew468|PMID=28203745|PMC=5409133}}</ref>。 |
|||
; 気管支痙攣 |
|||
: 術中の[[気管支喘息]]のことである。気管支喘息の素因のある患者に[[クラーレ]]や[[フェンタニル]]、[[プロプラノロール]]といったβ遮断薬、[[スキサメトニウム]]など気管支攣縮作用を持つ薬物を投与すると起こるといわれている。術中はリザーバーバックが急に硬くなること、酸素飽和度が低下することによって疑う。治療としては[[セボフルラン]]、[[イソフルラン]]といった気管支拡張作用のある[[吸入麻酔薬]]を深くしたり、[[エフェドリン]]の投与、また気管支喘息の発作に基づいた治療を行う。気管チューブが刺激となって起こることもあるため、チューブの位置を変えてみることも重要である。 |
|||
=== 眼球保護 === |
|||
; [[悪性高熱症]] |
|||
全身麻酔は[[眼輪筋]]の緊張性収縮を低下させ、59%の人に[[兎眼]](不完全な閉眼)を引き起こす<ref name="contractor">{{Cite journal|year=2006|title=Injury during anaesthesia|journal=Continuing Education in Anaesthesia, Critical Care & Pain|volume=6|issue=2|pages=67–70|DOI=10.1093/bjaceaccp/mkl004}}</ref>。さらに、涙の産生と涙液膜の安定性が低下し、角膜上皮の乾燥が起こり、[[リソソーム|リソゾーム]]による保護が低下する。また、[[ベル現象]](睡眠中に眼球が上を向き、角膜を保護する現象)による保護も失われてしまう。{{仮リンク|全身麻酔中の眼球損傷|en|Eye injuries during general anaesthesia}}の可能性を減らすために、慎重な管理が必要である<ref name="nair">{{Cite journal|year=2014|title=Care of the eye during anaesthesia and intensive care|journal=Anaesthesia & Intensive Care Medicine|volume=15|pages=40–43|DOI=10.1016/j.mpaic.2013.11.008}}</ref>。全身麻酔中の眼の損傷を防ぐ方法としては、瞼をテープで閉じる、眼軟膏を使用する、特殊なデザインの眼球保護ゴーグルを使用する、などがある。 |
|||
: スキサメトニウムや[[ハロタン]]を用いると発症しやすいといわれているが、平成19年(2007年)現在、これらの麻酔薬を用いることは非常に少ないものの発生している。セボフルランといった新しい吸入麻酔薬でも起こると考えられている。初発は頻脈や不整脈であることが多く、約15分で0.5度程度に体温が上昇する。筋強直が起こるとポートワイン尿(ミオグロビン尿を伴う腎不全)が起こる。危険因子としては、家族内発生、血中CK値高値、[[筋ジストロフィー]]といった筋疾患や側弯症といった骨格疾患があげられる。こういった危険因子がある場合は麻酔計画を考え、予防することが重要である。治療には[[ダントロレン|ダントロレンナトリウム]]を用いる。ダントロレンナトリウムによる治療が行われる以前は死亡率80%を超えていたが、治療法確立以後は20%程度に抑えられている。 |
|||
=== 神経筋遮断 === |
|||
; 嚥下性肺炎 |
|||
[[ファイル:Anesthesia_medications.JPG|サムネイル|全身麻酔下の手術で使用予定の薬剤が調製された[[注射器]]: [[プロポフォール]]([[鎮静薬]])- [[エフェドリン]]([[昇圧剤|昇圧薬]])- [[フェンタニル]]([[鎮痛剤|鎮痛薬]])- [[アトラクリウム]]([[神経筋遮断薬]])- 臭化[[グリコピロニウム]](商品名:ロビノール、分泌物減少)]] |
|||
: [[メンデルソン症候群]]ともいう。フルストマックの患者や肥満症、妊婦、[[イレウス]]、幽門狭窄症、食道裂孔ヘルニアの患者で多いといわれている。胃の内容物で起こった場合は、化学性肺炎となり重篤となる。喘息様症状、チアノーゼ、頻脈を起こし最終的に[[肺水腫]]にいたる。予防するために手術前には絶飲食となるが、妊婦の場合は胎児に対する栄養不足の可能性もあってその予防が難しい。 |
|||
[[神経筋遮断薬]]による麻痺、すなわち一時的な筋弛緩は、現代の麻酔に不可欠な要素である。この目的で最初に使用された薬剤は1940年代に導入された[[クラーレ]]であったが、現在では副作用が少なく、一般に作用時間の短い薬剤に取って代わられている。筋弛緩によって、腹部や胸部などの主要な[[体腔]]内の手術を、深い麻酔(循環器系などへの悪影響が強い)を必要とせずに行うことが可能となり、また気管挿管も容易となる。 |
|||
[[アセチルコリン]]は、{{仮リンク|神経筋接合部|en|neuromuscular junction}}に存在する天然の[[神経伝達物質]]で、神経末端から放出されると筋肉を収縮させる作用がある。筋弛緩剤は、アセチルコリンが受容体に結合するのを阻害することによって作用する。呼吸筋([[横隔膜]]と胸の{{仮リンク|肋間筋|en|Intercostal muscle}})が麻痺すると、何らかの人工呼吸が必要となる。喉頭筋も麻痺しているため、通常、気管チューブを用いて気道を確保する必要がある<ref name=":114">{{Cite book |title=Miller's anesthesia |date=2020 |publisher=Elsevier |editor=Michael A. Gropper |isbn=978-0-323-61264-7 |edition=Ninth |location=Philadelphia, PA |oclc=1124935549}}</ref>。 |
|||
; [[しゃっくり]] |
|||
: しゃっくりとは、おもに横隔膜への機械的な刺激などによって迷走神経が亢進状態になったときに起こるといわれている。迷走神経関与の[[不随意運動]]、[[ミオクローヌス]]であると考えられている。術中は麻酔を深くしたり、[[筋弛緩薬]]を投与したり、横隔膜刺激の原因の除去などを行う。術後は[[消化管機能調節薬]]なども効果的である。 |
|||
運動麻痺を最も簡単にモニターできるのは、[[筋弛緩モニタ]]である。この装置は、末梢神経の皮膚から短い電気パルスを断続的に送りながら、その神経に供給されている筋肉の収縮を観察するものある。筋弛緩剤の効果は、手術終了時に{{仮リンク|コリンエステラーゼ阻害薬|en|Cholinesterase inhibitor}}によって元に戻されることが多く、副作用を最小限に抑えるためにムスカリン系[[抗コリン薬]]と併用投与される。現在使用されている骨格筋弛緩薬の例としては、[[パンクロニウム]]、[[ロクロニウム]]、[[ベクロニウム]]、[[シスアトラクリウム]]、[[アトラクリウム]]、[[ミバクリウム]]、[[スキサメトニウム|サクシニルコリン]]がある。[[スガマデクス]]のような新しい[[選択的筋弛緩薬結合薬|神経筋遮断回復剤]]も使用できる;これは筋弛緩薬と直接結合して神経筋接合部からそれを取り除くことで効果を発揮する。スガマデクスは2015年に米国で使用が承認され、急速に普及が進んだ。2022年の研究では、スガマデクスと[[ネオスチグミン]](頻用されている[[アセチルコリンエステラーゼ阻害剤]])は、神経筋遮断から回復作用において同様に安全である可能性が高いことが示されている<ref>{{Cite journal|date=May 2022|title=Sugammadex Versus Neostigmine for Reversal of Residual Neuromuscular Blocks After Surgery: A Retrospective Cohort Analysis of Postoperative Side Effects|journal=Anesthesia and Analgesia|volume=134|issue=5|pages=1043–1053|DOI=10.1213/ANE.0000000000005842|PMID=35020636|postscript=6}}</ref>。 |
|||
; バッキング |
|||
:[[気管挿管]]中の[[咳]]であり、気道反射の亢進によって起こる。多くの場合は浅麻酔が原因となるが、気管チューブによる刺激が原因となる場合もある。麻酔薬(効果の早い[[静脈麻酔薬]]や[[筋弛緩薬]])の追加、気管チューブの位置を微調整する行為が直接の治療(解決策)となる。 |
|||
== 麻酔の維持 == |
|||
; 高血圧 |
|||
静脈内導入剤の作用時間は一般に5~10分で、その後、自然に意識が回復する<ref>{{Cite journal|date=June 2014|title=Pharmacology of anaesthetic agents I: intravenous anaesthetic agents|url=https://www.sciencedirect.com/science/article/pii/S1743181617300975|journal=Continuing Education in Anaesthesia Critical Care & Pain|volume=14|issue=3|pages=100–105|language=en|DOI=10.1093/bjaceaccp/mkt039|ISSN=1743-1816}}</ref>。手術の間、無意識状態を持続させるためには、麻酔を'''維持'''する必要がある。そのためには、酸素と[[吸入麻酔薬|揮発性麻酔薬]]の混合ガスを注意深くコントロールして患者に吸入させるか、静脈内投与を行う(通常は[[プロポフォール]])。吸入麻酔薬は、[[オピオイド]](通常は[[フェンタニル]]またはフェンタニル誘導体)系の静脈内鎮痛剤や[[鎮静薬|鎮静剤]](通常は[[プロポフォール]]または[[ミダゾラム]])などによってよく補完される。プロポフォールは[[全静脈麻酔]](TIVA)に使用できるため、吸入薬による補完は必要ない<ref>{{Cite journal|date=February 2019|title=Guidelines for the safe practice of total intravenous anaesthesia (TIVA): Joint Guidelines from the Association of Anaesthetists and the Society for Intravenous Anaesthesia|journal=Anaesthesia|volume=74|issue=2|pages=211–224|DOI=10.1111/anae.14428|PMID=30378102|postscript=6}}</ref>。2023年現在、日本で麻酔維持に保険適応があるのは[[プロポフォール]]と[[レミマゾラム]]である。全身麻酔は通常安全であると考えられているが、局所麻酔薬による味覚および/または嗅覚の変調、全身麻酔の副作用として脳卒中、神経損傷を生じた患者の報告例がある<ref>{{Cite journal|date=December 2017|title=Loss of Smell and Taste After General Anesthesia: A Case Report|journal=A&A Case Reports|volume=9|issue=12|pages=346–348|DOI=10.1213/XAA.0000000000000612|PMID=28767470}}</ref>。 |
|||
: 高血圧に関して、二酸化炭素の蓄積、軽度の低酸素血症や浅麻酔が原因と考えられている。痛みの度合いによって必要な麻酔深度は異なるため、浅麻酔による高血圧を疑ったらオピオイドをはじめとする鎮痛薬を投与する場合が多い。 |
|||
手術が終わると、麻酔薬の投与は中止される。脳内の麻酔薬の濃度が一定以下になると、意識が回復する(手術時間にもよるが、通常1~30分以内に回復する)<ref name=":115">{{Cite book |title=Miller's anesthesia |date=2020 |publisher=Elsevier |editor=Michael A. Gropper |isbn=978-0-323-61264-7 |edition=Ninth |location=Philadelphia, PA |oclc=1124935549}}</ref>。 |
|||
; 低血圧 |
|||
: [[体位]]変換による影響や麻酔薬の過剰投与で起こることが多い。ほかにも換気不全、心大血管操作、神経反射、異型[[輸血]]、アナフィラキシーショックなども考えられる。出血の場合は頻脈が先行することが多い。治療は原因除去が一番重要である。 |
|||
1990年代、スコットランドの[[グラスゴー]]で、麻酔を維持する新しい方法が開発された。[[標的制御注入]] (TCI)と呼ばれるこの方法は、コンピュータ制御の[[シリンジポンプ]]を用いて、手術中持続的にプロポフォールを注入し、[[吸入麻酔薬|揮発性麻酔薬]]を必要とせず、薬理学の理論により望ましい薬剤濃度を設定して、投与量をより正確に指定することができるものである。利点としては、麻酔からの回復が早い、[[術後嘔気嘔吐|術後の悪心・嘔吐]]の発生が少ない、[[悪性高熱症]]の誘因がない、などが挙げられる。現在、米国ではTCIは認められていないが、代わりに一定量の薬剤を供給するシリンジポンプが一般的に使用されている<ref>{{Cite journal|last=Absalom|first=Anthony R.|last2=Glen|first2=John Iain B.|last3=Zwart|first3=Gerrit J. C.|last4=Schnider|first4=Thomas W.|last5=Struys|first5=Michel M. R. F.|date=January 2016|title=Target-Controlled Infusion: A Mature Technology|url=https://pubmed.ncbi.nlm.nih.gov/26516798|journal=Anesthesia and Analgesia|volume=122|issue=1|pages=70–78|DOI=10.1213/ANE.0000000000001009|ISSN=1526-7598|PMID=26516798}}</ref>。日本では[[プロポフォール]]のTCIのみ、認められている。 |
|||
; 不整脈 |
|||
: 不適切な換気、不適切な麻酔深度など、さまざまな原因で不整脈が生じる。完全房室ブロックや[[心室頻拍]]、心室性不整脈は致命的な[[不整脈]]である[[心室細動]]に移行することが多く危険である。 |
|||
副作用の治療や合併症の予防のために、他の薬剤が使用されることもある。高血圧の治療には[[高血圧治療薬|降圧剤]]、低血圧の治療には[[エフェドリン]]や[[フェニレフリン]]、[[気管支喘息|喘息]]や{{仮リンク|喉頭痙攣|en|laryngospasm}}、[[気管支痙攣]]の治療には[[サルブタモール]]、アレルギー反応の治療には[[アドレナリン|エピネフリン]]や[[ジフェンヒドラミン]]などが使用される。炎症と感染を防ぐために、[[糖質コルチコイド|グルココルチコイド]]と[[抗生物質]]がそれぞれ投与されることもある<ref name=":115" />。 |
|||
== 全身麻酔でよく使われる薬物 == |
|||
ここでは全身麻酔でよく使われる薬を述べていく。 |
|||
== 覚醒・抜管 == |
|||
麻酔における'''覚醒''' ({{Lang-en-short|emergence}})とは、全身麻酔の終了後、すべての器官系が元の生理的機能に戻ることである。この段階では、{{仮リンク|覚醒時せん妄|en|Emergence delirium}}(急性精神錯乱)、[[失語症|失語]](会話の発声または理解の障害)、感覚または運動機能の[[巣症状]]などの一時的な神経学的症状を伴うことがある。血圧の上昇や低下、[[頻脈]]、その他の[[不整脈|心不整脈]]などの心血管系イベントも、[[呼吸困難]]などの呼吸器系症状と同様に、全身麻酔からの覚醒時に起こりやすい。 |
|||
==== 吸入麻酔薬 ==== |
|||
;[[亜酸化窒素]](笑気) |
|||
: 強力な鎮痛作用を持つが、[[最小肺胞内濃度]]が高いため単独で全身麻酔をするのは困難である。以下の吸入麻酔薬と併用して用いられる。しかし現在では全静脈麻酔(TIVA)の普及や、オピオイド主体のバランス麻酔が普及していること、また、術後の嘔気嘔吐の頻度が高まったり、笑気自体が[[温室効果]]の原因となるなど、次第に敬遠される方向にある。若手麻酔科医は吸入麻酔を用いる際も笑気をまったく用いない者も多く、次第に使用量は減少している。 |
|||
; [[イソフルラン]](フォーレン) |
|||
: 強烈なエーテル臭と気道の刺激性から、緩徐導入は困難であるが、生体内代謝率の低さから、肝・腎機能の低下した患者の麻酔などで好んで用いられた。調節性がセボフルランやデスフルランに劣るため、近年はあまり用いられない。 |
|||
;セボフルラン(セボフレン) |
|||
: 血液ガス分配係数の小ささと臭いが穏やかなことから緩徐導入に向く。ほぼどんな用途でも用いることができ、現在もっとも頻用されている[[吸入麻酔薬]]である。低流量麻酔下(総流量2リットル以下)では、旧タイプの二酸化炭素吸収剤との接触により発生するCompound Aが腎機能障害を起こすとされたこともあるが、現在ではほとんど問題とされることはない。 |
|||
麻酔薬を止め、意識が回復し、筋弛緩作用からの回復も十分で、[[一回換気量]]、呼吸回数、指示に従う、などの条件を満たせば気管チューブを抜くことができる。これを'''抜管'''(ばっかん)という。言葉による指示に反応し、従うことは、患者の抜管準備の評価によく利用される基準である{{Efn|麻酔科の代表的な教科書であるMiller麻酔科学への全体参照となっているが、該当記載を見つけられず。記載内容は専門的に正しいことは疑いがない。}}<ref name=":116">{{Cite book |title=Miller's anesthesia |date=2020 |publisher=Elsevier |editor=Michael A. Gropper |isbn=978-0-323-61264-7 |edition=Ninth |location=Philadelphia, PA |oclc=1124935549}}</ref>。ただし、この状態でも筋弛緩薬の効果はある程度残っているため、[[アセチルコリンエステラーゼ阻害剤|アセチルコリンエステラーゼ阻害薬]]である[[ネオスチグミン]]と、ムスカリン作用を抑制するための[[硫酸アトロピン]]を投与し、筋弛緩薬のリバース([[拮抗作用|拮抗]])を行う。リバースを行う場合、筋弛緩薬がある程度自然に消退していないと、再筋弛緩が発生するため危険である。近年では[[選択的筋弛緩薬結合薬]]である[[スガマデクス]]が用いられる事が多い。抜管後、患者を観察し問題なければ手術室から術後回復室又は病棟に帰室させる。 |
|||
'''デスフルラン(スープレン)''' |
|||
予想される濃度や時間を超えて意識や反応が回復しない状態は覚醒遅延という。 |
|||
: セボフルランよりもさらに調節性にすぐれた吸入麻酔薬であり、日本においてセボフルランと市場シェアを二分している。気道刺激性があり、緩徐導入には適さない。 |
|||
== 術後管理 == |
|||
<br /> |
|||
[[ファイル:Anesthesia_recovery_modified.jpg|サムネイル|麻酔後回復室の患者]] |
|||
==== 静脈麻酔薬 ==== |
|||
術後の痛みは、{{仮リンク|麻酔後回復室|en|Post-anesthesia care unit}}(PACU)で[[区域麻酔]]や非経口薬で管理される。患者は[[オピオイド]]のほか、[[非ステロイド性抗炎症薬]]や[[アセトアミノフェン]]などの薬剤を投与されることもある<ref name=":3">{{Cite journal|date=April 2018|title=Postanaesthetic shivering - from pathophysiology to prevention|journal=Romanian Journal of Anaesthesia and Intensive Care|volume=25|issue=1|pages=73–81|language=en-GB|DOI=10.21454/rjaic.7518.251.xum|PMID=29756066|PMC=5931188}}</ref>。また、[[患者管理鎮痛法|患者管理鎮痛]] (PCA)と呼ばれるシステムを用いて、患者自身がオピオイドを投与することもある<ref>{{Cite journal|date=April 2010|title=Comparison of perioperative oral multimodal analgesia versus IV PCA for spine surgery|journal=Journal of Spinal Disorders & Techniques|volume=23|issue=2|pages=139–145|DOI=10.1097/BSD.0b013e3181cf07ee|PMID=20375829|postscript=6}}</ref>。患者がPCAのボタンを押すと、注射器が作動し、通常[[モルヒネ]]、[[フェンタニル]]、[[オキシコドン]]などの[[強オピオイド]](例:フェンタニル10µg)の初期設定量の「[[ボーラス投与|ボーラス]]量」を投与される。PCA装置はその後、薬物が効果を発揮し、また患者が過剰摂取するのを防ぐために、あらかじめ設定された期間「ロックアウト」すなわちボタン操作不能となる。患者が眠くなりすぎたり、鎮静状態になると、それ以上鎮痛剤を要求しなくなる。このように、持続注入法にはない[[フェイルセーフ]]の側面がある。これらの薬物療法で効果的に痛みを抑えることができない場合は、[[神経ブロック]]と呼ばれる方法で神経に直接局所麻酔薬を注入することがある<ref>{{Cite journal|date=October 2019|title=Adductor canal blocks for postoperative pain treatment in adults undergoing knee surgery|journal=The Cochrane Database of Systematic Reviews|volume=2019|issue=10|DOI=10.1002/14651858.CD012262.pub2|PMID=31684698|PMC=6814953}}</ref><ref>{{Cite journal|date=October 2019|title=The Effect of Transversus Abdominis Plane Block for Analgesia in Patients Undergoing Liver Transplantation: A Systematic Review and Meta-Analysis|journal=Turkish Journal of Anaesthesiology and Reanimation|volume=47|issue=5|pages=359–366|DOI=10.5152/tjar.2019.60251|PMID=31572985|PMC=6756312}}</ref>。 |
|||
;[[チオペンタール]](ラボナール)/チアミラール(イソゾール) |
|||
: バルビツール系[[静脈麻酔薬]]。アメリカでは2009年に生産中止<ref name="Guardian2011">{{cite news |author=Ed Pilkington |title=Europe moves to block trade in medical drugs used in US executions |url=https://www.theguardian.com/world/2011/dec/20/death-penalty-drugs-european-commission |date=20 December 2011 |newspaper=[[ガーディアン|Guardian]] |accessdate=2016-6-9}}</ref>。小児にも成人にも使用可能である。重度の喘息には禁忌と[[添付文書]]に記載されている。 |
|||
;プロポフォール(ディプリバン、プロポフォールマルイシ) |
|||
: 肝臓での代謝が早く、麻酔の導入にも維持にも好んで用いられるもっとも主流の全身麻酔薬である。疼痛効果がなく、フェンタニルなどの[[麻薬]]鎮痛薬や硬膜外麻酔などの局所麻酔と併用する。小児に対する麻酔目的での使用は禁忌ではないが、避けられる傾向にある。これは集中治療分野で、長期間鎮静のために投与された患者にPropofol Infusion Syndromeという重篤な病態が発生した報告があるためである。 |
|||
;[[ミダゾラム]](ドルミカム) |
|||
: 短時間作用性のベンゾジアゼピン。循環抑制が軽く、重症患者の麻酔導入や、麻酔前投薬にも用いられる。 |
|||
;ケタミン(ケタラール) |
|||
: 解離性麻酔薬と呼ばれる。視床、大脳新皮質は抑制するが、大脳辺縁系を賦活する。血圧上昇、頻脈などを起こす。そのため、呼吸抑制による死亡は生じない。体性痛を非常によく抑え、熱傷の疼痛除去でも好んで用いられる。近年、日本では麻薬に指定され、法的な取り締まり対象となったが、薬理学的には麻薬(オピオイド)ではない。 |
|||
回復室では、酸素飽和度<ref name=":0">{{Cite journal|date=October 2018|title=Towards an automated multimodal clinical decision support system at the post anesthesia care unit|journal=Computers in Biology and Medicine|volume=101|pages=15–21|DOI=10.1016/j.compbiomed.2018.07.018|PMID=30092398}}</ref><ref name=":8">{{Cite journal|date=August 2018|title=Perioperative hyperoxia and post-operative cardiac complications in adults undergoing non-cardiac surgery: Systematic review protocol|journal=Acta Anaesthesiologica Scandinavica|volume=62|issue=7|pages=1014–1019|DOI=10.1111/aas.13123|PMID=29664117}}</ref>、心拍、呼吸<ref name=":0" /><ref name=":9">{{Cite journal|date=October 2019|title=Perioperative noninvasive cardiac output monitoring in parturients undergoing cesarean delivery with spinal anesthesia and prophylactic phenylephrine drip: a prospective observational cohort study|journal=The Journal of Maternal-Fetal & Neonatal Medicine|volume=32|issue=19|pages=3153–3159|DOI=10.1080/14767058.2018.1458835|PMID=29683007|postscript=6}}</ref>、[[血圧]]<ref name=":0" />、{{仮リンク|中枢温|en|core body temperature}}など、多くの[[バイタルサイン]]をモニターする。 |
|||
=== 麻薬 === |
|||
* [[レミフェンタニル]](アルチバ) |
|||
* [[フェンタニル]](フェンタニル) |
|||
* [[モルヒネ]](塩酸モルヒネ) |
|||
: 拮抗薬に[[ナロキソン]]がある。 |
|||
{{仮リンク|術後シバリング|en|Postanesthetic shivering}}はよく見られる。提唱されている機序は、脊髄が脳よりも速い速度で回復するという観察に基づいている。この結果、間代性活動(震え)として表れる脊髄反射が抑制されなくなる。この理論は、中枢神経刺激剤である[[ドキサプラム]]が術後のシバリングを消失させるのに幾分有効であるという事実からも支持される<ref>Basics of Anesthesia, 5th Edition Authors: Robert K. Stoelting & Ronald D. Miller {{ISBN2|978-0-443-06801-0}}</ref>。シバリングは、不快感や痛みの悪化のほか、酸素消費量の増加、[[カテコールアミン]]の放出、低体温のリスク、乳酸アシドーシスを誘発することが分かっている<ref>{{Cite journal|last=Lopez|first=Maria Bermudez|date=April 2018|title=Postanaesthetic shivering – from pathophysiology to prevention|journal=Romanian Journal of Anaesthesia and Intensive Care|volume=25|issue=1|pages=73–81|DOI=10.21454/rjaic.7518.251.xum|ISSN=2392-7518|PMID=29756066|PMC=5931188}}</ref>。シバリングを軽減するために、暖かい毛布<ref name=":4">{{Cite journal|date=May 2017|title=Effectiveness of active and passive warming for the prevention of inadvertent hypothermia in patients receiving neuraxial anesthesia: A systematic review and meta-analysis of randomized controlled trials|journal=Journal of Clinical Anesthesia|volume=38|pages=93–104|DOI=10.1016/j.jclinane.2017.01.005|PMID=28372696|PMC=5381733}}</ref><ref name=":5">{{Cite journal|date=June 2014|title=Thermal insulation for preventing inadvertent perioperative hypothermia|journal=The Cochrane Database of Systematic Reviews|issue=6|pages=CD009908|DOI=10.1002/14651858.CD009908.pub2|PMID=24895945}}</ref>や、{{仮リンク|ベアハガー|en|Bair Hugger|label=温風加温装置}}と呼ばれる暖められた空気を循環させるシートで患者を包むなど、様々な手法が用いられる<ref name=":6">{{Cite journal|date=August 2009|title=Predicting the efficacy of convection warming in anaesthetized children|journal=British Journal of Anaesthesia|volume=103|issue=2|pages=275–282|DOI=10.1093/bja/aep160|PMID=19541677}}</ref><ref name=":7">{{Cite journal|date=June 2008|title=Comparison of two convective warming systems during major abdominal and orthopedic surgery|journal=Canadian Journal of Anaesthesia|volume=55|issue=6|pages=358–363|DOI=10.1007/BF03021491|PMID=18566199}}</ref>。外部加温装置でシバリングを軽減できない場合は、[[デクスメデトミジン]]などの薬剤<ref name=":1">{{Cite journal|date=22 August 2017|title=Dexmedetomidine as a neuraxial adjuvant for prevention of perioperative shivering: Meta-analysis of randomized controlled trials|journal=PLOS ONE|volume=12|issue=8|pages=e0183154|bibcode=2017PLoSO..1283154Z|DOI=10.1371/journal.pone.0183154|PMID=28829798|PMC=5567500}}</ref><ref name=":2">{{Cite journal|date=April 2017|title=Efficacy and Safety of Dexmedetomidine as an Adjuvant in Epidural Analgesia and Anesthesia: A Systematic Review and Meta-analysis of Randomized Controlled Trials|journal=Clinical Drug Investigation|volume=37|issue=4|pages=343–354|DOI=10.1007/s40261-016-0477-9|PMID=27812971}}</ref>、またはその他のα2-アゴニスト、抗コリン剤、中枢神経刺激剤、または副腎皮質ステロイドを用いてもよい<ref name=":3" /><ref name="English2002">{{Cite journal|last=English W|year=2002|title=Post-operative shivering, causes, prevention and treatment (letter)|url=https://resources.wfsahq.org/wp-content/uploads/uia-15-LETTER-TO-THE-EDITOR.pdf|journal=Update in Anaesthesia|issue=15|accessdate=2023-01-21}}</ref>。 |
|||
=== 神経遮断薬 === |
|||
;[[ドロペリドール]](ドロレプタン) |
|||
: フェンタニルと併用される[[神経遮断薬]]である。NLA([[神経遮断麻酔]])に用いられる。近年では[[制吐薬]]として用いられることが多い。 |
|||
多くの症例において、腹部以外の手術すら、周術期に用いるオピオイドが術後[[イレウス]]の一因となり得る。{{仮リンク|アルビモパン|en|alvimopan}}などの{{仮リンク|μオピオイド受容体|en|Μ-opioid receptor|label=μオピオイド}}[[アンタゴニスト|拮抗薬]]を術後すぐに投与すれば、退院時期を早めることができるが、麻痺性イレウスの発症を抑えることはできない<ref>{{Cite journal|date=May 2021|title=Postoperative ileus-An ongoing conundrum|journal=Neurogastroenterology and Motility|volume=33|issue=5|pages=e14046|DOI=10.1111/nmo.14046|PMID=33252179|postscript=6}}</ref>。 |
|||
=== 筋弛緩薬 === |
|||
;[[ベクロニウム]](マスキュラックス) |
|||
: 非脱分極性[[筋弛緩薬]]である。拮抗薬に[[ネオスチグミン]](ワゴスチクミン)がある。 |
|||
;[[パンクロニウム]] |
|||
: 非脱分極性筋弛緩薬である。[[ベクロニウム]]と比較して作用時間が長い。 |
|||
;[[スキサメトニウム]] |
|||
: 脱分極性筋弛緩薬である。 |
|||
;[[ロクロニウム]](エスラックス) |
|||
: 非脱分極性筋弛緩薬である。作用はベクロニウムに類似するが、作用発現までの時間が短い(1、2分)。スガマデックス(ブリディオン)で拮抗されるが、ネオスチグミンでも拮抗される。 |
|||
'''Enhanced Recover After Surgery''' ('''ERAS'''、イーラス) は、ケアの継続性を確保し、回復と周術期ケアを改善するための最新のガイドラインとコンセンサスを提供する学会である。パスウェイとガイドラインの遵守は、術後の転帰の改善と医療システムのコスト削減につながることが示されている。 |
|||
=== 循環器官用薬 === |
|||
[[昇圧薬]]、[[降圧薬]](カルシウム拮抗薬)、[[血管拡張薬]]、[[抗不整脈薬]]がある。 |
|||
== 周術期死亡 == |
|||
{{Main|en:Perioperative mortality}}{{仮リンク|周術期死亡|en|perioperative mortality}}のほとんどは、[[出血]]、[[敗血症]]、重要臓器の機能不全など、手術による[[合併症]]に起因する。過去数十年の間に、投与された麻酔薬の麻酔関連死亡率全体は大幅に改善された。監視装置、麻酔薬の進歩、周術期の安全性に対する関心の高まりなどが、周術期死亡率低下の理由である。米国では、現在推定される麻酔関連死亡率は、人口100万人あたり年間約1.1人である。死亡率が最も高いのは、老年人口、特に85歳以上の高齢者であった<ref>{{Cite journal|last=Li|first=Guohua|last2=Warner|first2=Margaret|last3=Lang|first3=Barbara H.|last4=Huang|first4=Lin|last5=Sun|first5=Lena S.|date=April 2009|title=Epidemiology of Anesthesia-related Mortality in the United States, 1999–2005|journal=Anesthesiology|volume=110|issue=4|pages=759–765|DOI=10.1097/aln.0b013e31819b5bdc|ISSN=0003-3022|PMID=19322941|PMC=2697561}}</ref>。2018年のレビューでは、周術期の麻酔介入と麻酔関連死亡率への影響について検討された。死亡率を低下させることが判明した介入は、薬物療法、換気、輸血、栄養、血糖コントロール、透析、医療機器などである<ref>{{Cite journal|last=Boet|first=Sylvain|last2=Etherington|first2=Cole|last3=Nicola|first3=David|last4=Beck|first4=Andrew|last5=Bragg|first5=Susan|last6=Carrigan|first6=Ian D.|last7=Larrigan|first7=Sarah|last8=Mendonca|first8=Cassandra T.|last9=Miao|first9=Isaac|date=2018-11-30|title=Anesthesia interventions that alter perioperative mortality: a scoping review|journal=Systematic Reviews|volume=7|issue=1|pages=218|DOI=10.1186/s13643-018-0863-x|ISSN=2046-4053|PMID=30497505|PMC=6267894}}</ref>。医師から別の医師への引継ぎと、患者の死亡率との関連には従来から議論があったが、2022年の無作為化比較試験では、引き継ぎ群と対照群と比較して死亡率に有意差がないことが示された<ref>{{Cite journal|last=Meersch|first=Melanie|last2=Weiss|first2=Raphael|last3=Küllmar|first3=Mira|last4=Bergmann|first4=Lars|last5=Thompson|first5=Astrid|last6=Griep|first6=Leonore|last7=Kusmierz|first7=Desiree|last8=Buchholz|first8=Annika|last9=Wolf|first9=Alexander|date=2022-06-28|title=Effect of Intraoperative Handovers of Anesthesia Care on Mortality, Readmission, or Postoperative Complications Among Adults: The HandiCAP Randomized Clinical Trial|journal=JAMA|volume=327|issue=24|pages=2403–2412|DOI=10.1001/jama.2022.9451|ISSN=1538-3598|PMID=35665794|PMC=9167439}}</ref>。 |
|||
* [[エフェドリン]](エフェドリン) |
|||
* エチレフリン(エホチール) |
|||
* [[ドーパミン|ドパミン]](イノバン) |
|||
* [[ドブタミン]](ドブトレックス) |
|||
* [[アドレナリン]](ボスミン) |
|||
* [[ノルアドレナリン]](ノルアドレナリン) |
|||
麻酔管理に直接関連する死亡例は非常に稀であるが、胃内容物の[[誤嚥|肺誤嚥]]<ref>{{cite journal|date=September 1999|title=Pulmonary aspiration of gastric contents in anaesthesia|journal=British Journal of Anaesthesia|volume=83|issue=3|pages=453–460|doi=10.1093/bja/83.3.453|pmid=10655918|vauthors=Engelhardt T, Webster NR|doi-access=free}}</ref>、 [[窒息]]<ref>{{cite journal|date=July 1956|title=Maternal death from aspiration asphyxia|journal=British Medical Journal|volume=2|issue=4983|pages=16–19|doi=10.1136/bmj.2.4983.16|pmid=13329366|pmc=2034767|vauthors=Parker RB}}</ref>、[[アナフィラキシー]]が原因となることがある<ref>{{cite journal|date=November 2009|title=Anaphylaxis and anesthesia: controversies and new insights|journal=Anesthesiology|volume=111|issue=5|pages=1141–1150|doi=10.1097/ALN.0b013e3181bbd443|pmid=19858877|vauthors=Dewachter P, Mouton-Faivre C, Emala CW|doi-access=free}}</ref>。これらは、{{仮リンク|麻酔関連機器|en|Instruments used in anesthesiology}}の故障や、より一般的には[[ヒューマンエラー]]によって起こる可能性がある。1984年、米国で放送された麻酔事故のテレビ番組をきっかけに、米国の麻酔科医Ellison C. Pierceは、{{仮リンク|アメリカ麻酔科学会|en|American Society of Anesthesiologists|label=米国麻酔科学会}}内に麻酔患者安全・リスク管理委員会を設置した<ref name="Guadagnino2000">{{Cite web |title=Improving anesthesia safety |author=Guadagnino C |publisher=Physician's News Digest, Inc. |location=Narberth, Pennsylvania |year=2000 |url=http://physiciansnews.com/spotlight/200wp.html |access-date=8 September 2010 |archive-url=https://web.archive.org/web/20100815080827/http://physiciansnews.com/spotlight/200wp.html |archive-date=15 August 2010}}</ref>。この委員会は、麻酔に関連する[[罹患率]]や[[死亡率]]の原因を突き止め、低減させることを任務としていた<ref name="Guadagnino2000" />。この委員会から生まれた「麻酔患者安全財団」('''{{Lang-en|Anesthesia Patient Safety Foundation (APSF)}}''')は、「いかなる患者も麻酔によって害されることのないように」という目標を掲げ、1985年に独立[[法人#営利法人と非営利法人|非営利法人]]として設立された<ref>{{Cite web |title=Foundation History |author=Stoelting RK |publisher=Anesthesia Patient Safety Foundation |location=Indianapolis, IN |year=2010 |url=http://www.apsf.org/about_history.php |access-date=8 September 2010}}</ref>。 |
|||
==== 降圧薬(カルシウム拮抗薬) ==== |
|||
* ニカルジピン(ペルジピン) |
|||
* ジルチアゼム(ヘルベッサー) |
|||
稀ではあるが、重大な全身麻酔の合併症には'''[[悪性高熱症|悪性高熱]]'''がある<ref>{{Cite journal|date=January 2020|title=The anaesthetist, opioid analgesic drugs, and serotonin toxicity: a mechanistic and clinical review|journal=British Journal of Anaesthesia|volume=124|issue=1|pages=44–62|DOI=10.1016/j.bja.2019.08.010|PMID=31653394}}</ref><ref>{{Cite journal|date=December 2019|title=Malignant Hyperthermia: A Clinical Review|journal=Advances in Anesthesia|volume=37|pages=35–51|DOI=10.1016/j.aan.2019.08.003|PMID=31677658}}</ref>。 基幹病院では、この潜在的な合併症のために、手術室の近くに緊急用の薬剤([[ダントロレン]])を常備すべきとされる<ref>{{Cite journal|date=August 2004|title=Safe duration of postoperative monitoring for malignant hyperthermia susceptible patients|journal=Anaesthesia and Intensive Care|volume=32|issue=4|pages=502–509|DOI=10.1177/0310057X0403200407|PMID=15675210}}</ref>。 |
|||
==== 血管拡張薬 ==== |
|||
* [[ニトログリセリン]](ミリスロール) |
|||
: 虚血性心疾患の治療にも用いられる。 |
|||
* [[プロスタグランジン]]E<sub>1</sub>(プロスタンディン) |
|||
* [[ニコランジル]](シグマート) |
|||
: 冠血管拡張薬 |
|||
== 脚注 == |
|||
=== 注釈 === |
|||
===== 心拍数のコントロール ===== |
|||
{{Notelist}} |
|||
======徐脈に対して====== |
|||
=== 出典 === |
|||
* [[アトロピン]](硫酸アトロピン) |
|||
{{Reflist}} |
|||
* [[イソプロテレノール]](プロタノール) |
|||
== 関連項目 == |
|||
======頻脈に対して====== |
|||
* [[麻酔]] |
|||
* [[ベラパミル]](ワソラン) |
|||
* [[局所麻酔]] |
|||
* [[ジルチアゼム]](ヘルベッサー) |
|||
* [[神経遮断麻酔]] |
|||
* エスモロール(ブレビブロック) |
|||
* [[歯科麻酔学]] |
|||
* ランジオロール(オノアクト) |
|||
===== 心室性不整脈に対して ===== |
|||
* [[リドカイン]] |
|||
== バランス麻酔 == |
|||
全身麻酔の3要素として、鎮痛・鎮静・筋弛緩(有害反射の抑制を含めると4要素)があげられる。かつて用いられていたエーテルのような麻酔薬では、単一薬物で3要素を満たしているように考えられてきた。このため、麻酔深度という一言で麻酔レベルが表現されてきた。 |
|||
しかし、現在の全身麻酔薬は導入・覚醒が速い一方、麻酔の要素のいずれかを持たないか、持っていても弱いことが多い。したがって、単一で全身麻酔の3要素を満たすことは現実的ではない。さらに、深いレベルの鎮静によって手術侵襲に対する循環系の亢進が抑制されていても、サイトカインやカテコラミンなどで表される神経内分泌反応は抑制できないことが判明している。そこで、現在は3要素のそれぞれが至適レベルになるよう鎮静・鎮痛・筋弛緩薬を投与するバランス麻酔が主流になっている。なお、硬膜外麻酔などの神経ブロックを併用することによって強力な鎮痛や筋弛緩を得ることも可能であることから、薬物だけではなく局所麻酔法を併用することもバランス麻酔に含まれている。 |
|||
麻酔薬を併用する場合には薬物相互作用を考慮する必要がある。揮発性麻酔薬に亜酸化窒素を併用する場合には[[最小肺胞内濃度|MAC]]は相加的であるが、異なる受容体に作用する薬物の併用時、たとえばプロポフォールとオピオイドなどにおいては相乗的に働く。 |
|||
== 全静脈麻酔 == |
|||
全静脈麻酔(total intravenous anesthesia:TIVA)は全身麻酔を静脈麻酔薬のみで行う麻酔であるが、広義では揮発性麻酔薬やガス麻酔薬を用いない方法ととらえられており、[[硬膜外麻酔]]などの[[神経ブロック]]を併用することも含まれている。 |
|||
TIVAはプロポフォールと[[フェンタニル]]の組み合わせで行われてきたが、超短時間作用型オピオイドである[[レミフェンタニル]]や、蓄積性のより少ない非脱分極性筋弛緩薬である[[ロクロニウム]]の登場により、施行頻度は上昇している。TIVAに用いられる鎮静・鎮痛・筋弛緩薬はいずれも作用発現が速く、持続時間が短いことに加え、強力な作用を有していることから、全身麻酔薬の調節性が向上した。 |
|||
TIVAの利点は揮発性麻酔薬などによる[[オゾン層]]破壊といった地球環境への影響がないことと、亜酸化窒素使用に伴う腸管膨大作用や閉鎖腔の問題を回避できることなどがある。 |
|||
== NLA == |
|||
NLAとはニューロレプト鎮痛(neuroleptanalgesia)またはニューロレプト麻酔(neuroleptanesthesia)の略称である。ニューロレプト鎮痛では神経遮断薬(neuroleptics)と鎮痛薬(analgesics)を併用することにより、患者は周囲に無関心な鎮静状態となるが、意識は消失しない。 |
|||
ニューロレプト麻酔ではニューロレプト鎮痛に亜酸化窒素を併用し意識を消失させる。NLAには原法と変法があり、原法ではドロペリドールとフエンタニルを用いる。変法では原法以外の組み合わせが用いられ、ベンゾジアゼピンと拮抗性鎮痛薬を併用することが多い。 |
|||
NLAの特徴として循環抑制作用が比較的軽度であることがあげられるが、脱水患者などでは注意を要する。また、術後まで鎮静・鎮痛作用が持続することや、術中に指示動作が可能な点、ドロペリドールを用いる際には強力な制吐作用を得られる点があげられる。しかし、欠点として、鎮痛・鎮静レベルを推定することが困難であることや、手術侵襲による血圧上昇・頻脈がある。この麻酔法は薬剤添付文書や教科書には記載が見られるが、2018年現在では原法・変法ともにほとんど施行されることがなくなっている。理由としては、ドロペリドールには半減期が長く、錐体外路症状やQT延長の副作用があること、フェンタニルはレミフェンタニルよりも調節性に劣ること、亜酸化窒素は閉鎖腔の内圧を上昇させること、ベンゾジアゼピン系や拮抗性鎮痛薬は調節性に劣ることなどが挙げられる。しかし、意識下挿管時にはNLAはその呼吸・循環抑制の少なさから、よい適応となる場合がある。 |
|||
== 脚注 == |
|||
{{脚注ヘルプ}} |
|||
{{Reflist|30em}} |
|||
== 参考文献 == |
== 参考文献 == |
||
{{No footnotes|date=2016年7月|section=1}} |
|||
* 麻酔科必修マニュアル 羊土社 ISBN 4897063442 |
|||
* STEP 麻酔科 海馬書房 ISBN 4907704275 |
|||
* イヤーノート内科外科等編 2007年版 メディックメディア ISBN 9784896321500 |
|||
* 麻酔科シークレット メディカルサイエンスインターナショナル ISBN 9784895923224 |
|||
* 麻酔科研修の素朴な疑問に答えます ISBN 4895924440 |
|||
* 麻酔の研修ハンドブック ISBN 4765309762 |
|||
* 周術期管理チームテキスト 第3版, 公益社団法人 日本麻酔科学会(発行), 2016年8月10日発行 |
* 周術期管理チームテキスト 第3版, 公益社団法人 日本麻酔科学会(発行), 2016年8月10日発行 |
||
== |
== 外部リンク == |
||
* [[静脈麻酔薬]] |
|||
* [http://www.chm.bris.ac.uk/motm/chloroform/chloroformh.htm Chloroform: ''The molecular lifesaver''] ブリストル大学の論文で、クロロホルムに関する興味深い事実が紹介されている(英語)。 |
|||
* [[吸入麻酔薬]] |
|||
* [https://web.archive.org/web/20040515001721/http://www.anzca.edu.au/publications/profdocs/profstandards/PS18_2000.htm Australian & New Zealand College of Anaesthetists Monitoring Standard] オーストラリア・ニュージーランド麻酔学会(ANZCA)のモニター基準(英語) |
|||
* [[周術期管理]] |
|||
* [https://web.archive.org/web/20051219095333/http://www.rcoa.ac.uk/index.asp?PageID=69 Royal College of Anaesthetists Patient Information page] 英国王立麻酔科協会の患者向けサイト(英語) |
|||
* [[術中合併症]] |
|||
{{麻酔}} |
|||
* [[術後合併症]] |
|||
* [[麻酔]] |
|||
* [[歯科麻酔学]] |
|||
{{Medical-stub}} |
|||
{{Normdaten}} |
{{Normdaten}} |
||
2023年4月30日 (日) 08:36時点における版
| 全身麻酔 | |
|---|---|
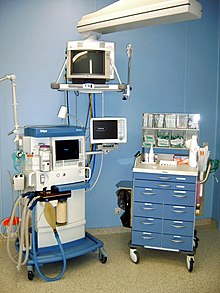 全身麻酔にて使われる器具の一例
| |
| MeSH | D000768 |
| MedlinePlus | 007410 |
全身麻酔(ぜんしんますい、英: General anesthesia)は、痛覚刺激を与えても患者が覚醒しないように、人為的に誘発される意識喪失である[1]。この効果は、静脈内または吸入の全身麻酔薬を投与することで得られ、しばしば鎮痛剤および神経筋遮断薬が併用される。手術中は自発呼吸が十分でないことが多く、気道を保護するための介入が必要となることが多い[1]。全身麻酔は一般に、手術室では患者にとって耐え難い痛みを伴う外科手術を可能にするために、集中治療室や救急救命室では、重症患者の気管挿管や機械換気を容易にするために実施される。
日本では、全身麻酔の目標は「麻酔の3要素」、すなわち鎮静・鎮痛・筋弛緩とされることが多い[2]。有害反射の抑制も加えて麻酔の4要素とされることもあるが、これは元はWoodbridgeらが1957年に提唱した麻酔深度の概念に遡ることができる[3]。英語圏では、無意識状態、健忘、鎮痛、自律神経系の反射消失、場合によっては骨格筋の麻痺を達成することが全体目標とされることも多い。すなわち、4要素ないしは5要素となっており、鎮静において無意識状態と健忘が別個の評価項目となっていることによる。
患者や処置に最適な麻酔薬の組み合わせは、通常、麻酔科医が、患者、外科医、歯科医師、または手術処置を行う他の施術者と相談しながら選択する[4](p58)。
歴史
全身麻酔の試みは、古代シュメール人、バビロニア人、アッシリア人、エジプト人、ギリシャ人、ローマ人、インド人、中国人の書物から、歴史的にたどることができる。2世紀から3世紀に書かれた『三国志』には、中国後漢末期に華陀が「麻沸散」という麻酔薬を用いて手術を行ったと記載されている。この「麻沸散」は全身麻酔薬であろうと考えられているが、どのようなものであったかは明らかではない。
中世には、東洋においてもヨーロッパにおいても科学は医学的に大きな進歩を遂げた。
ルネッサンス期には、解剖学と外科学に大きな進歩があった。しかし、このような進歩にもかかわらず、手術は依然として最後の治療法であった。手術は痛みを伴うため、多くの患者は手術を受けるよりも死を選んだ。全身麻酔の発見については、誰が最も功績を残したかについて定説は無いが、18世紀後半から19世紀初頭にかけてのいくつかの科学的発見が、近代的麻酔技術の導入と発展に不可欠であった[5]。
正確に確認できる全身麻酔の記録としては、文化元年10月13日(1804年11月14日)に華岡青洲が行った乳癌の手術が初出である[6]。このとき用いられた麻酔薬「通仙散」はチョウセンアサガオにトリカブトやトウキなどを配合した薬品であった。西洋では、1846年にアメリカでウィリアム・T・G・モートンが行ったジエチルエーテルによる手術が初の全身麻酔手術となる。エーテルは引火性が問題であり、すぐにクロロホルムに取って代わられたが、クロロホルムも毒性のために死者が相次ぎ、使われなくなるのに時間はかからなかった。
19世紀後半には、近代外科学への移行を可能にする二つの大きな飛躍があった。病原菌説の理解により、外科手術における感染予防技術の開発と応用が急速に進んだのである。防腐法(英語: antisepsis)はやがて無菌法(英語: asepsis)に変わり、外科手術の合併症と死亡率は、以前の時代よりはるかに低くなった[7]。
同時に、薬理学や生理学の分野でも大きな進歩があり、全身麻酔や痛みのコントロールが可能になった。
1934年に、アメリカのアーネスト・ヴォルワイラーによって開発されたチオペンタールは、現在に至るまで全身麻酔薬として使用されており、WHOの必須医薬品リストにも指定されている。
20世紀には、気管挿管やその他の高度な気道確保技術を日常的に使用することにより、全身麻酔の安全性と有効性が改善された。また、モニタリングの大幅な進歩や、薬物動態学的および薬力学的特性が改善された新しい麻酔薬も、この傾向に貢献した。最終的には、麻酔科医のための標準化されたトレーニングプログラムが、この時期に出現した。
目的
全身麻酔には多くの目的があり、あらゆる外科手術に日常的に使用されている。適切な手術時の麻酔には、以下のような目標が求められる。
- 催眠・無意識(意識の喪失)
- 鎮痛(痛みに対する反応の喪失)
- 健忘(記憶の喪失)
- 不動(運動反射の消失)
- 麻痺(骨格筋の弛緩)[8]
生化学的作用機序
全身麻酔薬の生化学的な作用機序はよく分かっていない[9]。植物も動物同様に麻酔薬による作用をうけることは分かっている[10]。意識を失わせるために、麻酔薬は無数の作用部位を持ち、中枢神経系(CNS)に複数のレベルで作用する。全身麻酔は、大脳皮質、視床、網様体賦活系、脊髄を含む中枢神経系構成要素の機能を抑制・変化させるのが一般的である。麻酔状態に関する現在の理論では、中枢神経系における標的部位だけでなく、無意識と関連した神経ネットワークや覚醒回路も特定されており、一部の麻酔薬は特定の睡眠活性部位を活性化する可能性があることが分かっている[11]。全身麻酔薬の分子薬理学的標的は、GABAAとNMDAグルタミン酸受容体であると考えられている。全身麻酔は、神経信号の抑制性伝達を増強するか、あるいは興奮性伝達を減少させるという仮説が立てられた[12]。ほとんどの揮発性麻酔薬はGABAAアゴニストであることが判明しているが、受容体への作用部位は不明なままである[13]。ケタミンは非競合的なNMDA受容体拮抗薬である[14]。
吸入麻酔薬は、化学構造と特性から、細胞膜を標的とすることが示唆されているが、その正確なメカニズムは100年以上謎のままであった。2020年の研究では、吸入麻酔薬(クロロホルムとイソフルラン)が脂質ラフトへのホスホリパーゼD2の局在を乱し、シグナル伝達分子であるホスファチジン酸の産生につながることが実証された。シグナル伝達分子はカスケード反応を引き起こし、最終的にはTWIK関連K+チャネル(TREK-1)を活性化させる。ホスホリパーゼD2遺伝子欠損 (PLDnull)ミバエは麻酔抵抗性であることが示されており、この結果により、吸入麻酔薬の標的が細胞膜介在性であることが確立された[15][16]。
術前評価
予定手術の前に、麻酔科医はカルテを調べたり、患者の問診をしたりして、病歴に関する情報を入手し、周術期のリスクを判断する。問診に基づき、麻酔科医は麻酔計画を立て、手術に最適な薬剤の組み合わせと投与量を決定する。また、安全で効果的な手術を行うために、モニタリング機器を追加する必要がある場合もある。この評価で重要なのは、患者の年齢、性別、ボディマス指数(BMI)、病歴、手術歴、現在服用している薬、絶食時間などである[17][18] 。術前の徹底的かつ正確な評価は、麻酔計画の効果的な安全性を確保するために極めて重要である。例えば、アルコールや違法薬物を大量に摂取している患者が、その事実を開示しなかった場合、手術中に薬物投与量が不足し、術中覚醒や術中高血圧の原因となる可能性がある[19][20]。また、一般的に使用されている薬剤は麻酔薬と相互作用する可能性があり、そのような使用状況を開示しないと、手術中のリスクが高まる可能性がある。また、最後の食事のタイミングが正確でないと、食物の誤嚥の危険性が高まり、重篤な合併症につながる可能性がある[21]。
麻酔前の評価で重要なのは、開口状況の確認と咽頭の軟部組織の観察を含む患者の気道の評価である[22]。歯の状態や歯冠の位置を確認し、頸部の柔軟性と伸展性を観察する[23][24]。最も一般的に行われている気道評価はマランパチ分類で、口を開けて舌を出した状態で軟口蓋の構造を見ることができるかどうかで気道を評価するものである。マランパチテストだけでは精度が低いため、マランパチテストに加え、開口度、甲状頤間距離、頸部可動域、下顎骨突出などの評価も日常的に行われている。また、気道の形態異常が疑われる患者には、内視鏡検査や超音波検査で気道の評価を行った上で、気道確保を計画することもある[25]。
アメリカ麻酔科学会では全身状態を6つに分類しており、ASA-PS(ASA physical status)と呼んでいる。手術前のASA-PSと予後は相関する。
予定手術であれば十分な時間をかけた術前評価が可能だが、緊急手術の術前評価は時間的な制限が多い。
前投薬
全身麻酔を行う前に、麻酔科医は麻酔の質や安全性を補ったり向上させたりするために、1種類以上の薬剤を投与することがある。これを前投薬という。前投薬の多くには弱い鎮静効果があり、手術中に使用する麻酔薬の量を減らすことができる場合が多い[26](pp643,646,1057)。
海外でよく使われる前投薬にα2アドレナリン作動薬であるクロニジンがある[27][28]。術後シバリング[29]、術後の悪心・嘔吐[30]、覚醒時せん妄を軽減する[26](p2259)。しかし、2021年の無作為化比較試験で、クロニジンは就学前の子どもには抗不安作用が少なく、鎮静作用が強いことが実証された。経口クロニジンは最大効果発現には45分ほどかかる[31]。クロニジンの欠点は低血圧と徐脈であるが、高血圧と頻脈の患者には有利に働く可能性がある[32]。もう一つのα-2アドレナリン作動薬であるデクスメデトミジンは、短期間の鎮静効果(24時間以内)のためによく使用される。デクスメデトミジンとある種の非定型抗精神病薬は、非協力的な子供にも使用されることがある[33]。日本では2023年現在、クロニジンもデクスメデトミジンも前投薬としては適応外使用となる。
ベンゾジアゼピン系も前投薬としてよく使用される薬物である。ベンゾジアゼピン系で最もよく使用されるのはミダゾラムであり、速効性と短時間作用が特徴である。ミダゾラムは、小児の分離不安など術前不安の軽減に効果的である[34]。また、術後の悪心・嘔吐の軽減、軽度の鎮静、交感神経抑制、前向性健忘をもたらす[26](p657)。
メラトニンは、催眠作用、抗不安作用、鎮静作用、鎮痛作用、抗けいれん作用があるため、成人および小児の麻酔前投薬として有効であることが判明している。メラトニンの前投薬後は、ミダゾラムよりも回復が早く、術後の興奮やせん妄の発生率も減少する[35]。メラトニンは、ベンゾジアゼピンと比較して、成人患者の周術期不安の軽減に同様の効果があることが示されている[36]。メラトニンも日本では前投薬は適応外使用となる。
麻酔前投薬のもう一つの例として、βアドレナリン拮抗薬の術前投与があり、これは心臓手術後の頻脈性不整脈を軽減することが示されている[37]。しかし、心臓以外の手術では、β遮断薬による有害事象の増加との関連も指摘されている。麻酔科医は、術後の悪心・嘔吐を防ぐために、オンダンセトロン、ドロペリドール、デキサメタゾンなどの制吐剤を少なくとも1種類は投与することがある[26](p2260)。NSAIDsも鎮痛前投薬として用いられることがあり、フェンタニルなどのオピオイドの必要性をしばしば減少させる。また、メトクロプラミドのような消化管運動促進剤、ファモチジンのようなヒスタミン拮抗剤も使用される[26](p2260)。
非薬物的な麻酔前介入としては、認知行動療法、音楽療法、アロマセラピー、催眠マッサージ、術前説明ビデオ、誘導イメージによるリラックス療法などがある[38]。これらの手法は、特に小児や知的障害のある患者に有効である。ビデオゲームによって、感覚刺激を最小限に抑えたり、気晴らしをすることは、全身麻酔の導入前または導入中の不安の軽減に役立つと考えられる。しかし、この種の不安の軽減に最も効果的な非薬物学的アプローチを確認するためには、より大規模で質の高い研究が必要である[39]。前投薬および麻酔導入時の両親の同席は、小児の不安を軽減することが示されていない。同席を希望する親を積極的に阻止すべきではなく、同席を希望しない親を無理強いすべきではないことが示唆されている[39]。
麻酔深度
ゲデルの麻酔深度分類は、1937年にアーサー・アーネスト・ゲデルが発表したもので[40]、 麻酔の4つの段階を表している。新しい麻酔薬や麻酔導入技術により、麻酔の開始と回復がより迅速に行われるようになったが(いくつかの段階は完全にスキップされることもある)、この原則は変わっていない。
- 1期
- 1期は、導入期とも呼ばれ、導入剤を投与してから意識を失うまでの期間である。この段階で、患者は記憶喪失を伴わない鎮痛状態から記憶喪失を伴う鎮痛状態へと進行する。この時、患者は会話を続けることができ、視覚障害を訴えることがある。
- 2期
- 第2期は、興奮期またはせん妄期とも呼ばれ、意識を失った後、興奮状態やせん妄状態が顕著になる時期である。この段階では、患者の呼吸と心拍が不規則になることがある。さらに、不随意運動、嘔吐、呼吸の中断、瞳孔散大がみられることもある。痙性運動、嘔吐、不規則な呼吸の組み合わせは患者の気道を損なう可能性があるため、この段階の時間を最小限に抑え、できるだけ早く第3期に到達するためには、速効性の薬剤を用いる。
- 3期
- 第3期は外科的麻酔期とも呼ばれ、骨格筋が弛緩し、嘔吐は停止する。呼吸抑制と眼球運動の停止がこの段階の特徴である。患者は意識を失い、手術ができる状態になる。この段階は4つの局面に分けられる。
- 眼球が上転し、その後固定され、眼瞼反射と嚥下反射が失われる。まだ規則的な自発呼吸がある。
- 角膜反射と喉頭反射が失われる。
- 瞳孔反射が消失し、腹筋・肋間筋の完全弛緩が認められる。ほとんどの手術に対応できる理想的な麻酔レベル。
- 横隔膜の完全麻痺と不規則な浅い腹式呼吸が起こる[41]。
- 4期
- 第4期は、昏睡期とも呼ばれ、手術刺激量に対して麻酔薬の投与量が多すぎる場合に起こり、患者は重度の脳幹または延髄の抑制を受け、呼吸が停止し、心血管虚脱を生じる可能性がある。この段階は、心血管系と呼吸器系のサポートがなければ致死的である[40]。
麻酔の導入
麻酔科学においてよく用いられる用語の「導入」とは、麻酔薬投与から気道確保を完了して、手術可能な状態となるまでの全身麻酔の初期段階のことを指す。全身麻酔は、通常、手術室または手術室に隣接する麻酔専用室で行われる。他に、内視鏡室、集中治療室、放射線科、循環器科、救急外来、救急車などでも行われる。災害現場など、患者の救出が不可能または非現実的な場所でも行われることがある。
麻酔薬は、吸入、注射(静脈内、筋肉内、皮下)、経口、直腸など、さまざまな経路で投与されることがある。麻酔薬は循環系に入ると、中枢神経系および自律神経系にある生化学的活性部位に到達する。
ほとんどの全身麻酔は、静脈内または吸入により導入される。一般的に使用される静脈内導入剤には、プロポフォール、チオペンタールナトリウム、エトミデート、メトヘキシタール、ケタミンなどがある。吸入麻酔は、静脈内投与が困難な場合(例、小児)、気道確保が困難と予想される場合、または患者が希望する場合に選択されることがある。セボフルランは、他の薬剤に比べて気管気管支樹への刺激が少ないため、吸入麻酔での導入に最もよく使用される薬剤である[42]。
導入に用いる薬剤の投与順序の一例
- 挿管中の無呼吸時間が長くなっても、血中酸素濃度に影響を与えないようにするために、肺を100%酸素で満たすために行う麻酔前の酸素吸入(前酸素化と称する。脱窒素ともいう)。
- 挿管時の鎮痛のためのレミフェンタニル
- 気管挿管のための鎮静剤としてのプロポフォール
- 開口や喉頭鏡操作を容易にするための筋弛緩薬として、ロクロニウム
- 挿管が完了したら、酸素から酸素と吸入麻酔薬の混合気体に変更する
喉頭展開と挿管は、どちらも非常に刺激が強いものである。上記の導入の過程では、これらの操作に対する血圧上昇などの反応を抑制すると同時に、挿管の間に意識がある、というような事が無いよう、昏睡に近い状態に誘導する。
導入方法

以下の3種類の方法に大別される[注釈 1]。
1. 急速導入(Rapid Induction)
- 静脈麻酔薬を用いて入眠させる、最も頻用されている麻酔導入方法。
2. 緩徐導入(Slow Induction)
- 吸入麻酔薬によりマスク換気で入眠させ、麻酔を深くしたあと、静脈路確保を行う麻酔導入方法。覚醒状態で末梢静脈カテーテルの確保が困難な小児などに用いる。
3. 迅速導入(Rapid sequence induction)
- 以前はCrash Inductionとも呼ばれた。緊急時の手術などで、胃内容物が多く(フルストマック)、誤嚥の危険性が高い状況で行われる導入方法で、十分な前酸素化のあと、静脈麻酔薬と筋弛緩薬を一度に投与し、マスク換気を行わずに気管挿管を行う方法。挿管前後に輪状軟骨を圧迫して食道を閉鎖して胃内容物の逆流を防ぐ。
生理学的モニタリング
モニタリング機器により、全身麻酔の導入、維持、そして覚醒をコントロールすることができる。麻酔の基本的なモニタリングの基準は、アメリカ麻酔科学会が発表したガイドラインで、麻酔中に患者の酸素化、換気、循環、体温を継続的に評価する必要があると記述されている[43]。
- 連続心電図モニタ(ECGまたはEKG): 電極を患者の皮膚に貼り付けて、心拍数と心拍リズムを監視する。これは、麻酔科医が心臓の虚血の初期徴候を識別するのに役立つ場合がある。通常、不整脈はⅡ誘導、虚血はⅤ5誘導でモニターする。
- 連続パルスオキシメトリー(SpO2): 患者のヘモグロビン酸素飽和度の低下(低酸素血症)を早期に発見するために、通常、指に装着する装置。
- 血圧モニタリング: 患者の血圧を測定する方法は2つある。まず、最も一般的なのは、非侵襲的血圧(NIBP)モニタリングである。これは、患者の腕、前腕、または脚に血圧計を装着するものである。手術中は、あらかじめ設定された一定の間隔で、機械が血圧を測定する。2つ目の方法は、侵襲的血圧(IBP)モニタリングで、血圧の一拍ごとのモニタリングが可能である。この方法は、重症の心臓疾患や肺疾患のある患者、心臓手術や移植手術などの大きな手術を受ける患者、大量の出血が予想される患者に限られる。この方法では、通常、手首(橈骨動脈)または鼠径部(大腿動脈)の動脈に、特殊なプラスチック製のカニューレを挿入する。
- 薬剤濃度測定:麻酔器には通常、吸入麻酔薬の使用割合や呼気濃度を測定するためのモニターがある。これらのモニターには、酸素、二酸化炭素、および吸入麻酔薬(亜酸化窒素、セボフルランなど)の測定が含まれる。
- 酸素濃度計: ほとんどすべての麻酔器の回路には、患者への酸素供給が損なわれた場合に備えてアラームが搭載されている。アラームは、吸入酸素の割合が設定された閾値を下回ると作動する。
- 回路外れアラーム(または低圧アラーム): 機械換気中に麻酔器の回路内圧が、正常に陽圧換気が行われていれば到達するはずの圧力に達しないことを示す。
- カプノグラフィー: 患者の呼気の二酸化炭素の量をパーセントまたはmmHgで表示し、麻酔科医が換気の適切さを評価できるようにするものである。通常、麻酔科医はより繊細な変化を確認するためにmmHgを使用する。
- 体温測定: 低体温や発熱の判別、悪性高熱症の早期発見のため
- 脳波、エントロピーモニター、その他の脳波測定システム: 麻酔の深さを確認するために用いられる。これにより、術中覚醒や過剰投与の可能性を低減することができる。
気道管理
麻酔中の患者は、麻酔薬、オピオイド、筋弛緩剤の影響により、気道保護反射(咳など)、気道開存性、時には規則的な呼吸パターンが消失する。気道を確保し、呼吸を調節するために、患者が意識を失った後に何らかの呼吸チューブが挿入される。機械換気を可能にするために、気管チューブがしばしば使用されるが、フェイスマスクやラリンジアルマスクなど、呼吸を補助できる別の器具も存在する。一般に、完全な機械的換気は、侵襲度の高い処置のために非常に深い全身麻酔状態を引き起こす場合、および/または重症患者や負傷した患者に対してのみ使用される。とはいえ、全身麻酔を導入すると、通常は無呼吸になり、薬物が切れて自発呼吸が始まるまで換気が必要となる。つまり、全身麻酔の導入と維持の両方に換気が必要な場合と、導入時だけに換気が必要な場合がある。しかし、人工呼吸器による機械換気は、自発呼吸の間、十分なガス交換を確保するための換気補助を行うこともできる。
全身麻酔は、患者が自発的に呼吸している状態でも行うことができ、その結果、患者自身の酸素濃度を維持することができる。よって、自発呼吸維持は特殊な状況(例:気道確保困難、非挿管下手術)において有益となることがある。自発呼吸は従来、吸入剤(ハロタンやセボフルランなど)で維持されてきたが、これは緩徐導入と呼ばれる。また、静脈麻酔(例:プロポフォール)を使用して自発呼吸を維持することも可能である。自発呼吸を維持するための静脈麻酔は、吸入麻酔薬に比べて一定の利点(喉頭反射の抑制など)があるが、慎重に滴定する必要がある。静脈麻酔と高流量鼻腔酸素を用いた自発呼吸(STRIVE HiTM)は、困難気道で閉塞している場合に使用されてきた技術である[44]。
眼球保護
全身麻酔は眼輪筋の緊張性収縮を低下させ、59%の人に兎眼(不完全な閉眼)を引き起こす[45]。さらに、涙の産生と涙液膜の安定性が低下し、角膜上皮の乾燥が起こり、リソゾームによる保護が低下する。また、ベル現象(睡眠中に眼球が上を向き、角膜を保護する現象)による保護も失われてしまう。全身麻酔中の眼球損傷の可能性を減らすために、慎重な管理が必要である[46]。全身麻酔中の眼の損傷を防ぐ方法としては、瞼をテープで閉じる、眼軟膏を使用する、特殊なデザインの眼球保護ゴーグルを使用する、などがある。
神経筋遮断

神経筋遮断薬による麻痺、すなわち一時的な筋弛緩は、現代の麻酔に不可欠な要素である。この目的で最初に使用された薬剤は1940年代に導入されたクラーレであったが、現在では副作用が少なく、一般に作用時間の短い薬剤に取って代わられている。筋弛緩によって、腹部や胸部などの主要な体腔内の手術を、深い麻酔(循環器系などへの悪影響が強い)を必要とせずに行うことが可能となり、また気管挿管も容易となる。
アセチルコリンは、神経筋接合部に存在する天然の神経伝達物質で、神経末端から放出されると筋肉を収縮させる作用がある。筋弛緩剤は、アセチルコリンが受容体に結合するのを阻害することによって作用する。呼吸筋(横隔膜と胸の肋間筋)が麻痺すると、何らかの人工呼吸が必要となる。喉頭筋も麻痺しているため、通常、気管チューブを用いて気道を確保する必要がある[47]。
運動麻痺を最も簡単にモニターできるのは、筋弛緩モニタである。この装置は、末梢神経の皮膚から短い電気パルスを断続的に送りながら、その神経に供給されている筋肉の収縮を観察するものある。筋弛緩剤の効果は、手術終了時にコリンエステラーゼ阻害薬によって元に戻されることが多く、副作用を最小限に抑えるためにムスカリン系抗コリン薬と併用投与される。現在使用されている骨格筋弛緩薬の例としては、パンクロニウム、ロクロニウム、ベクロニウム、シスアトラクリウム、アトラクリウム、ミバクリウム、サクシニルコリンがある。スガマデクスのような新しい神経筋遮断回復剤も使用できる;これは筋弛緩薬と直接結合して神経筋接合部からそれを取り除くことで効果を発揮する。スガマデクスは2015年に米国で使用が承認され、急速に普及が進んだ。2022年の研究では、スガマデクスとネオスチグミン(頻用されているアセチルコリンエステラーゼ阻害剤)は、神経筋遮断から回復作用において同様に安全である可能性が高いことが示されている[48]。
麻酔の維持
静脈内導入剤の作用時間は一般に5~10分で、その後、自然に意識が回復する[49]。手術の間、無意識状態を持続させるためには、麻酔を維持する必要がある。そのためには、酸素と揮発性麻酔薬の混合ガスを注意深くコントロールして患者に吸入させるか、静脈内投与を行う(通常はプロポフォール)。吸入麻酔薬は、オピオイド(通常はフェンタニルまたはフェンタニル誘導体)系の静脈内鎮痛剤や鎮静剤(通常はプロポフォールまたはミダゾラム)などによってよく補完される。プロポフォールは全静脈麻酔(TIVA)に使用できるため、吸入薬による補完は必要ない[50]。2023年現在、日本で麻酔維持に保険適応があるのはプロポフォールとレミマゾラムである。全身麻酔は通常安全であると考えられているが、局所麻酔薬による味覚および/または嗅覚の変調、全身麻酔の副作用として脳卒中、神経損傷を生じた患者の報告例がある[51]。
手術が終わると、麻酔薬の投与は中止される。脳内の麻酔薬の濃度が一定以下になると、意識が回復する(手術時間にもよるが、通常1~30分以内に回復する)[52]。
1990年代、スコットランドのグラスゴーで、麻酔を維持する新しい方法が開発された。標的制御注入 (TCI)と呼ばれるこの方法は、コンピュータ制御のシリンジポンプを用いて、手術中持続的にプロポフォールを注入し、揮発性麻酔薬を必要とせず、薬理学の理論により望ましい薬剤濃度を設定して、投与量をより正確に指定することができるものである。利点としては、麻酔からの回復が早い、術後の悪心・嘔吐の発生が少ない、悪性高熱症の誘因がない、などが挙げられる。現在、米国ではTCIは認められていないが、代わりに一定量の薬剤を供給するシリンジポンプが一般的に使用されている[53]。日本ではプロポフォールのTCIのみ、認められている。
副作用の治療や合併症の予防のために、他の薬剤が使用されることもある。高血圧の治療には降圧剤、低血圧の治療にはエフェドリンやフェニレフリン、喘息や喉頭痙攣、気管支痙攣の治療にはサルブタモール、アレルギー反応の治療にはエピネフリンやジフェンヒドラミンなどが使用される。炎症と感染を防ぐために、グルココルチコイドと抗生物質がそれぞれ投与されることもある[52]。
覚醒・抜管
麻酔における覚醒 (英: emergence)とは、全身麻酔の終了後、すべての器官系が元の生理的機能に戻ることである。この段階では、覚醒時せん妄(急性精神錯乱)、失語(会話の発声または理解の障害)、感覚または運動機能の巣症状などの一時的な神経学的症状を伴うことがある。血圧の上昇や低下、頻脈、その他の心不整脈などの心血管系イベントも、呼吸困難などの呼吸器系症状と同様に、全身麻酔からの覚醒時に起こりやすい。
麻酔薬を止め、意識が回復し、筋弛緩作用からの回復も十分で、一回換気量、呼吸回数、指示に従う、などの条件を満たせば気管チューブを抜くことができる。これを抜管(ばっかん)という。言葉による指示に反応し、従うことは、患者の抜管準備の評価によく利用される基準である[注釈 2][54]。ただし、この状態でも筋弛緩薬の効果はある程度残っているため、アセチルコリンエステラーゼ阻害薬であるネオスチグミンと、ムスカリン作用を抑制するための硫酸アトロピンを投与し、筋弛緩薬のリバース(拮抗)を行う。リバースを行う場合、筋弛緩薬がある程度自然に消退していないと、再筋弛緩が発生するため危険である。近年では選択的筋弛緩薬結合薬であるスガマデクスが用いられる事が多い。抜管後、患者を観察し問題なければ手術室から術後回復室又は病棟に帰室させる。
予想される濃度や時間を超えて意識や反応が回復しない状態は覚醒遅延という。
術後管理

術後の痛みは、麻酔後回復室(PACU)で区域麻酔や非経口薬で管理される。患者はオピオイドのほか、非ステロイド性抗炎症薬やアセトアミノフェンなどの薬剤を投与されることもある[55]。また、患者管理鎮痛 (PCA)と呼ばれるシステムを用いて、患者自身がオピオイドを投与することもある[56]。患者がPCAのボタンを押すと、注射器が作動し、通常モルヒネ、フェンタニル、オキシコドンなどの強オピオイド(例:フェンタニル10µg)の初期設定量の「ボーラス量」を投与される。PCA装置はその後、薬物が効果を発揮し、また患者が過剰摂取するのを防ぐために、あらかじめ設定された期間「ロックアウト」すなわちボタン操作不能となる。患者が眠くなりすぎたり、鎮静状態になると、それ以上鎮痛剤を要求しなくなる。このように、持続注入法にはないフェイルセーフの側面がある。これらの薬物療法で効果的に痛みを抑えることができない場合は、神経ブロックと呼ばれる方法で神経に直接局所麻酔薬を注入することがある[57][58]。
回復室では、酸素飽和度[59][60]、心拍、呼吸[59][61]、血圧[59]、中枢温など、多くのバイタルサインをモニターする。
術後シバリングはよく見られる。提唱されている機序は、脊髄が脳よりも速い速度で回復するという観察に基づいている。この結果、間代性活動(震え)として表れる脊髄反射が抑制されなくなる。この理論は、中枢神経刺激剤であるドキサプラムが術後のシバリングを消失させるのに幾分有効であるという事実からも支持される[62]。シバリングは、不快感や痛みの悪化のほか、酸素消費量の増加、カテコールアミンの放出、低体温のリスク、乳酸アシドーシスを誘発することが分かっている[63]。シバリングを軽減するために、暖かい毛布[64][65]や、温風加温装置と呼ばれる暖められた空気を循環させるシートで患者を包むなど、様々な手法が用いられる[66][67]。外部加温装置でシバリングを軽減できない場合は、デクスメデトミジンなどの薬剤[68][69]、またはその他のα2-アゴニスト、抗コリン剤、中枢神経刺激剤、または副腎皮質ステロイドを用いてもよい[55][70]。
多くの症例において、腹部以外の手術すら、周術期に用いるオピオイドが術後イレウスの一因となり得る。アルビモパンなどのμオピオイド拮抗薬を術後すぐに投与すれば、退院時期を早めることができるが、麻痺性イレウスの発症を抑えることはできない[71]。
Enhanced Recover After Surgery (ERAS、イーラス) は、ケアの継続性を確保し、回復と周術期ケアを改善するための最新のガイドラインとコンセンサスを提供する学会である。パスウェイとガイドラインの遵守は、術後の転帰の改善と医療システムのコスト削減につながることが示されている。
周術期死亡
周術期死亡のほとんどは、出血、敗血症、重要臓器の機能不全など、手術による合併症に起因する。過去数十年の間に、投与された麻酔薬の麻酔関連死亡率全体は大幅に改善された。監視装置、麻酔薬の進歩、周術期の安全性に対する関心の高まりなどが、周術期死亡率低下の理由である。米国では、現在推定される麻酔関連死亡率は、人口100万人あたり年間約1.1人である。死亡率が最も高いのは、老年人口、特に85歳以上の高齢者であった[72]。2018年のレビューでは、周術期の麻酔介入と麻酔関連死亡率への影響について検討された。死亡率を低下させることが判明した介入は、薬物療法、換気、輸血、栄養、血糖コントロール、透析、医療機器などである[73]。医師から別の医師への引継ぎと、患者の死亡率との関連には従来から議論があったが、2022年の無作為化比較試験では、引き継ぎ群と対照群と比較して死亡率に有意差がないことが示された[74]。
麻酔管理に直接関連する死亡例は非常に稀であるが、胃内容物の肺誤嚥[75]、 窒息[76]、アナフィラキシーが原因となることがある[77]。これらは、麻酔関連機器の故障や、より一般的にはヒューマンエラーによって起こる可能性がある。1984年、米国で放送された麻酔事故のテレビ番組をきっかけに、米国の麻酔科医Ellison C. Pierceは、米国麻酔科学会内に麻酔患者安全・リスク管理委員会を設置した[78]。この委員会は、麻酔に関連する罹患率や死亡率の原因を突き止め、低減させることを任務としていた[78]。この委員会から生まれた「麻酔患者安全財団」(英語: Anesthesia Patient Safety Foundation (APSF))は、「いかなる患者も麻酔によって害されることのないように」という目標を掲げ、1985年に独立非営利法人として設立された[79]。
稀ではあるが、重大な全身麻酔の合併症には悪性高熱がある[80][81]。 基幹病院では、この潜在的な合併症のために、手術室の近くに緊急用の薬剤(ダントロレン)を常備すべきとされる[82]。
脚注
注釈
出典
- ^ a b “Position on Monitored Anesthesia Care”. American Society of Anesthesiologists.. 2022年11月6日閲覧。 “Approved by the House of Delegates on October 25, 2005, and last amended on October 17, 2018”
- ^ 佐倉, 考信 (2021-10-01), 特集 麻酔 Part 1 麻酔総論(生理学)麻酔科医による術中管理の目的と実際 2.鎮痛薬総論-薬理作用,使用方法,使用上の注意点, 株式会社医学書院, doi:10.11477/mf.3102200904 2023年2月23日閲覧。
- ^ Woodbridge, Philip D. (1957-07-01). “CHANGING CONCEPTS CONCERNING DEPTH OF ANESTHESIAE”. Anesthesiology 18 (4): 536–550. doi:10.1097/00000542-195707000-00002. ISSN 0003-3022.
- ^ Michael A. Gropper, ed (2020). Miller's anesthesia (Ninth ed.). Philadelphia, PA: Elsevier. ISBN 978-0-323-61264-7. OCLC 1124935549
- ^ “Medical Renaissance”. Journal of Investigative Surgery 28 (3): 127–130. (June 2015). doi:10.3109/08941939.2015.1054747. PMID 26065591.
- ^ “Two Japanese Pioneers in Anesthesiology: Seishū Hanaoka and Gendai Kamada”. Journal of Anesthesia History 3 (1): 19–23. (January 2017). doi:10.1016/j.janh.2016.12.002. PMID 28160985.
- ^ “Asepsis and bacteriology: a realignment of surgery and laboratory science”. Medical History 56 (3): 308–334. (July 2012). doi:10.1017/mdh.2012.22. PMC 3426977. PMID 23002302.
- ^ “The Stages and Signs of General Anaesthesia”. British Medical Journal 2 (3996): 274–276. (August 1937). doi:10.1136/bmj.2.3996.274. PMC 2087073. PMID 20780832.
- ^ “General Anesthetics and Neurotoxicity: How Much Do We Know?”. Anesthesiology Clinics 34 (3): 439–451. (September 2016). doi:10.1016/j.anclin.2016.04.001. PMC 5477636. PMID 27521190.
- ^ “Plants, Like People, Succumb to Anesthesia”. Scientific American. (2018年1月26日) 2018年1月26日閲覧。
- ^ Moody, Olivia A.; Zhang, Edlyn R.; Vincent, Kathleen F.; Kato, Risako; Melonakos, Eric D.; Nehs, Christa J.; Solt, Ken (2021-05-01). “The Neural Circuits Underlying General Anesthesia and Sleep”. Anesthesia and Analgesia 132 (5): 1254–1264. doi:10.1213/ANE.0000000000005361. ISSN 1526-7598. PMC 8054915. PMID 33857967.
- ^ Lambert, David G. (2020-05-01). “Mechanisms of action of general anaesthetic drugs” (English). Anaesthesia & Intensive Care Medicine 21 (5): 235–237. doi:10.1016/j.mpaic.2020.02.006. ISSN 1472-0299.
- ^ Woll, Kellie A.; Zhou, Xiaojuan; Bhanu, Natarajan V.; Garcia, Benjamin A.; Covarrubias, Manuel; Miller, Keith W.; Eckenhoff, Roderic G. (August 2018). “Identification of binding sites contributing to volatile anesthetic effects on GABA type A receptors”. The FASEB Journal 32 (8): 4172–4189. doi:10.1096/fj.201701347R. ISSN 0892-6638. PMC 6044061. PMID 29505303.
- ^ Zhang, Youyi; Ye, Fei; Zhang, Tongtong; Lv, Shiyun; Zhou, Liping; Du, Daohai; Lin, He; Guo, Fei et al. (August 2021). “Structural basis of ketamine action on human NMDA receptors”. Nature 596 (7871): 301–305. Bibcode: 2021Natur.596..301Z. doi:10.1038/s41586-021-03769-9. ISSN 1476-4687. PMID 34321660.
- ^ “Studies on the mechanism of general anesthesia”. Proceedings of the National Academy of Sciences of the United States of America 117 (24): 13757–13766. (June 2020). Bibcode: 2020PNAS..11713757P. doi:10.1073/pnas.2004259117. PMC 7306821. PMID 32467161.
- ^ “全身麻酔薬(General Anesthetics) - 薬理学電子教科書 - Confluence”. drugacademy.atlassian.net. 2023年1月17日閲覧。
- ^ “Anesthetic considerations for lung resection: preoperative assessment, intraoperative challenges and postoperative analgesia”. Annals of Translational Medicine 7 (15): 356. (August 2019). doi:10.21037/atm.2019.03.67. PMC 6712248. PMID 31516902.
- ^ “Evaluation of preoperative risk factors for postpancreatectomy hemorrhage”. Langenbeck's Archives of Surgery 404 (8): 967–974. (December 2019). doi:10.1007/s00423-019-01830-w. PMC 6935390. PMID 31650216.
- ^ “Preoperative Interventions for Alcohol and Other Recreational Substance Use: A Systematic Review and Meta-Analysis”. Frontiers in Psychology 10: 34. (2019-02-04). doi:10.3389/fpsyg.2019.00034. PMC 6369879. PMID 30778307.
- ^ “Incidences and factors associated with perioperative cardiac arrest in trauma patients receiving anesthesia”. Risk Management and Healthcare Policy 11: 177–187. (2018-10-18). doi:10.2147/rmhp.s178950. PMC 6201994. PMID 30425598.
- ^ Michael A. Gropper, ed (2020). Miller's anesthesia (Ninth ed.). Philadelphia, PA: Elsevier. ISBN 978-0-323-61264-7. OCLC 1124935549
- ^ “Airway management and training in obstetric anaesthesia”. Current Opinion in Anesthesiology 29 (3): 261–267. (June 2016). doi:10.1097/ACO.0000000000000309. PMID 26844863.
- ^ “Institutional preparedness to prevent and manage anaesthesia-related 'can't intubate, can't oxygenate' events in Australian and New Zealand teaching hospitals”. Anaesthesia 75 (6): 767–774. (June 2020). doi:10.1111/anae.14909. PMID 31709522.
- ^ “Comparison of forces acting on maxillary incisors during tracheal intubation with different laryngoscopy techniques: a blinded manikin study”. Anaesthesia 74 (12): 1563–1571. (December 2019). doi:10.1111/anae.14815. PMID 314484046
- ^ Roth, Dominik; Pace, Nathan L.; Lee, Anna; Hovhannisyan, Karen; Warenits, Alexandra-Maria; Arrich, Jasmin; Herkner, Harald (2018-05-15). “Airway physical examination tests for detection of difficult airway management in apparently normal adult patients”. The Cochrane Database of Systematic Reviews 5 (5): CD008874. doi:10.1002/14651858.CD008874.pub2. ISSN 1469-493X. PMC 6404686. PMID 29761867.
- ^ a b c d e Michael A. Gropper, ed (2020). Miller's anesthesia (Ninth ed.). Philadelphia, PA: Elsevier. ISBN 978-0-323-61264-7. OCLC 1124935549
- ^ “Clonidine in paediatric anaesthesia: review of the literature and comparison with benzodiazepines for premedication”. Acta Anaesthesiologica Scandinavica 50 (2): 135–143. (February 2006). doi:10.1111/j.1399-6576.2006.00940.x. PMID 16430532.
- ^ “Premedication with clonidine is superior to benzodiazepines. A meta analysis of published studies”. Acta Anaesthesiologica Scandinavica 54 (4): 397–402. (April 2010). doi:10.1111/j.1399-6576.2009.02207.x. PMID 200855416
- ^ Vanderstappen, I.; Vandermeersch, E.; Vanacker, B.; Mattheussen, M.; Herijgers, P.; Van Aken, H. (1996-04). “The effect of prophylactic clonidine on postoperative shivering. A large prospective double-blind study”. Anaesthesia 51 (4): 351–355. doi:10.1111/j.1365-2044.1996.tb07747.x. ISSN 0003-2409. PMID 8686824.
- ^ Oddby-Muhrbeck, Eva; Eksborg, Staffan; Bergendahl, Henrik T. G.; Muhrbeck, Olle; Lönnqvist, Per Arne (2002-05). “Effects of clonidine on postoperative nausea and vomiting in breast cancer surgery”. Anesthesiology 96 (5): 1109–1114. doi:10.1097/00000542-200205000-00013. ISSN 0003-3022. PMID 11981150.
- ^ Bromfalk, Åsa; Myrberg, Tomi; Walldén, Jakob; Engström, Åsa; Hultin, Magnus (November 2021). Cravero, Joseph. ed. “Preoperative anxiety in preschool children: A randomized clinical trial comparing midazolam, clonidine, and dexmedetomidine” (英語). Pediatric Anesthesia 31 (11): 1225–1233. doi:10.1111/pan.14279. ISSN 1155-5645. PMID 34403548.
- ^ “Clonidine as a preoperative sedative”. Special Care in Dentistry 38 (2): 80–88. (March 2018). doi:10.1111/scd.12269. PMID 29364538.
- ^ Manning, Alexander N.; Bezzo, Leah K.; Hobson, Jamie K.; Zoeller, Justine E.; Brown, Courtney A.; Henderson, Kristin J. (October 2020). “Dexmedetomidine Dosing to Prevent Pediatric Emergence Delirium”. AANA Journal 88 (5): 359–364. ISSN 2162-5239. PMID 32990204.
- ^ El Batawi, Hisham Yehia (2015). “Effect of preoperative oral midazolam sedation on separation anxiety and emergence delirium among children undergoing dental treatment under general anesthesia”. Journal of International Society of Preventive & Community Dentistry 5 (2): 88–94. doi:10.4103/2231-0762.155728. ISSN 2231-0762. PMC 4415335. PMID 25992332.
- ^ “Melatonin and anesthesia: a clinical perspective”. Journal of Pineal Research 42 (1): 12–21. (January 2007). doi:10.1111/j.1600-079X.2006.00384.x. PMID 17198534.
- ^ “Melatonin for preoperative and postoperative anxiety in adults”. The Cochrane Database of Systematic Reviews 2020 (12): CD009861. (December 2020). doi:10.1002/14651858.CD009861.pub3. PMC 8092422. PMID 33319916.
- ^ “Perioperative beta-blockers for preventing surgery-related mortality and morbidity”. The Cochrane Database of Systematic Reviews 2018 (3): CD004476. (March 2018). doi:10.1002/14651858.CD004476.pub3. PMC 6494407. PMID 295334706
- ^ Wang, Rulin; Huang, Xin; Wang, Yuan; Akbari, Masod (2022-04-11). “Non-pharmacologic Approaches in Preoperative Anxiety, a Comprehensive Review”. Frontiers in Public Health 10: 854673. doi:10.3389/fpubh.2022.854673. ISSN 2296-2565. PMC 9035831. PMID 35480569.
- ^ a b “Non-pharmacological interventions for assisting the induction of anaesthesia in children”. The Cochrane Database of Systematic Reviews 2015 (7): CD006447. (July 2015). doi:10.1002/14651858.CD006447.pub3. PMC 8935979. PMID 26171895.
- ^ a b “The Stages and Signs of General Anaesthesia”. British Medical Journal 2 (3996): 274–276. (August 1937). doi:10.1136/bmj.2.3996.274. PMC 2087073. PMID 20780832.
- ^ “Effects of anesthesia on the respiratory system”. Best Practice & Research. Clinical Anaesthesiology 29 (3): 273–284. (September 2015). doi:10.1016/j.bpa.2015.08.008. PMID 26643094.
- ^ “Neurocirculatory responses to sevoflurane in humans. A comparison to desflurane”. Anesthesiology 83 (1): 88–95. (July 1995). doi:10.1097/00000542-199507000-00011. PMID 7605024.
- ^ “Standards for Basic Anesthetic Monitoring”. American Society of Anesthesiologists.. 2022年11月10日閲覧。 “Approved by the ASA House of Delegates on October 21, 1986, last amended on October 20, 2010, and reaffirmed on December 13, 2020”
- ^ “SponTaneous Respiration using IntraVEnous anaesthesia and Hi-flow nasal oxygen (STRIVE Hi) maintains oxygenation and airway patency during management of the obstructed airway: an observational study”. British Journal of Anaesthesia 118 (3): 444–451. (March 2017). doi:10.1093/bja/aew468. PMC 5409133. PMID 28203745.
- ^ “Injury during anaesthesia”. Continuing Education in Anaesthesia, Critical Care & Pain 6 (2): 67–70. (2006). doi:10.1093/bjaceaccp/mkl004.
- ^ “Care of the eye during anaesthesia and intensive care”. Anaesthesia & Intensive Care Medicine 15: 40–43. (2014). doi:10.1016/j.mpaic.2013.11.008.
- ^ Michael A. Gropper, ed (2020). Miller's anesthesia (Ninth ed.). Philadelphia, PA: Elsevier. ISBN 978-0-323-61264-7. OCLC 1124935549
- ^ “Sugammadex Versus Neostigmine for Reversal of Residual Neuromuscular Blocks After Surgery: A Retrospective Cohort Analysis of Postoperative Side Effects”. Anesthesia and Analgesia 134 (5): 1043–1053. (May 2022). doi:10.1213/ANE.0000000000005842. PMID 350206366
- ^ “Pharmacology of anaesthetic agents I: intravenous anaesthetic agents” (英語). Continuing Education in Anaesthesia Critical Care & Pain 14 (3): 100–105. (June 2014). doi:10.1093/bjaceaccp/mkt039. ISSN 1743-1816.
- ^ “Guidelines for the safe practice of total intravenous anaesthesia (TIVA): Joint Guidelines from the Association of Anaesthetists and the Society for Intravenous Anaesthesia”. Anaesthesia 74 (2): 211–224. (February 2019). doi:10.1111/anae.14428. PMID 303781026
- ^ “Loss of Smell and Taste After General Anesthesia: A Case Report”. A&A Case Reports 9 (12): 346–348. (December 2017). doi:10.1213/XAA.0000000000000612. PMID 28767470.
- ^ a b Michael A. Gropper, ed (2020). Miller's anesthesia (Ninth ed.). Philadelphia, PA: Elsevier. ISBN 978-0-323-61264-7. OCLC 1124935549
- ^ Absalom, Anthony R.; Glen, John Iain B.; Zwart, Gerrit J. C.; Schnider, Thomas W.; Struys, Michel M. R. F. (January 2016). “Target-Controlled Infusion: A Mature Technology”. Anesthesia and Analgesia 122 (1): 70–78. doi:10.1213/ANE.0000000000001009. ISSN 1526-7598. PMID 26516798.
- ^ Michael A. Gropper, ed (2020). Miller's anesthesia (Ninth ed.). Philadelphia, PA: Elsevier. ISBN 978-0-323-61264-7. OCLC 1124935549
- ^ a b “Postanaesthetic shivering - from pathophysiology to prevention” (英語). Romanian Journal of Anaesthesia and Intensive Care 25 (1): 73–81. (April 2018). doi:10.21454/rjaic.7518.251.xum. PMC 5931188. PMID 29756066.
- ^ “Comparison of perioperative oral multimodal analgesia versus IV PCA for spine surgery”. Journal of Spinal Disorders & Techniques 23 (2): 139–145. (April 2010). doi:10.1097/BSD.0b013e3181cf07ee. PMID 203758296
- ^ “Adductor canal blocks for postoperative pain treatment in adults undergoing knee surgery”. The Cochrane Database of Systematic Reviews 2019 (10). (October 2019). doi:10.1002/14651858.CD012262.pub2. PMC 6814953. PMID 31684698.
- ^ “The Effect of Transversus Abdominis Plane Block for Analgesia in Patients Undergoing Liver Transplantation: A Systematic Review and Meta-Analysis”. Turkish Journal of Anaesthesiology and Reanimation 47 (5): 359–366. (October 2019). doi:10.5152/tjar.2019.60251. PMC 6756312. PMID 31572985.
- ^ a b c “Towards an automated multimodal clinical decision support system at the post anesthesia care unit”. Computers in Biology and Medicine 101: 15–21. (October 2018). doi:10.1016/j.compbiomed.2018.07.018. PMID 30092398.
- ^ “Perioperative hyperoxia and post-operative cardiac complications in adults undergoing non-cardiac surgery: Systematic review protocol”. Acta Anaesthesiologica Scandinavica 62 (7): 1014–1019. (August 2018). doi:10.1111/aas.13123. PMID 29664117.
- ^ “Perioperative noninvasive cardiac output monitoring in parturients undergoing cesarean delivery with spinal anesthesia and prophylactic phenylephrine drip: a prospective observational cohort study”. The Journal of Maternal-Fetal & Neonatal Medicine 32 (19): 3153–3159. (October 2019). doi:10.1080/14767058.2018.1458835. PMID 296830076
- ^ Basics of Anesthesia, 5th Edition Authors: Robert K. Stoelting & Ronald D. Miller ISBN 978-0-443-06801-0
- ^ Lopez, Maria Bermudez (April 2018). “Postanaesthetic shivering – from pathophysiology to prevention”. Romanian Journal of Anaesthesia and Intensive Care 25 (1): 73–81. doi:10.21454/rjaic.7518.251.xum. ISSN 2392-7518. PMC 5931188. PMID 29756066.
- ^ “Effectiveness of active and passive warming for the prevention of inadvertent hypothermia in patients receiving neuraxial anesthesia: A systematic review and meta-analysis of randomized controlled trials”. Journal of Clinical Anesthesia 38: 93–104. (May 2017). doi:10.1016/j.jclinane.2017.01.005. PMC 5381733. PMID 28372696.
- ^ “Thermal insulation for preventing inadvertent perioperative hypothermia”. The Cochrane Database of Systematic Reviews (6): CD009908. (June 2014). doi:10.1002/14651858.CD009908.pub2. PMID 24895945.
- ^ “Predicting the efficacy of convection warming in anaesthetized children”. British Journal of Anaesthesia 103 (2): 275–282. (August 2009). doi:10.1093/bja/aep160. PMID 19541677.
- ^ “Comparison of two convective warming systems during major abdominal and orthopedic surgery”. Canadian Journal of Anaesthesia 55 (6): 358–363. (June 2008). doi:10.1007/BF03021491. PMID 18566199.
- ^ “Dexmedetomidine as a neuraxial adjuvant for prevention of perioperative shivering: Meta-analysis of randomized controlled trials”. PLOS ONE 12 (8): e0183154. (22 August 2017). Bibcode: 2017PLoSO..1283154Z. doi:10.1371/journal.pone.0183154. PMC 5567500. PMID 28829798.
- ^ “Efficacy and Safety of Dexmedetomidine as an Adjuvant in Epidural Analgesia and Anesthesia: A Systematic Review and Meta-analysis of Randomized Controlled Trials”. Clinical Drug Investigation 37 (4): 343–354. (April 2017). doi:10.1007/s40261-016-0477-9. PMID 27812971.
- ^ English W (2002). “Post-operative shivering, causes, prevention and treatment (letter)”. Update in Anaesthesia (15) 2023年1月21日閲覧。.
- ^ “Postoperative ileus-An ongoing conundrum”. Neurogastroenterology and Motility 33 (5): e14046. (May 2021). doi:10.1111/nmo.14046. PMID 332521796
- ^ Li, Guohua; Warner, Margaret; Lang, Barbara H.; Huang, Lin; Sun, Lena S. (April 2009). “Epidemiology of Anesthesia-related Mortality in the United States, 1999–2005”. Anesthesiology 110 (4): 759–765. doi:10.1097/aln.0b013e31819b5bdc. ISSN 0003-3022. PMC 2697561. PMID 19322941.
- ^ Boet, Sylvain; Etherington, Cole; Nicola, David; Beck, Andrew; Bragg, Susan; Carrigan, Ian D.; Larrigan, Sarah; Mendonca, Cassandra T. et al. (2018-11-30). “Anesthesia interventions that alter perioperative mortality: a scoping review”. Systematic Reviews 7 (1): 218. doi:10.1186/s13643-018-0863-x. ISSN 2046-4053. PMC 6267894. PMID 30497505.
- ^ Meersch, Melanie; Weiss, Raphael; Küllmar, Mira; Bergmann, Lars; Thompson, Astrid; Griep, Leonore; Kusmierz, Desiree; Buchholz, Annika et al. (2022-06-28). “Effect of Intraoperative Handovers of Anesthesia Care on Mortality, Readmission, or Postoperative Complications Among Adults: The HandiCAP Randomized Clinical Trial”. JAMA 327 (24): 2403–2412. doi:10.1001/jama.2022.9451. ISSN 1538-3598. PMC 9167439. PMID 35665794.
- ^ “Pulmonary aspiration of gastric contents in anaesthesia”. British Journal of Anaesthesia 83 (3): 453–460. (September 1999). doi:10.1093/bja/83.3.453. PMID 10655918.
- ^ “Maternal death from aspiration asphyxia”. British Medical Journal 2 (4983): 16–19. (July 1956). doi:10.1136/bmj.2.4983.16. PMC 2034767. PMID 13329366.
- ^ “Anaphylaxis and anesthesia: controversies and new insights”. Anesthesiology 111 (5): 1141–1150. (November 2009). doi:10.1097/ALN.0b013e3181bbd443. PMID 19858877.
- ^ a b Guadagnino C (2000年). “Improving anesthesia safety”. Narberth, Pennsylvania: Physician's News Digest, Inc.. 2010年8月15日時点のオリジナルよりアーカイブ。2010年9月8日閲覧。
- ^ Stoelting RK (2010年). “Foundation History”. Indianapolis, IN: Anesthesia Patient Safety Foundation. 2010年9月8日閲覧。
- ^ “The anaesthetist, opioid analgesic drugs, and serotonin toxicity: a mechanistic and clinical review”. British Journal of Anaesthesia 124 (1): 44–62. (January 2020). doi:10.1016/j.bja.2019.08.010. PMID 31653394.
- ^ “Malignant Hyperthermia: A Clinical Review”. Advances in Anesthesia 37: 35–51. (December 2019). doi:10.1016/j.aan.2019.08.003. PMID 31677658.
- ^ “Safe duration of postoperative monitoring for malignant hyperthermia susceptible patients”. Anaesthesia and Intensive Care 32 (4): 502–509. (August 2004). doi:10.1177/0310057X0403200407. PMID 15675210.
関連項目
参考文献
- 周術期管理チームテキスト 第3版, 公益社団法人 日本麻酔科学会(発行), 2016年8月10日発行
外部リンク
- Chloroform: The molecular lifesaver ブリストル大学の論文で、クロロホルムに関する興味深い事実が紹介されている(英語)。
- Australian & New Zealand College of Anaesthetists Monitoring Standard オーストラリア・ニュージーランド麻酔学会(ANZCA)のモニター基準(英語)
- Royal College of Anaesthetists Patient Information page 英国王立麻酔科協会の患者向けサイト(英語)
