第一級アルコールからカルボン酸への酸化
本項では、有機化学における重要な酸化反応である第一級アルコールからカルボン酸への酸化(だいいっきゅうアルコールからカルボンさんへのさんか)について記述する。
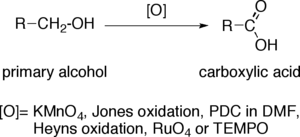
第一級アルコールをカルボン酸に変換すると、末端炭素原子の酸化数は4に増加する。酸化剤によってこの操作を有機分子に対して行うことができるが、酸化に対して敏感な官能基がある場合そちらも酸化されてしまうため、選択制が重要となる。一般的な酸化剤には過マンガン酸カリウム (KMnO4)、ジョーンズ試薬、DMF中のPDC、四酸化ルテニウム (RuO4) およびTEMPOなどがある。
過マンガン酸カリウム
過マンガン酸カリウム (KMnO4) は、第二級アルコール、1,2-ジオール、アルデヒド、アルケン、オキシム、スルフィドそしてチオールなど多くの官能基を酸化する非常に強力な酸化剤である。管理条件下では、KMnO4は非常に効率よく第一級アルコールをカルボン酸に酸化する。この反応は一般にKMnO4をアルカリ性水溶液のアルコール溶液または懸濁液に加えると起こり、Fournierによって初めて詳細に記述された[1][2]。この混合溶液を酸化が終わるまで撹拌する。この反応を効率的に反応させるためにはアルコールは少なくとも部分的には溶解させる必要がある。ジオキサン、ピリジン、アセトンまたはt-BuOHなど有機共溶媒を添加することにより反応を進行させることもできる。KMnO4は、第一級アルコールを酸化する前に炭素-炭素二重結合と容易に反応する。
ふつう、この酸化は大きな酸化速度と選択制のために、1N NaOHまたはKOHの強アルカリ性条件下で行われる。基質が強塩基に適さない場合、低pHまたは酸性条件下でも反応は進行するが、反応速度は大幅に低下する。

KMnO4は水中で二酸化マンガン (MnO2) と気体の酸素に分解する。この分解は酸、塩基およびMnO2に触媒される。この分解の度合いは第一級アルコールの酸化中は推定が難しく、酸化が終了するまでKMnO4を加えることによって調節しなければならない。
ジョーンズ酸化
硫酸水溶液に三酸化クロムを溶かすとクロム酸 (H2CrO4) を含む赤みを帯びた溶液となる。これがジョーンズ試薬である。ジョーンズ試薬をアセトンの一級アルコール溶液に加えると(ジョーンズにより初めて報告された[4][5])、一級アルコールがカルボン酸に酸化される。この古典的手法は相当な量のエステルが形成するにも関わらず頻繁に使われている。 HollandとGilman[6]は、この副反応は第一級アルコールのアセトン溶液をできるだけ希釈したジョーンズ試薬に加えるという、"逆に添加する"手法にすることにより抑えられることを証明した。
ジョーンズ試薬を第二級アルコールとも反応しケトンを生じる。第一級および第二級アルコールを含む化合物にジョーンズ試薬を反応させるとケト酸が生成する。
出典
- ^ Fournier, H.M. (1907), Compt. Rend. Chim.: 331
- ^ Fournier, H.M. (1909), Bull. Soc. Chim. Fr.: 920
- ^ Ciufolini, M.A.; Swaminathan, S. (1989). “Synthesis of a model depsipeptide segment of Luzopeptins (BBM 928), potent antitumor and antiretroviral antibiotics”. Tetrahedron Lett. 30 (23): 3027. doi:10.1016/S0040-4039(00)99393-6.
- ^ Heilbron, I.; Jones, E.R.H.; Sondheimer, F. (1947). “315. Researches on acetylenic compounds. Part XIV. A study of the reactions of the readily available ethynyl-ethylenic alcohol, pent-2-en-4-yn-1-ol”. J. Chem. Soc.: 1586. doi:10.1039/jr9470001586.
- ^ Heilbron, I.; Jones, E.R.H. (1949). “129. Researches on acetylenic compounds. Part XV. The oxidation of primary acetylenic carbinols and glycols”. J. Chem. Soc.: 604. doi:10.1039/jr9490000604.
- ^ Holland, B.C.; Gilman, N.W. (1974). “An Improved Procedure for the Oxidation of Alkynols to Alkynoic Acids”. Synth. Commun. 4 (4): 203. doi:10.1080/00397917408062073.
参考文献
- Marcos Fernández; Gabriel Tojo (2006). Oxidation of Primary Alcohols to Carboxylic Acids: A Guide to Current Common Practice (Basic Reactions in Organic Synthesis). Berlin: Springer. ISBN 0-387-35431-X
