フィセチン
| フィセチン | |
|---|---|
| |
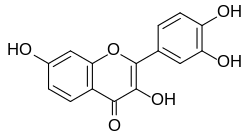
2-(3,4-dihydroxyphenyl)-3,7-dihydroxychromen-4-one | |
別称 Cotinin (not to be confused with Cotinine) 5-Desoxyquercetin Superfustel Fisetholz Fietin Fustel Fustet Viset Junger fustik | |
| 識別情報 | |
| CAS登録番号 | 528-48-3 |
| PubChem | 5281614 |
| ChemSpider | 4444933 |
| 日化辞番号 | J1.584I |
| DrugBank | DB07795 |
| KEGG | C10041 |
| ChEBI | |
| ChEMBL | CHEMBL31574 |
| |
| |
| 特性 | |
| 化学式 | C15H10O6 |
| モル質量 | 286.2363 g/mol |
| 精密質量 | 286.047738 |
| 融点 |
330 °C |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
フィセチン(fisetin)は、ポリフェノール類のフラボノイド群に属する構造的に特徴のある化学物質であるフラボノールの一種である。多くの植物に含まれており、色素剤として作用している。フィセチンの化学式はオーストリアの化学者Josef Herzigによって1891年に初めて明らかにされた[1]。
フィセチンは、Acacia greggii[2]、Acacia berlandieri[2]、ハグマノキの黄色色素、ハナモツヤクノキ、アメリカサイカチ(ハニーローカスト)、Quebracho colorado、ヌルデ属植物[3]、アラスカヒノキといった様々な植物に含まれている。イチゴにはフィセチンが豊富に含まれている[4]。
生物活性[編集]
フィセチンは、サーチュインを制御する強力なサーチュイン活性化化合物 (STAC) である[5]。したがって、フィセチンは、出芽酵母[5]、線虫 C. elegans[6]、キイロショウジョウバエ[6]といったモデル生物において加齢効果を緩和することができる薬剤であるカロリー制限ミメティック候補である。こういった効果がヒトでも再現されるかは現在明らかになっておらず、科学的研究および論争の的となっている。
老化における効果は別として、様々なin vitroにおける研究によってフィセチンが異なる複数の培養細胞株において抗炎症[7][8]、抗発がん[9][10]作用を示すことが明らかにされている。しかしながら、in vitro実験は体内においてフィセチンが受ける代謝をほとんどあるいは全く反映していないため、in vivoにおけるフィセチンの実際の効果を正確に反映していない可能性がある。
構造的に類縁のフラボノールであるクェルセチンといった多くのその他のフラボノイドと同様に、フィセチンは強力な抗酸化物質である。フィセチンの抗酸化活性はその構造特性[11]やある細胞シグナル伝達経路、特にプロテインキナーゼおよび脂質キナーゼ経路を制御する活性に因ると考えられている。例えば、フィセチンは転写因子Nrf2を誘導し[12]、いくつかの防御および抗酸化遺伝子の発現を増強させることが明らかにされている。
ソーク研究所での研究では、フィセチンが記憶力を改善し、アルツハイマー病の発病から脳を保護する可能性や、糖尿病による腎障害の低減に有効である可能性が示されている[4]。
副作用[編集]
その他のフラボノイドの中でフィセチンは強力なトポイソメラーゼ阻害剤であることが明らかになっている[13]。この作用は、抗発がん効果ならびに発がん効果の両方の原因となる可能性がある[14]。フィセンチンは、(稀な)小児白血病のリスクを増加させる疑いが持たれている[15]。
脚注[編集]
- ^ Herzig, J. (1891). “Studien über Quercetin und seine Derivate, VII. Abhandlung [Studies on Quercetin and its Derivatives, Treatise VII]” (German). Monatshefte für Chemie 12 (1): 177–90. doi:10.1007/BF01538594.
- ^ a b Forbes TDA, Clement BA. “Chemistry of Acacia's from South Texas” (PDF). Texas A&M Agricultural Research and Extension Center at. 2011年5月16日時点のオリジナルよりアーカイブ。2010年4月14日閲覧。
- ^ Gábor, M.; Eperjessy, E. (1966). “Antibacterial Effect of Fisetin and Fisetinidin”. Nature 212 (5067): 1273. doi:10.1038/2121273a0. PMID 21090477.
- ^ a b Maher, Pamela; Dargusch, Richard; Ehren, Jennifer L.; Okada, Shinichi; Sharma, Kumar; Schubert, David (2011). Deli, Maria A.. ed. “Fisetin Lowers Methylglyoxal Dependent Protein Glycation and Limits the Complications of Diabetes”. PLoS ONE 6 (6): e21226. doi:10.1371/journal.pone.0021226. PMC 3124487. PMID 21738623. 非専門家向けの内容要旨 – ScienceDaily (June 28, 2011).
- ^ a b Howitz, Konrad T.; Bitterman, Kevin J.; Cohen, Haim Y.; Lamming, Dudley W.; Lavu, Siva; Wood, Jason G.; Zipkin, Robert E.; Chung, Phuong et al. (2003). “Small molecule activators of sirtuins extend Saccharomyces cerevisiae lifespan”. Nature 425 (6954): 191–6. doi:10.1038/nature01960. PMID 12939617.
- ^ a b Wood, Jason G.; Rogina, Blanka; Lavu, Siva; Howitz, Konrad; Helfand, Stephen L.; Tatar, Marc; Sinclair, David (2004). “Sirtuin activators mimic caloric restriction and delay ageing in metazoans”. Nature 430 (7000): 686–9. doi:10.1038/nature02789. PMID 15254550.
- ^ Geraets, Liesbeth; Haegens, Astrid; Brauers, Karen; Haydock, Jane A.; Vernooy, Juanita H.J.; Wouters, Emiel F.M.; Bast, Aalt; Hageman, Geja J. (2009). “Inhibition of LPS-induced pulmonary inflammation by specific flavonoids”. Biochemical and Biophysical Research Communications 382 (3): 598–603. doi:10.1016/j.bbrc.2009.03.071. PMID 19292976.
- ^ Park, Hyo-Hyun; Lee, Soyoung; Son, Hee-Young; Park, Seung-Bin; Kim, Mi-Sun; Choi, Eun-Ju; Singh, Thoudam S. K.; Ha, Jeoung-Hee et al. (2008). “Flavonoids inhibit histamine release and expression of proinflammatory cytokines in mast cells”. Archives of Pharmacal Research 31 (10): 1303–11. doi:10.1007/s12272-001-2110-5. PMID 18958421.
- ^ Lim, D. Y.; Park, J. H. Y. (2009). “Induction of p53 contributes to apoptosis of HCT-116 human colon cancer cells induced by the dietary compound fisetin”. AJP: Gastrointestinal and Liver Physiology 296 (5): G1060–8. doi:10.1152/ajpgi.90490.2008.
- ^ Khan, N.; Afaq, F.; Syed, D. N.; Mukhtar, H. (2008). “Fisetin, a novel dietary flavonoid, causes apoptosis and cell cycle arrest in human prostate cancer LNCaP cells”. Carcinogenesis 29 (5): 1049–56. doi:10.1093/carcin/bgn078. PMC 2902387. PMID 18359761.
- ^ Williams, Robert J; Spencer, Jeremy P.E; Rice-Evans, Catherine (2004). “Flavonoids: Antioxidants or signalling molecules?”. Free Radical Biology and Medicine 36 (7): 838–49. doi:10.1016/j.freeradbiomed.2004.01.001. PMID 15019969.
- ^ Hanneken, A.; Lin, FF; Johnson, J; Maher, P (2006). “Flavonoids Protect Human Retinal Pigment Epithelial Cells from Oxidative-Stress-Induced Death”. Investigative Ophthalmology & Visual Science 47 (7): 3164–77. doi:10.1167/iovs.04-1369. PMID 16799064.
- ^ Olaharski, A.J.; Mondrala, S.T.; Eastmond, D.A. (2005). “Chromosomal malsegregation and micronucleus induction in vitro by the DNA topoisomerase II inhibitor fisetin”. Mutation Research/Genetic Toxicology and Environmental Mutagenesis 582 (1–2): 79–86. doi:10.1016/j.mrgentox.2005.01.002. PMID 15781213.
- ^ López-Lázaro, Miguel; Willmore, Elaine; Austin, Caroline A. (2010). “The dietary flavonoids myricetin and fisetin act as dual inhibitors of DNA topoisomerases I and II in cells”. Mutation Research/Genetic Toxicology and Environmental Mutagenesis 696 (1): 41–7. doi:10.1016/j.mrgentox.2009.12.010. PMID 20025993.
- ^ Spector, L. G.; Xie, Y; Robison, LL; Heerema, NA; Hilden, JM; Lange, B; Felix, CA; Davies, SM et al. (2005). “Maternal Diet and Infant Leukemia: The DNA Topoisomerase II Inhibitor Hypothesis: A Report from the Children's Oncology Group”. Cancer Epidemiology Biomarkers & Prevention 14 (3): 651–5. doi:10.1158/1055-9965.EPI-04-0602. PMID 15767345.
